年龄相关性黄斑变性(age-related macular degeneration, AMD)是一种复杂的、多因素的黄斑退行性疾病,是60岁以上成年人失明的主要原因[1]。据估计,AMD的全球流行率为8.7%,到2040年,这一患病群体将增加至近3亿人[1],我国2015年的一项调查显示,AMD的患病率在5.2%左右,约有2 665万人受到影响[2]。
AMD的发生与多种因素有关,是衰老、遗传易感性和环境风险因素之间的复杂相互作用,其中年龄增长是最严重的风险因素[3]。早期AMD的病理表现为玻璃膜疣,这是一种在视网膜色素上皮下局灶性或弥漫性富含脂蛋白的沉积,晚期AMD则根据有无脉络膜新生血管可分为湿性AMD(又称新生血管性AMD)和干性AMD(又称萎缩性AMD)两类[4]。干性AMD的病理特征是视网膜和脉络膜毛细血管萎缩融合,晚期出现地图状萎缩(geographic atrophy, GA),监测GA区域进展的金标准是眼底自发荧光(fundus autofluorescence, FAF),其表现为低自发荧光信号。
目前抗血管内皮生长因子治疗的出现为治疗湿性AMD带来了巨大的变革,但针对干性AMD的治疗进展相对缓慢。补充维生素和抗氧化剂虽然可以降低进展到晚期黄斑变性的风险,但似乎无法延缓GA的发生和发展[5-9]。
近年来,遗传和流行病学研究确定了数十个与AMD的发展风险相关的遗传变异,其中许多与补体系统有关,补体级联失调也被认为与干性AMD的进展密切相关[10-12]。鉴于补体系统和AMD之间的潜在联系,补体相关疗法已成为治疗GA的一种策略。本文主要介绍补体激活途径、补体过度激活致GA发生和发展的研究证据以及针对补体系统不同靶点的药物研发进展。
1 补体系统在GA发生发展中的作用机制
1.1 补体级联途径
补体系统已被证实在GA的发生和发展过程中发挥着重要作用[13-15]。补体作用途径包括经典途径、替代途径、凝集素途径,均通过形成C3转化酶、C5转化酶最终合成攻膜复合物而发挥作用。
在经典途径中,由免疫复合沉积物激活补体C1,从而启动补体级联[16]。首先,抗原抗体复合物中暴露的Fc段与C1复合体中的C1q相结合,启动C1复合体的构象变化,从而激活具有切割能力的丝氨酸蛋白酶单元(C1r、C1s),丝氨酸蛋白酶单元将C4和C2切割成较小的C4b和C2a片段以及较大的C4a和C2b片段[17],前者共同组成C3转化酶(C4bC2a),从而获得切割C3的能力。凝集素途径是通过甘露糖结合凝集素等模式识别受体识别病原体表面或凋亡、坏死细胞表面的病原体相关分子模式[18],激活下游的C2和C4,从而产生C3转化酶(C4bC2a)[19]。替代途径的激活则是通过血浆中C3的自发水解生成C3(H2O),后者与CFB结合,形成的复合物经CFD的切割作用成为C3转化酶[C3(H2O)Bb][16,20]。
三种途径形成的C3转化酶切割C3形成活化的C3a和C3b,C3b与C3转化酶(C4bC2a)结合形成C5转化酶C4bC2aC3b(经典途径和凝集素途径)和C3bBbC3b(替代途径)。然后C5转化酶将C5切割成C5a和C5b,前者可能参与炎症小体的启动和激活[21],后者相继与C6、C7、C8结合,形成C5b-8,最后C5b-8促进众多C9分子的结合和聚合形成稳定的膜攻击复合物C5b-9(membrane attack complex, MAC)。MAC能够插入外来病原体的细胞膜,导致细胞裂解死亡,从而发挥补体作用[19,22-23],见图1。

图1 补体级联途径及补体相关药物作用靶点
Fig.1 The complement cascade pathway and targets of drugs related complement
1.2 补体过度激活致GA发生和发展的研究证据
AMD的发病机制十分复杂,但多项研究表明补体过度激活是GA发生和发展的关键组成部分。
有研究发现,补体的过度激活贯穿AMD发生发展的各个阶段。与非AMD对照相比,AMD患者的全身补体激活水平更高,而与其他AMD分期相比,中度AMD和GA患者的补体活化水平相对更高[24]。在AMD患者眼底玻璃膜疣和富含脂质和蛋白质的沉积物中均发现有大量补体激活产物的积累[25-27]。一系列证据表明补体过度激活导致AMD的发生发展与视网膜细胞外基质(extracellular matrix, ECM)和Bruch膜的变化、脂质沉积、慢性炎症、氧化应激等密切相关[28]。
全基因组关联研究发现补体替代途径是AMD的主要驱动部分[29]。目前已知最强遗传风险因素是CFH位点,该位点可表达补体因子H(CFH)、H因子样蛋白1(FHL-1)及补体因子H相关蛋白1-5(FHR1-5)。其中,CFH/FHL-1是补体的负调节因子,它们允许CFI介导的C3b在ECM等非细胞表面切割[30],同时CFH可以物理取代C3b中的FB,从而加速C3bBb转化酶的代谢[31]。而FHR1和FHR5可与ECM相互作用,降低CFH活性,从而增强补体活化[32]。研究发现,携带CFH罕见编码变异的AMD患者的血浆CFH水平显著降低[33],FHR4水平升高与AMD风险增加有关[34]。除了Bruch膜和脉络膜毛细血管外,在AMD患者的玻璃膜疣中也发现了FHR2、FHR4和FHR5蛋白。补体因子I(CFI)是一种丝氨酸蛋白酶,可以将沉积在任何表面的C3b切割成无活性的C3b,从而直接减慢并阻止下游补体激活。有研究发现血浆CFI水平降低与晚期AMD相关[35],与非携带者相比,CFI Gly119Arg变体的携带者更有可能进入终末期干性AMD[36]。除此之外,AMD患者脉络膜中的MAC积累会显著增加,在GA病变边缘的RPE上最为明显[37]。有研究在AMD人诱导多能干细胞(induced pluripotent stem cell, iPSC)衍生的脉络膜内皮细胞(choroidal endothelial cell, CEC)模型上发现,局部CEC产生的CFH可以防止MAC沉积,增加局部CFH蛋白可能有益于限制AMD中的MAC沉积[38]。值得注意的是,虽然许多研究发现补体基因变异与AMD的存在有很强的关联,但风险相关基因变异与AMD进展之间没有明确的关联[39-41]。
2 针对补体系统不同靶点的药物研发进展
目前研究的药物针对补体激活途径的潜在靶点包括C1q、C3、C5、CFB、CFD、CFH、CFI和MAC,依据药物形式可分为生物大分子药物、化学小分子药物及基因治疗药物,详见表1。
表1 针对补体级联途径中各靶点的临床试验药物
Tab.1 The drugs of clinical trials targeting sites in the complement cascade pathway

靶点药物作用机制给药方式研究阶段NCT编码开始时间主要终点状态C3APL-2聚乙二醇化肽抑制剂玻璃体腔内注射Ⅱ期NCT025033322015达到完成Ⅲ期NCT035256132018达到完成Ⅲ期NCT037773322021达到进行中Ⅲ期NCT047705452021达到进行中POT-4NCT01603043衍生物玻璃体腔内注射Ⅱ期NCT016030432012未达到终止NGM621人源化单克隆抗体玻璃体腔内注射Ⅱ期NCT044659552020未达到完成Cp40-KKKCompstatin衍生物玻璃体腔内注射动物实验C5Zimura®聚乙二醇化RNA 适体玻璃体腔内注射Ⅰ期NCT009506382009达到完成Ⅱ/Ⅲ期NCT026866582016达到完成Ⅲ期NCT044353662020达到进行中Eculizumab人源化单克隆抗体玻璃体腔内注射Ⅱ期NCT009358832009未达到完成LFG316人源化单克隆抗体玻璃体腔内注射Ⅱ期NCT015275002012未达到完成Lampalizumab人源化单克隆抗体玻璃体腔内注射Ⅲ期NCT02247479NCT022475312014未达到终止Ⅲ期NCT027451192016未达到终止CFDALXN2040可逆小分子CFD抑制剂口服Ⅱ期NCT050195212021进行中CFHGEM103重组人CFH玻璃体腔内注射Ⅰ期NCT042468662020达到完成Ⅱ期NCT046438862020进行中AdCAGfH腺相关病毒载体临床前研究C1qANX007重组单克隆抗体抗原结合片段玻璃体腔内注射Ⅱ期NCT046565612020进行中CFBIONIS-FB-LRx特异性反义寡核苷酸皮下注射Ⅱ期NCT038158252019进行中MACHMR59腺相关病毒载体玻璃体腔内注射Ⅰ期NCT031449992017达到完成Ⅱ期NCT043584712020进行中CFIGT005腺相关病毒载体视网膜下注射Ⅰ/Ⅱ期NCT038461932019进行中Ⅱ期NCT04437368NCT045664452020进行中
2.1 生物大分子药物
生物大分子药物分子量大,结构多为蛋白质、核酸片段,需通过局部或全身注射等方式发挥作用,其作用效果迅速,可外源性补充补体级联途径的各类成分,从而下调补体级联,是目前GA治疗药物的主要研究类型。
2.1.1 针对补体因子C3的生物大分子药物 NGM621是一种由NGM公司设计的人源化的IgG单克隆抗体,经玻璃体腔注射(intravitreal injection, IVT)给药。在已完成的Ⅰ期临床试验中,该药物显示出良好的安全性,未出现眼内炎、脉络膜新生血管(choroidal neovascularization, CNV)等不良事件[42]。正在进行的多中心随机对照Ⅱ期临床试验(CATALINA)中,有320名GA患者进行了为期52周的NGM621治疗,试验结束时每4周(Q4W, n=108)注射组和每8周(Q8W, n=104)注射组的GA面积变化率分别降低了6.3%和6.5%,与假注射组相比,差异均未达到统计学意义。试验过程中未发生与药物相关的严重不良事件。对基线GA病变面积在2.5![]() 17.5 mm2的患者(25%
17.5 mm2的患者(25%![]() 75%)进行亚组分析,试验结束时Q4W组GA面积变化率降低21.9%(n=55,P=0.02),经重复测量的混合效应模型分析,其GA面积变化率为20.6%(P=0.024),显示出NGM621良好的疗效。此发现为NGM621治疗GA提供了进一步研究的可能。
75%)进行亚组分析,试验结束时Q4W组GA面积变化率降低21.9%(n=55,P=0.02),经重复测量的混合效应模型分析,其GA面积变化率为20.6%(P=0.024),显示出NGM621良好的疗效。此发现为NGM621治疗GA提供了进一步研究的可能。
Pegcetacoplan(又称APL-2)是由Apellis公司研制的一种经IVT注射的C3补体抑制剂。Ⅱ期临床试验(FILLY)到达了主要研究终点[43],在排除中心凹外病变和较大的低亮度视力缺损(low-luminance deficit, LLD)等GA的潜在危险因素后,Pegcetacoplan的治疗仍旧能够显著控制GA的进展[44-45]。Apellis公司开展了两项随机对照Ⅲ期临床试验(OAKS和DERBY),分别有637名和621名GA患者参与为期24个月的治疗,其中OAKS试验中每月注射组和隔月注射组的GA生长速度较假注射组分别减少22%(P<0.000 1)和18%(P=0.000 2),而DERBY试验每月注射组和隔月注射组的GA生长速度较假注射组分别减少19%(P=0.000 4)和16%(P=0.003 0),两项试验均提示在治疗的第18![]() 24个月,GA的生长速度更加缓慢。事后分析发现,与假注射组相比,每月和隔月注射Pegcetacoplan能保留GA病变边界附近视网膜细胞的视觉功能。目前正在进行一项Ⅲ期开放标签的多中心扩展研究(GALE),旨在评估Pegcetacoplan在GA患者中的长期安全性和有效性。研究发现,在Pegcetacoplan治疗的第24至30个月期间,与假注射组相比,每月注射组中非中心凹下的GA生长速度减少了45%,显示出Pegcetacoplan治疗的长期有效性。值得欣喜的是,美国食品和药品监督管理局(Food and Drug Administration, FDA)已批准SYFOVRETM(Pegcetacoplan)用于治疗AMD所致GA,这是GA治疗领域的一大进步。
24个月,GA的生长速度更加缓慢。事后分析发现,与假注射组相比,每月和隔月注射Pegcetacoplan能保留GA病变边界附近视网膜细胞的视觉功能。目前正在进行一项Ⅲ期开放标签的多中心扩展研究(GALE),旨在评估Pegcetacoplan在GA患者中的长期安全性和有效性。研究发现,在Pegcetacoplan治疗的第24至30个月期间,与假注射组相比,每月注射组中非中心凹下的GA生长速度减少了45%,显示出Pegcetacoplan治疗的长期有效性。值得欣喜的是,美国食品和药品监督管理局(Food and Drug Administration, FDA)已批准SYFOVRETM(Pegcetacoplan)用于治疗AMD所致GA,这是GA治疗领域的一大进步。
AMY-106(又称Cp40-KKK, Amyndas Pharmaceuticals)是由Amyndas公司研制的非聚乙二醇化的第四代Compstatin衍生物。其药代动力学表明[46],该药物在眼内停留时间可达3个月以上。有研究表明,聚乙二醇滞留在眼内,可能提高GA患者发生CNV的概率。因此,Cp40-KKK可能会在提高AMD患者的疗效、减少给药频率和降低与聚乙二醇相关的不良事件风险方面带来益处。
2.1.2 针对补体因子C5的生物大分子药物 Avacincaptad pegol(又称Zimura®)是由IVERIC公司开发的一种补体C5的强效特异性抑制剂,其结构为聚乙二醇化的RNA适体,能抑制C5的切割,进而发挥作用。在一项为期18个月的Ⅱ/Ⅲ期临床试验中(GATHER1),试验结果达到了主要研究终点,且未发生严重眼内不良反应或眼内炎[47]。事后分析提示Zimura®具有保留GA患者中心视力的潜力,可能延长GA患者的生活质量[48]。IVERIC进行了一项多中心的随机对照Ⅲ期临床试验(GATHER2)[49],共招募448名参与者,以评估每月2 mg经IVT注射Zimura®对GA患者的有效性和安全性。在前12个月中,患者被随机分配每月接受Zimura®2 mg或假注射。在第12个月至第23个月期间,Zimura®组的参与者被重新随机分配至每个月一次或每隔一个月注射Zimura®2 mg。主要终点为治疗12个月内经FAF测量的GA区域的平均增长率。治疗12个月后,每月注射组的GA区域的平均增长率较假注射组降低了14.3%(P=0.006 4)。试验过程中未发生眼内炎、缺血性视神经病变等严重不良事件,每月注射组中7%的患者出现了CNV。事后分析表明,接受Zimura®2 mg治疗的患者在治疗的前12个月内视力丧失率较假注射组降低了56%(HR=0.44,95%CI: 0.21![]() 0.92),提示Zimura®2 mg有助于减缓视力丧失。目前,FDA已授予Zimura®在治疗GA领域首个突破性疗法的称号,该公司也已向FDA提交新药申请。
0.92),提示Zimura®2 mg有助于减缓视力丧失。目前,FDA已授予Zimura®在治疗GA领域首个突破性疗法的称号,该公司也已向FDA提交新药申请。
令人遗憾的是,C5抑制剂Eculizumab(Alexion)和LFG316(Novartis)的Ⅱ期临床试验均未能阻止GA的进展,以失败告终[50]。
2.1.3 针对补体因子C1q的生物大分子药物 ANX007是由Annexon公司设计的一种单克隆抗体抗原结合片段(Fab),旨在通过阻断C1q和整个经典途径来保护感光细胞和视网膜功能。动物试验中显示安全性和耐受性良好,单次给药后,ANX007半衰期约为3 d,4周内均可测量玻璃体游离药物水平[51]。目前正在进行一项随机对照的Ⅱ期临床试验,纳入270名患者,所有患者以2∶2∶1∶1的比例被随机分为4组: 每个月5 mg、每隔1个月5 mg、每个月假注射、每隔1个月假注射,进行为期12个月的治疗,观察期为6个月,主要终点是经FAF测量的GA面积的变化率。中期结果表明ANX007治疗12个月后,未能达到主要终点。但值得注意的是,与假注射组相比,每个月5 mg组、每隔1个月5 mg组的BCVA≥15个字母丢失率分别减少了74%和47%,这显示出ANX007良好的视力保护潜力。目前该试验仍在进行为期6个月的随访。
2.1.4 针对补体因子B的生物大分子药物 IONIS-FB-LRx(IONIS)是由IONIS和Roche公司联合开发的一种针对人CFB基因的特异性反义寡核苷酸(antisense oligonucleotide, ASO),通过与FB mRNA结合从而抑制补体因子B基因表达[52-53]。有关该药物的一项Ⅰ期临床试验结果显示,与对照组相比,皮下注射IONIS-FB-LRx10 mg和20 mg后,GA患者血浆FB浓度分别下降约56%和72%,呈剂量依赖关系,且未出现严重眼内不良反应等安全事件[54]。目前正在进行一项Ⅱ期多中心双盲安慰剂对照临床试验,以进一步评估IONIS-FB-LRx对AMD患者GA面积变化率的影响,该试验共招募330名患者,治疗周期为49周,预计2026年完成试验。
2.1.5 针对补体因子H的生物大分子药物 GEM103是由Gemini公司开发的一种新型的重组人补体因子H,体外研究表明GEM103与天然CFH活性相当[55]。经IVT注射GEM103旨在恢复AMD患者眼内适当的替代途径调节。该药物Ⅰ期临床试验结果显示,在受试的12名GA患者中,IVT注射GEM103后CFH水平以剂量依赖的方式增加,在用药第1周即观察到超生理学水平;在所有接受单剂≥100 μg的参与者中,血清药物浓度持续时间≥8周,未出现与药物相关的眼部或全身不良事件,未发生眼内炎或CNV,显示出良好的安全性和耐受性[56]。目前正在进行一项多中心的Ⅱa期临床试验(ReGAtta),以探究重复IVT注射GEM103的安全性、耐受性、药效学和免疫原性,初步结果表明,经过9个月治疗,GEM103具有良好的耐受性,能够持久地降低补体激活的生物标志物,并能够维持CFH的超生理水平。目前Gemini公司正着手扩大GEM103的治疗范围,计划用于湿性AMD的辅助治疗。
2.2 小分子药物
化学小分子药物的分子量小,可以口服经消化道吸收,相比于玻璃体腔注药和视网膜下注射,用药方式更加简便,能够提高患者的依从性,方便AMD人群的管理。目前GA发病机制尚不明确,其分子调控机制仍有待进一步研究,阻碍了该类药物的研发。
针对补体因子D的小分子药物,如Danicopan(又称ALXN2040)是由Alexion公司开发的一种口服的选择性CFD抑制剂,通过与CFD蛋白酶相结合以抑制CFD的产生,从而减少替代途径中C3转化酶的生成,达到补体抑制的作用。由于补体经典途径和凝集素途径的激活不需要CFD,选择性CFD抑制可避免补体过度抑制,因此可以降低细菌感染的风险[57]。目前正在进行一项Ⅱ期临床试验,旨在评估Danicopan在GA患者中的疗效、安全性和药代动力学特征。该试验共招募330名,共分为4个治疗组: 100 mg每日2次、200 mg每日2次、400 mg每日1次以及安慰剂组,主要研究终点为治疗52周时经FAF测量的GA病变区域的平均变化率。该试验研究周期包括4周的筛选期、104周的治疗期以及1年的开放标签延长期(extension period of open label, OLE),预计初步完成日期在2024年底。
2.3 基因治疗药物
相比于生物大分子药物和化学小分子药物,基因治疗药物的优势在于可以通过单次注射将目标基因送入病变部位,减少重复治疗次数,达到长时间甚至永久实现目标基因的眼内表达。随着全基因组关联研究的深入发现,基因治疗药物的种类将会越来越多。
2.3.1 携带补体因子I基因的载体药物 GT005是由Gyroscope公司开发的一种基于腺相关病毒(adeno-associated virus, AAV)递送药物的基因疗法,通过单次视网膜下注射药物,促进人体CFI的表达,从而减缓GA的进展[58-60]。一项多中心非随机的Ⅰ/Ⅱ期试验(FOCUS)正在进行中,以评估治疗GA的安全性和剂量反应。该试验共招募56名受试者,其中31例经玻璃体视网膜下注射(transvitreous subretinal injection, TVSI)递送GT005,25例使用眼眶视网膜下递送系统(orbital subretinal delivery system, Orbit SDS)递送GT005,研究主要终点是GT005在48周内的安全性。中期数据显示,TVSI队列玻璃体内CFI浓度显著增加,C3及其裂解产物显著减少。TVSI组及Orbit SDS组均显示出良好安全性和耐受性。目前,正在进行两项多中心随机对照Ⅱ期临床试验(HORIZON和EXPLORE),用以评估GT005单次注射治疗GA的安全性和有效性,预计招募的患者分别为250名和75名。
2.3.2 针对MAC的药物 AAVCAGsCD59(又称HMR59)是由Hemera公司开发的一种经IVT注射的AAV载体,可诱导可溶性CD59(sCD59)的形成,从而阻止C9结合形成MAC。一项非随机Ⅰ期临床试验(HMR1001)评估了HMR59对17名GA患者的治疗效果。结果显示,与对照组相比,最高剂量HMR59组的生长减少了23%。在安全性方面,17名患者中有3名(18%)患有轻度玻璃体炎,局部类固醇治疗有效,未发现湿性AMD的发生。目前该试验正处于延长的随访期,以评估HMR59的长期安全性[61]。另有一项多中心随机Ⅱ期临床试验正在进行中,以评估IVT注射HMR59对治疗GA的有效性和安全性。
2.3.3 针对补体因子H的药物 AdCAGfH是一种以AAV为载体的基因疗法,旨在通过阻止C3b形成C3转化酶来下调补体替代途径,目前该药物仍处于临床前研究,是一种潜在的治疗干性AMD的方法[62]。
3 展 望
随着Pegcetacoplan的获批上市,Zimura®的Ⅲ期临床试验数据的公布,GA的治疗正迎来曙光。目前补体抑制治疗GA的治疗靶点逐渐增多,进行临床试验的药物越来越多,相信补体抑制治疗GA能迎来令人更加兴奋的突破,也期待越来越多的GA治疗药物能早日获批上市。
[1] WONG W L, SU X Y, LI X, et al. Global prevalence of age-related macular degeneration and disease burden projection for 2020 and 2040: a systematic review and meta-analysis[J]. Lancet Glob Health, 2014,2(2): e106-e116.
[2] SONG P G, DU Y H, CHAN K Y, et al. The national and subnational prevalence and burden of age-related macular degeneration in China[J]. J Glob Health, 2017,7(2): 020703.
[3] FLECKENSTEIN M, KEENAN T D L, GUYMER R H, et al. Age-related macular degeneration[J]. Nat Rev Dis Primers, 2021,7: 31.
[4] 陈开传,盛敏杰,李敏,等.OCTA评估抗VEGF治疗老年性黄斑变性患者视网膜血流密度变化[J].同济大学学报(医学版),2021,42(3): 333-342.
[5] Age-Related Eye Disease Study Research Group. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no.8[J]. Arch Ophthalmol, 2001,119(10): 1417-1436.
[6] VAVVAS D G, SMALL K W, AWH C C, et al. CFH and ARMS2 genetic risk determines progression to neovascular age-related macular degeneration after antioxidant and zinc supplementation[J]. Proc Natl Acad Sci U S A, 2018,115(4): E696-E704.
[7] RESEARCH GROUP A R E D S 2. Lutein+Zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2(AREDS2) randomized clinical trial[J]. JAMA, 2013,309(19): 2005-2015.
[8] Age-Related Eye Disease Study Research Group, CHEW E Y, CLEMONS T E, et al. Secondary analyses of the effects of lutein/Zeaxanthin on age-related macular degeneration progression: AREDS2 report No.3[J]. JAMA Ophthalmol, 2014,132(2): 142-149.
[9] CHEW E Y, CLEMONS T E, AGR N E, et al. Long-term effects of vitamins C and E, β-carotene, and zinc on age-related macular degeneration: AREDS report no.35[J]. Ophthalmology, 2013,120(8): 1604-1611.e4.
N E, et al. Long-term effects of vitamins C and E, β-carotene, and zinc on age-related macular degeneration: AREDS report no.35[J]. Ophthalmology, 2013,120(8): 1604-1611.e4.
[10] VAN DE VEN J P, NILSSON S C, TAN P L, et al. A functional variant in the CFI gene confers a high risk of age-related macular degeneration[J]. Nat Genet, 2013,45(7): 813-817.
[11] STANTON C M, YATES J R W, DEN HOLLANDER A I, et al. Complement factor D in age-related macular degeneration[J]. Invest Ophthalmol Vis Sci, 2011,52(12): 8828-8834.
[12] MAUGERI A, BARCHITTA M, AGODI A. The association between complement factor H rs1061170 polymorphism and age-related macular degeneration: a comprehensive meta-analysis stratified by stage of disease and ethnicity[J]. Acta Ophthalmol, 2019,97(1): e8-e21.
[13] KHANDHADIA S, CIPRIANI V, YATES J R W, et al. Age-related macular degeneration and the complement system[J]. Immunobiology, 2012,217(2): 127-146.
[14] FRITSCHE L G, FARISS R N, STAMBOLIAN D, et al. Age-related macular degeneration: genetics and biology coming together[J]. Annu Rev Genomics Hum Genet, 2014,15: 151-171.
[15] ANDERSON D H, RADEKE M J, GALLO N B, et al. The pivotal role of the complement system in aging and age-related macular degeneration: hypothesis re-visited[J]. Prog Retin Eye Res, 2010,29(2): 95-112.
[16] VIGNESH P, RAWAT A, SHARMA M, et al. Complement in autoimmune diseases[J]. Clin Chim Acta, 2017,465: 123-130.
[17] DOB J, KOCSIS A, G
J, KOCSIS A, G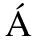 L P. Be on target: strategies of targeting alternative and lectin pathway components in complement-mediated diseases[J]. Front Immunol, 2018,9: 1851.
L P. Be on target: strategies of targeting alternative and lectin pathway components in complement-mediated diseases[J]. Front Immunol, 2018,9: 1851.
[18] DEGN S E, JENSENIUS J C, BJERRE M. The lectin pathway and its implications in coagulation, infections and auto-immunity[J]. Curr Opin Organ Transplant, 2011,16(1): 21-27.
[19] NORIS M, REMUZZI G. Overview of complement activation and regulation[J]. Semin Nephrol, 2013,33(6): 479-492.
[20] DUNKELBERGER J R, SONG W C. Complement and its role in innate and adaptive immune responses[J]. Cell Res, 2010,20(1): 34-50.
[21] SWANSON K V, DENG M, TING J P Y. The NLRP3 inflammasome: molecular activation and regulation to therapeutics[J]. Nat Rev Immunol, 2019,19(8): 477-489.
[22] MERLE N S, CHURCH S E, FREMEAUX-BACCHI V, et al. Complement system part Ⅰ-molecular mechanisms of activation and regulation[J]. Front Immunol, 2015,6: 262.
[23] MERLE N S, NOE R, HALBWACHS-MECARELLI L, et al. Complement system part Ⅱ: role in immunity[J]. Front Immunol, 2015,6: 257.
[24] HEESTERBEEK T J, LECHANTEUR Y T E, LORÉS-MOTTA L, et al. Complement activation levels are related to disease stage in AMD[J]. Invest Ophthalmol Vis Sci, 2020,61(3): 18.
[25] JOHNSON L V, OZAKI S, STAPLES M K, et al. A potential role for immune complex pathogenesis in drusen formation[J]. Exp Eye Res, 2000,70(4): 441-449.
[26] ANDERSON D H, MULLINS R F, HAGEMAN G S, et al. A role for local inflammation in the formation of drusen in the aging eye[J]. Am J Ophthalmol, 2002,134(3): 411-431.
[27] JOHNSON L V, LEITNER W P, STAPLES M K, et al. Complement activation and inflammatory processes in Drusen formation and age related macular degeneration[J]. Exp Eye Res, 2001,73(6): 887-896.
[28] ARMENTO A, UEFFING M, CLARK S J. The complement system in age-related macular degeneration[J]. Cell Mol Life Sci, 2021,78(10): 4487-4505.
[29] FRITSCHE L G, IGL W, BAILEY J N, et al. A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants[J]. Nat Genet, 2016,48(2): 134-143.
[30] SCHMIDT C Q, LAMBRIS J D, RICKLIN D. Protection of host cells by complement regulators[J]. Immunol Rev, 2016,274(1): 152-171.
[31] MCHARG S, CLARK S J, DAY A J, et al. Age-related macular degeneration and the role of the complement system[J]. Mol Immunol, 2015,67(1): 43-50.
[32] PAPP A, PAPP K, UZONYI B, et al. Complement factor H-related proteins FHR1 and FHR5 interact with extracellular matrix ligands, reduce factor H regulatory activity and enhance complement activation[J]. Front Immunol, 2022,13: 845953.
[33] JONG S D, BREUK A D, VOLOKHINA E B, et al. Systemic complement levels in patients with age-related macular degeneration carrying rare or low-frequency variants in the CFH gene[J]. Hum Mol Genet, 2022,31(3): 455-470.
[34] CIPRIANI V, LORÉS-MOTTA L, HE F, et al. Increased circulating levels of factor H-related protein 4 are strongly associated with age-related macular degeneration[J]. Nat Commun, 2020,11(1): 778.
[35] HALLAM T M, MARCHBANK K J, HARRIS C L, et al. Rare genetic variants in complement factor I lead to low FI plasma levels resulting in increased risk of age-related macular degeneration[J]. Invest Ophthalmol Vis Sci, 2020,61(6): 18.
[36] SAKSENS N T, GEERLINGS M J, BAKKER B, et al. Rare genetic variants associated with development of age-related macular degeneration[J]. JAMA Ophthalmol, 2016,134(3): 287-293.
[37] BONILHA V L, BELL B A, HU J, et al. Geographic atrophy: confocal scanning laser ophthalmoscopy, histology, and inflammation in the region of expanding lesions[J]. Invest Ophthalmol Vis Sci, 2020,61(8): 15.
[38] MULFAUL K, MULLIN N K, GIACALONE J C, et al. Local factor H production by human choroidal endothelial cells mitigates complement deposition: implications for macular degeneration[J]. J Pathol, 2022,257(1): 29-38.
[39] GRASSMANN F, HARSCH S, BRANDL C, et al. Assessment of novel genome-wide significant gene loci and lesion growth in geographic atrophy secondary to age-related macular degeneration[J]. JAMA Ophthalmol, 2019,137(8): 867-876.
[40] SCHOLL H P N, FLECKENSTEIN M, FRITSCHE L G, et al. CFH, C3 and ARMS2 are significant risk loci for susceptibility but not for disease progression of geographic atrophy due to AMD[J]. PLoS One, 2009,4(10): e7418.
[41] KLEIN M L, FERRIS F L 3rd, FRANCIS P J, et al. Progression of geographic atrophy and genotype in age-related macular degeneration[J]. Ophthalmology, 2010,117(8): 1554-1559, 1559.e1.
[42] WYKOFF C C, HERSHBERGER V, EICHENBAUM D, et al. Inhibition of complement factor 3 in geographic atrophy with NGM621: phase 1 dose-escalation study results[J]. Am J Ophthalmol, 2022,235: 131-142.
[43] LIAO D S, GROSSI F V, MEHDI D E, et al. Complement C3 inhibitor pegcetacoplan for geographic atrophy secondary to age-related macular degeneration: a randomized phase 2 trial[J]. Ophthalmology, 2020,127(2): 186-195.
[44] WYKOFF C C, ROSENFELD P J, WAHEED N K, et al. Characterizing new-onset exudation in the randomized phase 2 FILLY trial of complement inhibitor pegcetacoplan for geographic atrophy[J]. Ophthalmology, 2021,128(9): 1325-1336.
[45] STEINLE N C, PEARCE I, MONÉS J, et al. Impact of baseline characteristics on geographic atrophy progression in the FILLY trial evaluating the complement C3 inhibitor pegcetacoplan[J]. Am J Ophthalmol, 2021,227: 116-124.
[46] HUGHES S, GUMAS J, LEE R, et al. Prolonged intraocular residence and retinal tissue distribution of a fourth-generation compstatin-based C3 inhibitor in non-human Primates[J]. Clin Immunol, 2020,214: 108391.
[47] JAFFE G J, WESTBY K, CSAKY K G, et al. C5 inhibitor avacincaptad pegol for geographic atrophy due to age-related macular degeneration: a randomized pivotal phase 2/3 trial[J]. Ophthalmology, 2021,128(4): 576-586.
[48] PATEL S S, LALLY D R, HSU J, et al. Avacincaptad pegol for geographic atrophy secondary to age-related macular degeneration: 18-month findings from the GATHER1 trial[J]. Eye, 2023,37(17): 3551-3557.
[49] KHANANI A M, PATEL S S, STAURENGHI G, et al. Efficacy and safety of avacincaptad pegol in patients with geographic atrophy(GATHER2): 12-month results from a randomised, double-masked, phase 3 trial[J]. Lancet, 2023,402(10411): 1449-1458.
[50] YEHOSHUA Z, DE AMORIM GARCIA FILHO C A, NUNES R P, et al. Systemic complement inhibition with eculizumab for geographic atrophy in age-related macular degeneration: the COMPLETE study[J]. Ophthalmology, 2014,121(3): 693-701.
[51] GROVER A, SANKARANARAYANAN S, MATHUR V, et al. Pharmacokinetic and target engagement measures of ANX007, an anti-C1q antibody fragment, following intravitreal administration in nonhuman Primates[J]. Invest Ophthalmol Vis Sci, 2023,64(2): 3.
[52] GROSSMAN T R, CARRER M, SHEN L J, et al. Reduction in ocular complement factor B protein in mice and monkeys by systemic administration of factor B antisense oligonucleotide[J]. Mol Vis, 2017,23: 561-571.
[53] DREISMANN A K, HALLAM T M, TAM L C, et al. Gene targeting as a therapeutic avenue in diseases mediated by the complement alternative pathway[J]. Immunol Rev, 2023,313(1): 402-419.
[54] JAFFE G, SAHNI J, FAUSER S, et al. Development of IONIS-FB-LRx to treat geographic atrophy associated with AMD[J]. Investig Ophthalmol Vis Sci, 2020,61: 4305.
[55] BIGGS R M, MAKOU E, LAUDER S, et al. A novel full-length recombinant human complement factor H(CFH; GEM103) for the treatment of age-related macular degeneration shows similar in vitro functional activity to native CFH[J]. Curr Eye Res, 2022,47(7): 1087-1093.
[56] KHANANI A M, MATURI R K, BAGHERI N, et al. A phase I, single ascending dose study of GEM103(recombinant human complement factor H) in patients with geographic atrophy[J]. Ophthalmol Sci, 2022,2(2): 100154.
[57] WILES J A, GALVAN M D, PODOS S D, et al. Discovery and development of the oral complement factor D inhibitor danicopan(ACH-4471)[J]. Curr Med Chem, 2020,27(25): 4165-4180.
[58] AHMAD A, MANDWIE M, DREISMANN A K, et al. Adeno-associated virus vector gene delivery elevates factor I levels and downregulates the complement alternative pathway in vivo[J]. Hum Gene Ther, 2021,32(21-22): 1370-1381.
[59] DREISMANN A K, MCCLEMENTS M E, BARNARD A R, et al. Functional expression of complement factor I following AAV-mediated gene delivery in the retina of mice and human cells[J]. Gene Ther, 2021,28(5): 265-276.
[60] ANNAMALAI B, PARSONS N, NICHOLSON C, et al. Subretinal rather than intravitreal adeno-associated virus-mediated delivery of a complement alternative pathway inhibitor is effective in a mouse model of RPE damage[J]. Invest Ophthalmol Vis Sci, 2021,62(4): 11.
[61] KHANANI A M, THOMAS M J, AZIZ A A, et al. Review of gene therapies for age-related macular degeneration[J]. Eye, 2022,36(2): 303-311.
[62] CASHMAN S M, GRACIAS J, ADHI M, et al. Adenovirus-mediated delivery of factor H attenuates complement C3 induced pathology in the murine retina: a potential gene therapy for age-related macular degeneration[J]. J Gene Med, 2015,17(10-12): 229-243.