肺部听诊是利用听诊器辨析患者呼吸音与正常呼吸音差异,从而即刻评估患者肺部状态的临床基本体格检查手段,具有易上手、无创、无辐射、快速简便等优点。自1816年La⊇nnec发明听诊器以来,听诊广泛应用于临床尤其是呼吸系统疾病中,成为呼吸科医师诊断和评估疾病的重要检查手段。随着CT、磁共振成像、超声等影像技术快速发展,因其可以提供客观准确的信息,使传统听诊在体格检查、呼吸疾病诊断和评估中的作用逐渐弱化。近年来,传感芯片以及人工智能技术迅速发展,记录存储呼吸音并通过人工智能算法对其进行分析实现了对呼吸音的客观定量分析,并具有快速准确、远程操作等优点,使之重新成为医生的关注点。因此,本文将依次从传统听诊面临的挑战、呼吸音数字化分析概述、呼吸音数字化分析对肺部体格检查的意义及其在呼吸系统疾病中的辅助价值进行综述,旨在帮助呼吸学界提高对呼吸音数字化的认识,进而提高呼吸系统疾病管理水平。
1 传统听诊面临的挑战与解决方案
肺部听诊是利用听诊器辨析患者呼吸音与正常呼吸音差异,从而即刻评估患者肺部状态的临床基本体格检查手段,具有易上手、无创、无辐射、快速简便等优点[1]。然而,传统听诊方式也面临着诸多挑战。第一,听诊具有较强的主观性,临床经验存在差异的不同年资医生对呼吸音的判断有所差别[2]。第二,人耳的听觉范围具有局限性,正常呼吸音的强度常覆盖异常呼吸音,人耳难以做到有效辨别,且异常呼吸音频率较低,易被胸壁过滤而容易被人耳忽略[3]。第三,传统听诊无法进行回顾性分析,不适用于远程评估,限制了其在非医院场景或医生穿着防护服等情况下的使用。第四,传统听诊的结果为“是否听到干湿啰音等异常呼吸音”等定性描述,过于笼统,无法通过标准化的声音频率、幅度等定量指标来描述和分析呼吸音[1]。此外,由于CT、核磁、超声的快速发展,其客观结果的呈现致使部分临床医生在诊断和治疗过程中使用听诊的意愿下降,忽视了传统体格检查的重要性,转而依赖这类辅助检查。
随着科学技术的不断发展,依托于人工智能的呼吸音数字化分析可能成为解决这一难题的有力工具。呼吸音数字化分析依托电子听诊器,实现了呼吸音的记录和储存,具有敏感性高、分辨率高、可分析、可回放的特点。相比于传统的听诊方式,呼吸音数字化分析能精确地记录呼吸音,实现对呼吸音的定量分析,使输出结果更加客观。其次,医联体远程会诊无法现场查看患者,依托于数字化呼吸音分析的远程听诊有广泛的用武之地,尤其在新型冠状病毒感染(coronavirus disease 2019, COVID-19)等气溶胶疾病流行期间,这一方法无疑具有潜在的应用价值[4-5]。
2 呼吸音数字化概述
2.1 呼吸音概述及声学特征
呼吸音是指通过口鼻吸入的空气在通过呼吸道和肺泡时由于振动或撞击气道壁所产生相应的声音,后者通过肺组织和胸壁传递到体表,有效地反映气道和肺部的状况。
呼吸音可分为正常呼吸音和异常呼吸音。正常呼吸音包括肺泡呼吸音、支气管呼吸音、支气管肺泡呼吸音,其声学特征与呼吸音产生的位置、传播方式等相关。支气管呼吸音常闻及于喉部、胸骨上窝和背部颈椎(C6![]() C7),支气管呼吸音可不透过胸壁传播直接被闻及,频率分布于100
C7),支气管呼吸音可不透过胸壁传播直接被闻及,频率分布于100![]() 5 000 Hz。当支气管呼吸音出现减弱或增强时,常提示上呼吸道的梗阻或狭窄,此时支气管的呼吸音变为喘鸣音(stridor)。肺泡呼吸音可闻及于大部分肺野,频率约为100
5 000 Hz。当支气管呼吸音出现减弱或增强时,常提示上呼吸道的梗阻或狭窄,此时支气管的呼吸音变为喘鸣音(stridor)。肺泡呼吸音可闻及于大部分肺野,频率约为100![]() 1 000 Hz,由于胸壁对声波的滤过作用,声音频率在200 Hz左右其强度便出现明显下降,肺泡呼吸音的减弱常提示呼吸音产生或传播出现异常,前者包括中枢性呼吸衰竭、肺气肿等,后者囊括肥胖、胸廓畸形等[1]。
1 000 Hz,由于胸壁对声波的滤过作用,声音频率在200 Hz左右其强度便出现明显下降,肺泡呼吸音的减弱常提示呼吸音产生或传播出现异常,前者包括中枢性呼吸衰竭、肺气肿等,后者囊括肥胖、胸廓畸形等[1]。
异常呼吸音可根据持续时间进一步分为连续性异常呼吸音和非连续性异常呼吸音: 连续性异常呼吸音包括“喘鸣音(stridor)”、“哮鸣音(wheeze)”、“干啰音(rhonchus)”、“鸣鸟音(squawk)”等。在第九版诊断学中,“wheeze”和“rhonchus”被统称为干啰音[6]。而“wheeze”是一种音调高的干啰音,频率常大于1 000 Hz,产生机制多为各种原因造成的气道狭窄,中文中更常被翻译为“哮鸣音”。“rhonchus”是一种音调低的干啰音,频率仅有150 Hz,产生机制多为气道分泌物所引起的气管或支气管狭窄,性质类似于鼾声[7]。非连续性异常呼吸音包括“粗湿啰音(coarse crackle)”、“细湿啰音(fine crackle)”等。在波形图上粗细湿啰音都呈现为重复一致的声波,但细湿啰音的持续时间短仅有5 ms,频率较高约为650 Hz,而粗湿啰音持续时间较长而频率低,其原因可能与细湿啰音的产生是由于小气道的突然开放,而粗湿啰音则是与由气管内气泡破裂引起有关。细湿啰音中还有一种特殊的类型: “Velcro啰音”。其性质类似于尼龙扣撕开时的声音,常见于间质性肺纤维化患者。此外,还有各种异常呼吸音如“鸣鸟音”等,各类呼吸音特点详见表1。
表1 常见异常呼吸音及其特点
Tab.1 Common abnormal breath sounds and characteristics
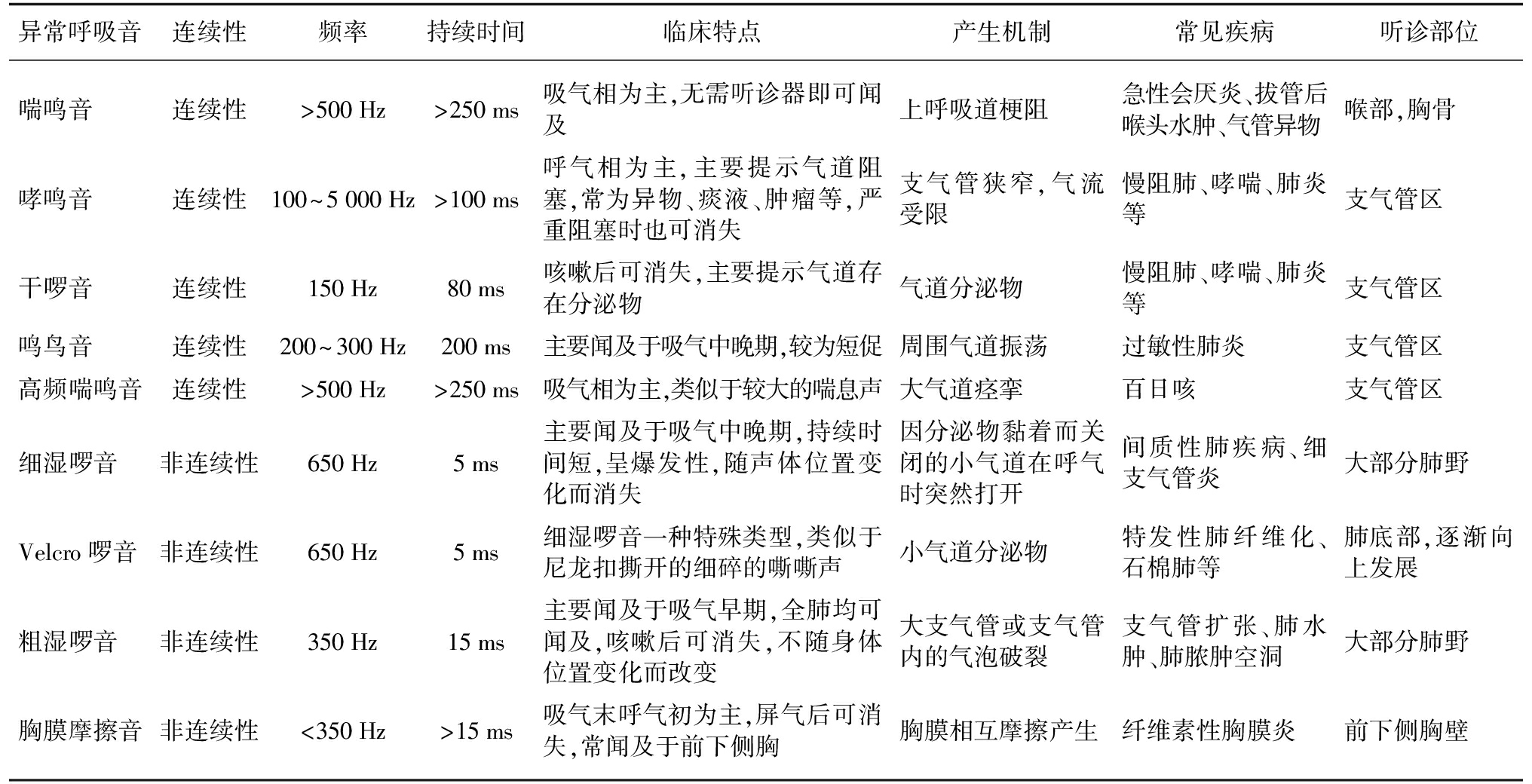
异常呼吸音连续性频率持续时间临床特点产生机制常见疾病听诊部位喘鸣音连续性>500Hz>250ms吸气相为主,无需听诊器即可闻及上呼吸道梗阻急性会厌炎、拔管后喉头水肿、气管异物喉部,胸骨哮鸣音连续性100~5000Hz>100ms呼气相为主,主要提示气道阻塞,常为异物、痰液、肿瘤等,严重阻塞时也可消失支气管狭窄,气流受限慢阻肺、哮喘、肺炎等支气管区干啰音连续性150Hz80ms咳嗽后可消失,主要提示气道存在分泌物气道分泌物慢阻肺、哮喘、肺炎等支气管区鸣鸟音连续性200~300Hz200ms主要闻及于吸气中晚期,较为短促周围气道振荡过敏性肺炎支气管区高频喘鸣音连续性>500Hz>250ms吸气相为主,类似于较大的喘息声大气道痉挛百日咳支气管区细湿啰音非连续性650Hz5ms主要闻及于吸气中晚期,持续时间短,呈爆发性,随声体位置变化而消失因分泌物黏着而关闭的小气道在呼气时突然打开间质性肺疾病、细支气管炎大部分肺野Velcro啰音非连续性650Hz5ms细湿啰音一种特殊类型,类似于尼龙扣撕开的细碎的嘶嘶声小气道分泌物特发性肺纤维化、石棉肺等肺底部,逐渐向上发展粗湿啰音非连续性350Hz15ms主要闻及于吸气早期,全肺均可闻及,咳嗽后可消失,不随身体位置变化而改变大支气管或支气管内的气泡破裂支气管扩张、肺水肿、肺脓肿空洞大部分肺野胸膜摩擦音非连续性<350Hz>15ms吸气末呼气初为主,屏气后可消失,常闻及于前下侧胸胸膜相互摩擦产生纤维素性胸膜炎前下侧胸壁
目前国际上对各种异常呼吸音的分类和命名仍存在分歧,不同地区异常呼吸音的名称、描述以及定义也不尽相同,未来应针对我国呼吸音门类实施更加准确的定义及分类。
2.2 呼吸音数字化分析流程
呼吸音数字化分析流程主要包含呼吸音的采集、肺音库的构建、呼吸音的预处理、特征选择提取和算法模型分类多个步骤,详细流程可见图1。
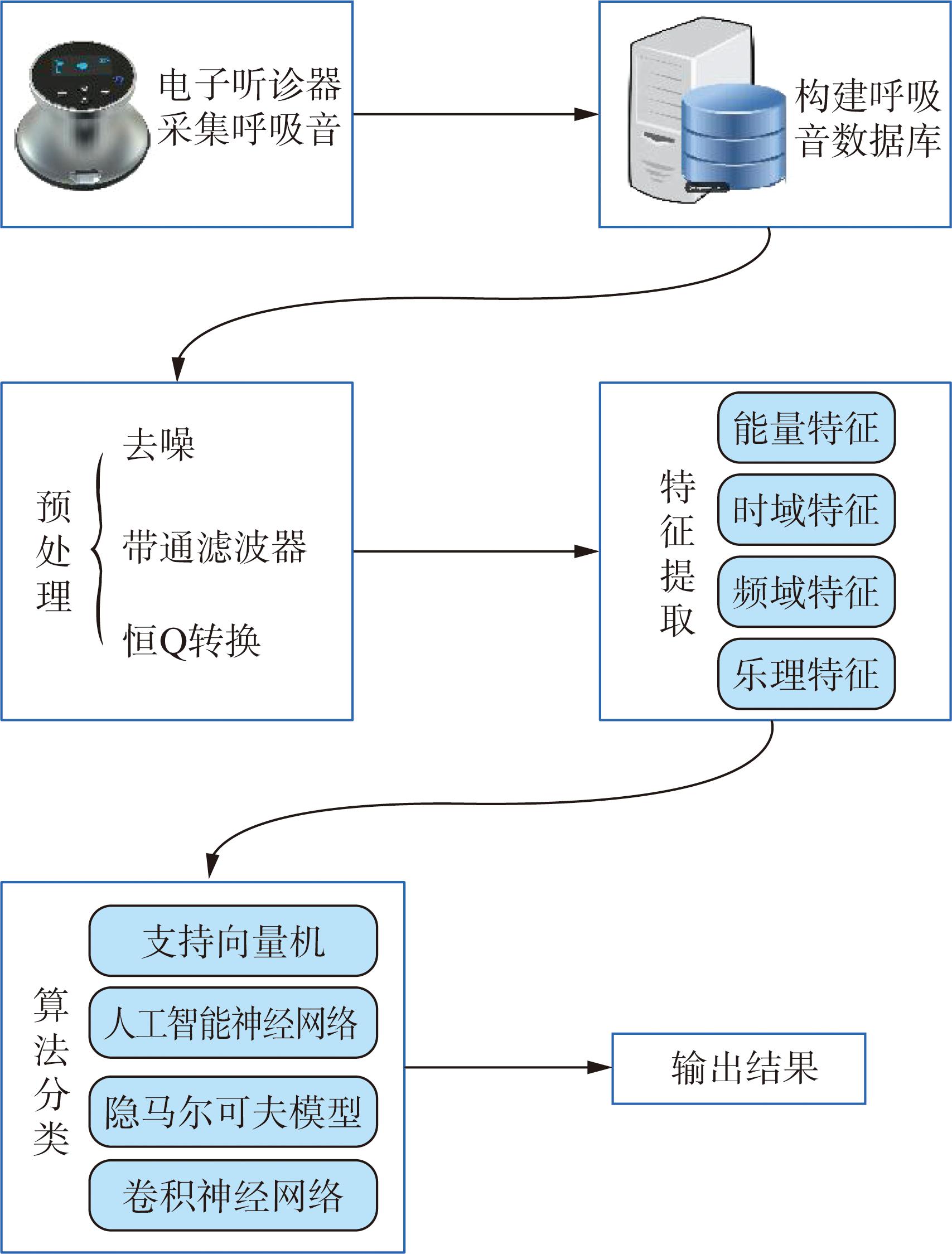
图1 数字化呼吸音分析流程图
Fig.1 Flow chart of computerized respiratory sound analysis
2.2.1 呼吸音的采集 电子听诊器使用各种传感器包括电容式麦克风以及电压传感器对声音信号进行转换处理,完成呼吸音的储存与传输,并且通过外界设备实时显示呼吸音的波形,进一步完成呼吸音分析[8]。相比传统听诊器,电子听诊器能够放大声音信号,去除噪声等伪影,并且能够储存回放呼吸音。目前常见的商业化电子听诊器有Littmann3200、LD-DS-20、Wholter、VRI和LSA-2000等,可完成家庭日常监控、识别异常呼吸音并判断严重程度等功能。
为实现呼吸音采集标准化,2000年CRSA计算机化呼吸音指南[9](computerized respiratory sound analysis, CRSA)提出了电子呼吸音的采集标准,即在周围环境安静的状态下,受试者取坐位双手放置于大腿上,张口进行潮式呼吸,吸气呼气的峰值流速达到1![]() 1.5 L/s或预计最大峰值流速的10%
1.5 L/s或预计最大峰值流速的10%![]() 15%。同时在收集异常呼吸音时,推荐受试者进行张口呼吸以及深呼吸以增强异常呼吸音,过程中注意使用鼻夹避免干扰。
15%。同时在收集异常呼吸音时,推荐受试者进行张口呼吸以及深呼吸以增强异常呼吸音,过程中注意使用鼻夹避免干扰。
2.2.2 肺音库的构建 高质量的肺音数据库是构建人工智能或电子呼吸音自动分析模型的基础。基于构建呼吸音算法以及比较不同呼吸音算法模型的需要,2017年国际生物医学和健康信息学会议(International Conference on Biomedical and Health Informatics, ICBHI)建立了目前最大的呼吸音数据库,其中包含126名受试者的呼吸音,6 898个呼吸循环,1 898条干啰音和8 877条湿啰音数据。同时呼吸音中还包含一定数量的干扰杂音以帮助算法模型提高性能。目前已有多个区分异常呼吸音的算法在ICBHI数据库上开发并且取得了较高的准确率[10-12]。其他的呼吸音数据库包括Marburg呼吸音数据库、Stethoscope和HF_Lung_V1[13]等。但目前开放获取的呼吸音库都规模较小,存在异常呼吸音种类不齐全等不足,未来应建立更多大型、异质性、全面的呼吸音数据库以解决这类难题。
2.2.3 呼吸音预处理 尽管在采集声音时采取了避免人为噪声的措施,但由于电子干扰、听诊器微小移动和其他未知原因,多数呼吸音数据有必要实施预处理,其中包括通过小波去噪等方法消除部分背景噪声,而后对呼吸音进行预加重补偿,增强呼吸音特点区域的振幅,同时对呼吸音进行分帧和加窗等从而转换为多个短时、平稳的信号等。
2.2.4 特征提取 目前呼吸音特征提取主要有两种方式,一是基于机器学习人工提取的特征,二是依靠深度学习算法通过深度神经网络自动完成。
呼吸音人工提取的特征通常包括音调、持续时间、谐波噪声比(harmonics-to-noise ratio, HNR)和时域抖动等,这些特征被提取后输入相应分类器,被广泛应用于异常呼吸音分类等问题[14]。相比于依靠特征的机器学习模型,深度学习算法并不依赖于人为地对明显的特征实施提取,而是自动化地利用整条呼吸音数据进行学习自动分类。Zulfiqar等[15]提出在呼吸音中加入人工噪声(artificial noise addition, ANA)能够增加异常呼吸音的特征,帮助深度卷积神经网络算法对呼吸音的特征提取,同时添加人工噪声能够防止算法模型出现过拟合等问题。
2.2.5 算法模型分类 呼吸音分析算法也可分为依靠特征提取的机器学习以及通过大量数据自动提取特征的深度学习。
传统机器学习模型则常用于异常呼吸音分类问题,包括支持向量机(support vector machine, SVM)、人工智能神经网络(artificial neural network, ANN)、高斯混合模型、随机森林和隐马尔可夫模型等[16-18]。
深度学习算法主要应用于基于呼吸音进行呼吸系统疾病分类问题,包括卷积神经网络(conventional neural network, CNN)、循环神经网络(recurrent neural network, RNN)等。近年来,随着深度学习的发展,越来越多的混合人工智能模型被应用于呼吸音分析领域。例如Fraiwan等[12]采用CNN和长短期记忆(long short-term memory, LSTM)建立模型,通过分析呼吸音来区分哮喘、肺炎、支气管扩张、慢性阻塞性肺疾病及心力衰竭的患者,该模型总体平均准确率可达99.62%。
3 呼吸音数字化分析对肺部体格检查的意义
听诊是肺部体格检查中最为重要的组成部分,可辅助临床医生对患者病情进行合理的评估。呼吸音数字化则赋予了临床医生在开展肺部体格检查时的更多可能性: 第一,记录并储存患者治疗前后呼吸音变化,以便对比病情变化程度;第二,这类设备记录的数据可以实现线上传输,为远程医疗评估患者的病情提供了新的资料,补齐该过程中缺乏体格检查的这一缺陷;第三,呼吸音数字化为肺部体格检查的定量分析开启了新的可能,通过对某一异常呼吸音具体持续时长、音调的变化客观分析,将其转化为定量数据,有利于精准评估。
3.1 哮鸣音
哮鸣音是呼吸系统疾病中常见的异常呼吸音,常闻及于哮喘患者,部分慢性阻塞性肺疾病、肺炎患者由于气道狭窄或阻塞也会出现哮鸣音。哮鸣音的出现通常预示着呼气峰值流量低于正常时的50%,在临床实践中多预示着患者可能会出现呼吸困难、窒息等危及生命事件。
呼吸音数字化分析对哮鸣音的研究主要集中在哮鸣音的鉴别以及通过哮鸣音预测气道阻塞比例这两方面: 如Taplidou等[19]收集了10例慢性阻塞性肺疾病以及11例哮喘患者的呼吸音,通过连续小波转换提取23个特征。该研究团队发现其中22种特征在区分慢性阻塞性肺疾病及哮喘患者吸气呼气相哮鸣音时差异都具有统计学意义,明确其可作为不同疾病相关哮喘的有效鉴别依据。而Oud[20]团队使用第一秒用力呼气量(forced expiratory volume in one second, FEV1)代表呼吸道阻塞程度,寻找哮鸣音随着气道阻塞的程度逐渐变化的可能性。研究团队使用Welch法计算哮鸣音的功率图谱,通过K邻近算法并根据FEV1对不同阻塞程度的哮鸣音进行分类,该模型准确率为60%![]() 90%,通过哮鸣音评估呼吸道阻塞程度存在一定的可能性。不仅如此,数字化分析哮鸣音在诊断儿童哮喘也有用武之地,Sakama[21]团队收集114例儿童哮喘患者的呼吸音以及肺功能数据,通过哮鸣音以及肺功能降低(FEV1/预计值<80%)对哮喘儿童进行分类,该研究团队发现出现哮鸣音或肺功能降低的哮喘患者的吸气/呼气声功率比(expiration-to-inspiration lung sound power ratio, E/I)显著高于无哮鸣音且肺功能正常的儿童哮喘患者,提示哮鸣音和肺功能一样能够作为一种评估哮喘患者气道阻塞的指标。
90%,通过哮鸣音评估呼吸道阻塞程度存在一定的可能性。不仅如此,数字化分析哮鸣音在诊断儿童哮喘也有用武之地,Sakama[21]团队收集114例儿童哮喘患者的呼吸音以及肺功能数据,通过哮鸣音以及肺功能降低(FEV1/预计值<80%)对哮喘儿童进行分类,该研究团队发现出现哮鸣音或肺功能降低的哮喘患者的吸气/呼气声功率比(expiration-to-inspiration lung sound power ratio, E/I)显著高于无哮鸣音且肺功能正常的儿童哮喘患者,提示哮鸣音和肺功能一样能够作为一种评估哮喘患者气道阻塞的指标。
目前也有团队基于以上基础,开发了服务于长期呼吸音监测的可穿戴式设备,如Yilmaz等[15]采用压电式传感器设计了一款穿戴式听诊器,相较目前常见的Littmann 3200电子听诊器,该设备在性能上具有一定差距,其去除低频噪声、高保真记录异常呼吸音方面仍有一定进步空间,但作为一种穿戴设备,其在未来具有广泛的应用前景,可用于非医疗场景下及时发现哮喘发作患者。
3.2 湿啰音
湿啰音是一种短暂,不连续的异常呼吸音,根据湿啰音音调、持续时间又可进一步分为粗湿啰音和细湿啰音。湿啰音的产生多由于气体通过呼吸道内的分泌物或痰液,或是因痰液在小气道内移动或排出,引起气流阻塞和重新开放所致。常见于慢性阻塞性肺疾病、支气管扩张、肺炎、心力衰竭等容易引起肺部感染的疾病,对湿啰音的识别和分析对诊断评估这类呼吸系统疾病具有重要临床意义[1]。
不同呼吸系统疾病所产生的湿啰音时间、类型各不相同,Melbye等[22]对慢性阻塞性肺疾病患者的湿啰音特征进行了探索,该研究团队收集了特罗姆瑟地区4 000多例居民的呼吸音数据,通过分析吸气相和呼气相湿啰音出现频次,该团队发现吸气相的早期湿啰音比粗湿啰音更加具有预测诊断慢阻肺价值。但该研究收集的慢阻肺患者呼吸音数据较少,同时采用人耳分辨湿啰音,受人为因素影响较大。
Velcro啰音是细湿啰音的一种特殊类型,因其独特的声音性质而被命名。Velcro啰音常闻及特发性肺纤维化患者,早期位于肺底部,并随着疾病的进展逐渐向上蔓延。相比于慢阻肺或肺炎患者的细湿啰音,Velcro啰音持续存在于整个吸气相,在特发性肺纤维化患者中,Velcro啰音的出现甚至早于影像学表现。Pancaldi等[23]使用Littmann 3200收集并使用快速傅立叶转换等算法分析了70例风湿性关节炎患者的呼吸音,通过高分辨率CT确诊其中27例风湿性关节炎已经并发间质性肺疾病,研究者发现电子听诊器区分这类间质性肺疾病的患者准确率达到90%,而内科医生的准确率只有60%![]() 70%。
70%。
目前对于异常呼吸音的数字化分析研究较多的对象仍是哮鸣音、湿啰音、Velcro啰音等。而其余一些较少见的异常呼吸音如喘鸣音、鸣鸟音的数字化分析研究较少,这类异常呼吸音如喘鸣音在气道狭窄时也具有重要的临床意义,数字化呼吸音分析在这些少见的异常呼吸音中仍有广阔的研究前景。
4 呼吸音数字化分析在呼吸系统疾病中的价值
在明确呼吸音数字化分析可用于辅助肺部体格检查及其本身的一些优势后,当前已有多个研究团队将呼吸音数字化分析应用特定的某一种呼吸系统疾病中,以提高对疾病的诊疗水平。
4.1 慢性阻塞性肺疾病
慢性阻塞性肺疾病是一种严重危害人类健康的呼吸系统疾病,当前全球呈高发病率和死亡率[24]。呼吸音数字化分析实现了对慢性阻塞性肺疾病常见的湿罗音等呼吸音的定量分析,在该病的筛查、诊断和鉴别中展现出了良好的应用前景。Haider等[16]记录了30例慢性阻塞性肺疾病患者以及25例健康者的呼吸音,采用支持向量机、K邻近算法、Logistic回归对慢阻肺患者和正常人呼吸音进行分类,研究者发现当支持向量机结合肺音中位频率和线性预测系数时,分类模型准确率可达83.6%;进一步结合肺功能数据,准确率可达100%。结果表明呼吸音能够辅助肺功能,提高慢阻肺诊断的准确性。
慢性阻塞性肺疾病急性加重指慢性阻塞性肺疾病稳定期患者病情突然加重,导致患者需要改变用药方案并增加额外的医疗措施。慢性阻塞性肺疾病急性加重的发生明显增加了患者的住院率和死亡率,预防和早期诊断慢阻肺急性加重至关重要。Oliveira等[25]收集了25例未在院期间慢性阻塞性肺疾病急性加重患者以及34例健康志愿者的呼吸音,并分别采集了慢性阻塞性肺疾病急性加重患者住院期间、出院15 d和45 d的呼吸音。作者发现哮鸣音在出院15 d后数量出现明显下降,而吸气相的湿啰音在患者出院15 d后仍会存在。Granero等[26]将电子听诊器和呼吸音数字化分析技术相结合,通过穿戴式听诊设备检测16例慢阻肺稳定期患者呼吸音长达6个月,并采用主要成分分析和支持向量机分类器来识别患者的异常呼吸音如湿啰音等,并证实该方法可预测出75.8%患者的慢性阻塞性肺疾病急性加重事件,平均提前(5±1.9) d。
此外,在鉴别哮喘和慢性阻塞性肺疾病方面,数字化分析呼吸音也有很高的价值。Sen等[27]收集30例哮喘患者的呼吸音和20例慢性阻塞性肺疾病患者的呼吸音并将呼吸音分为吸气早中晚、呼气早中晚6个阶段分别进行分析,通过高斯混合模型结合支持向量机,研究者发现分类器对哮喘和慢性阻塞性肺疾病的分类准确率高达100%和95%,并且吸气相中期的呼吸音在区分哮喘和慢性阻塞性肺疾病中起主要作用。
4.2 哮喘
哮喘是一种反复发作的可逆性气流受限为特征的疾病,这种气道炎症与气道高反应性有关,且罹患人数呈不断上升趋势。实施哮喘的早期诊断及干预临床意义重大,人工智能分析呼吸音能够帮助哮喘的早期诊断,突破哮喘症状早期不典型,且在未发作时无明显症状这一特点。Shimoda等[28]利用快速傅立叶变换提取轻中度哮喘患者肺音的低频吸气呼气声功率比(expiration-to-inspiration lung sound power ratio at low frequencies, E-I LF),开始了对通过肺音预测无症状哮喘患者嗜酸性气道炎症的探索。该团队发现嗜酸性气道炎症哮喘患者的E-I LF明显高于正常哮喘患者和健康人,痰嗜酸性粒细胞的比例、呼出气一氧化氮与E-I LF相关,提示呼吸音数字化分析可作为一种预测哮喘患者嗜酸性气道炎症的一种指标。此外,呼吸音数字化分析还可作为哮喘控制情况的一项指标,Shimoda等[29]分别收集了68例依从性较好的哮喘患者和18位依从性差的患者的呼吸音、肺功能、呼出气一氧化氮和诱导痰等数据样本。通过比较患者的E-I LF和吸入性糖皮质激素(inhaled corticosteroids, ICS)治疗后指标的改变,作者发现哮喘患者的E-I LF明显高于正常人,依从性好的哮喘患者在接受ICS治疗后E-I LF下降明显高于依从性差的患者。
呼吸音数字化分析诊断哮喘主要依靠对哮鸣音的检测识别,但哮鸣音也可在其他呼吸系统疾病以及正常人中被闻及。Islam等[30]在后胸多个部位收集哮喘患者和正常人的呼吸音,并提取呼吸音的功率谱密度特征,采用人工智能神经网络和支持向量机进行分类。作者发现即使在没有哮鸣音的情况下,采用两处呼吸音和三处呼吸音进行分类的准确率分别达到89.2%和93.3%。以上结果表明呼吸音数字化分析有潜力成为哮喘筛查检测的一种新方式。
4.3 肺炎
肺炎是肺部出现炎症性改变的总称,呼吸音数字化分析对肺炎的诊断主要依靠识别肺部炎症时出现的异常呼吸音如湿啰音、哮鸣音和咳嗽等。
肺炎患者的异常呼吸音与慢阻肺急性加重时的呼吸音相类似,将慢阻肺急性加重患者简单地诊断为肺炎会引起严重的后果。Naqvi等[31]提取肺音的时间域特征、倒谱特征和频谱特征相融合来区分这两种异常呼吸音,该算法在ICBHI数据库中区分异常呼吸音准确率达到99.7%。在新型冠状病毒感染流行期间,呼吸音数字化分析从检测湿啰音、哮鸣音等异常呼吸音深入至新型冠状病毒感染合并肺炎的预测中。目前该病的诊断主要依靠核酸检测、抗体检测和抗原检测,但这些检测大多耗时较长且需要收集患者咽拭子等标本。而新型冠状病毒感染引起的呼吸音改变能帮助对其诊断评估,Chen等[17]则对此进行了尝试。在Coswara-Data数据库中分析COVID-19患者呼吸音与正常人呼吸音,作者发现COVID-19患者呼吸音在高频率分段有更高的能量,这种高频能量是由呼吸困难所引起。作者进一步通过深度学习分类器CNN对呼吸音进行COVID-19呼吸音诊断,正确率达到97%。不仅如此,训练后的模型可在智能手机上快速应用计算,呼吸音数字化分析在协助COVID-19诊断方面已经初有成果,目前已有10多种COVID-19呼吸音数据库已经建立来促进呼吸音数字化分析在诊断COVID-19方面的应用。
此外,呼吸音数字化分析还在间质性肺疾病、支气管扩张、气道狭窄等呼吸系统疾病诊断、监测中有所探索。Sgalla等[32]收集了19例间质性肺纤维化患者的呼吸音以及高分辨率胸部CT进行分析,作者发现采集的肺音特征与高分辨率CT(high resolution CT, HRCT)中的网状和蜂窝状结构高度相关,提示呼吸音数字化分析肺音特征可作为间质性肺纤维化严重程度的一种衡量标准,而其在其他呼吸系统疾病中的应用场景,值得进一步拓宽和探寻。
5 展 望
伴随着人工智能技术的高速发展,越来越多的深度学习算法被应用于呼吸音数字化分析,但目前仍然存在一些问题: 首先,呼吸音的采集缺乏标准的采集方法和流程,尽管CRSA指南提出了标准化的呼吸音即在1![]() 1.5 L/s的呼吸流速下所采集的呼吸音,但目前的各项研究中呼吸音的采集工具和方式各不相同,因此在未来需要制定更加详细规范的呼吸音采集标准以帮助提高数字呼吸音的质量。
1.5 L/s的呼吸流速下所采集的呼吸音,但目前的各项研究中呼吸音的采集工具和方式各不相同,因此在未来需要制定更加详细规范的呼吸音采集标准以帮助提高数字呼吸音的质量。
其次,目前大部分呼吸音相关的人工智能算法在开发时都遇到了缺乏呼吸音数据的问题。由于各类型呼吸音数据库中呼吸音采集方式、记录部位、记录时间和呼吸音种类各不相同,导致部分算法无法在各个数据库中进行测试,同时目前公开的呼吸音数据库数量仍然稀少,研究者应着手建立更多的大型公开的呼吸音数据库,在提高人工智能本身算力的同时,尽可能提供训练样本助力模型性能的提高。此外,在呼吸音数字化分析方面,也期待有更多创新独特的呼吸音特征被发现,以更好地帮助提高人工智能模型的性能。
最后,当前该领域多数研究都集中于异常呼吸音的自动分类问题,而针对异常呼吸音相关的肺部疾病的研究较少,还有更多的其他呼吸系统疾病领域有待被挖掘,明确肺部疾病与数字呼吸音之间的联系。
在人工智能技术迅猛发展的背景下,呼吸音数字化分析得到了进一步的发展,相比于传统听诊方式,呼吸音数字化分析客观、准确、远程操作的特点使之逐渐成为临床医生的关注点。但呼吸音数字化分析目前仍处于研究的初级阶段,更多性能优良的呼吸音算法也有待被开发。本文主要综述了传统听诊面临的挑战、呼吸音数字化分析对肺部体格检查的意义以及在呼吸系统疾病诊断中的应用,希望能帮助呼吸音学界更好地理解使用呼吸音数字化分析这项技术,进而提高呼吸系统疾病的整体管理水平。
[1] BOHADANA A, IZBICKI G, KRAMAN S S. Fundamentals of lung auscultation[J]. N Engl J Med, 2014,370(21): 2053.
[2] BERRY M P, MART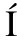 J D, NTOUMENOPOULOS G. Inter-rater agreement of auscultation, palpable fremitus, and ventilator waveform sawtooth patterns between clinicians[J]. Respir Care, 2016,61(10): 1374-1383.
J D, NTOUMENOPOULOS G. Inter-rater agreement of auscultation, palpable fremitus, and ventilator waveform sawtooth patterns between clinicians[J]. Respir Care, 2016,61(10): 1374-1383.
[3] PRAMONO R X A, BOWYER S, RODRIGUEZ-VILLEGAS E. Automatic adventitious respiratory sound analysis: a systematic review[J]. PLoS One, 2017,12(5): e0177926.
[4] NODA A, SARAYA T, MORITA K, et al. Evidence of the sequential changes of lung sounds in COVID-19 pneumonia using a novel wireless stethoscope with the telemedicine system[J]. Intern Med, 2020,59(24): 3213-3216.
[5] WANG B, LIU Y B, WANG Y, et al. Characteristics of pulmonary auscultation in patients with 2019 novel coronavirus in China[J]. Respiration, 2020,99(9): 755-763.
[6] 万学红,卢雪峰.诊断学[M].9版.北京: 人民卫生出版社,2018.
[7] PASTERKAMP H, BRAND P L, EVERARD M, et al. Towards the standardisation of lung sound nomenclature[J]. Eur Respir J, 2016,47(3): 724-732.
[8] NOWAK L J, NOWAK K M. Sound differences between electronic and acoustic stethoscopes[J]. Biomed Eng Online, 2018,17(1): 104.
[9] SOVIJRVI A R A, VANDERSCHOOT J, EARIS J E. Standardization of computerized respiratory sound analysis[J]. European Respiratory Review, 2000,10(77).
[10] ACHARYA J, BASU A. Deep neural network for respiratory sound classification in wearable devices enabled by patient specific model tuning[J]. IEEE Trans Biomed Circuits Syst, 2020,14(3): 535-544.
[11] DEMIR F, SENGUR A, BAJAJ V. Convolutional neural networks based efficient approach for classification of lung diseases[J]. Health Inf Sci Syst, 2020,8(1): 4.
[12] FRAIWAN M, FRAIWAN L, ALKHODARI M, et al. Recognition of pulmonary diseases from lung sounds using convolutional neural networks and long short-term memory[J]. J Ambient Intell Humaniz Comput, 2022,13(10): 4759-4771.
[13] HSU F S, HUANG S R, HUANG C W, et al. Benchmarking of eight recurrent neural network variants for breath phase and adventitious sound detection on a self-developed open-access lung sound database-HF_Lung_V1[J]. PLoS One, 2021,16(7): e0254134.
[14] SHI L K, ZHANG Y X, ZHANG J Y. Lung sound recognition method based on wavelet feature enhancement and time-frequency synchronous modeling[J]. IEEE J Biomed Health Inform, 2023,27(1): 308-318.
[15] ZULFIQAR R, MAJEED F, IRFAN R, et al. Abnormal respiratory sounds classification using deep CNN through artificial noise addition[J]. Front Med, 2021,8: 714811.
[16] HAIDER N S, SINGH B K, PERIYASAMY R, et al. Respiratory sound based classification of chronic obstructive pulmonary disease: a risk stratification approach in machine learning paradigm[J]. J Med Syst, 2019,43(8): 255.
[17] CHEN Z A, LI M Y, WANG R Y, et al. Diagnosis of COVID-19 via acoustic analysis and artificial intelligence by monitoring breath sounds on smartphones[J]. J Biomed Inform, 2022,130: 104078.
[18] SPERANZA C G, MORAES R. Instantaneous frequency based index to characterize respiratory crackles[J]. Comput Biol Med, 2018,102: 21-29.
[19] TAPLIDOU S A, HADJILEONTIADIS L J. Analysis of wheezes using wavelet higher order spectral features[J]. IEEE Trans Biomed Eng, 2010,57(7): 1596-1610.
[20] OUD M, DOOIJES E H, VAN DER ZEE J S. Asthmatic airways obstruction assessment based on detailed analysis of respiratory sound spectra[J]. IEEE Trans Biomed Eng, 2000,47(11): 1450-1455.
[21] SAKAMA T, ICHINOSE M, OBARA T, et al. Effect of wheeze and lung function on lung sound parameters in children with asthma[J]. Allergol Int, 2023,72(4): 545-550.
[22] MELBYE H, AVILES SOLIS J C, J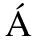 COME C, et al. Inspiratory crackles-early and late-revisited: identifying COPD by crackle characteristics[J]. BMJ Open Respir Res, 2021,8(1): e000852.
COME C, et al. Inspiratory crackles-early and late-revisited: identifying COPD by crackle characteristics[J]. BMJ Open Respir Res, 2021,8(1): e000852.
[23] PANCALDI F, SEBASTIANI M, CASSONE G, et al. Analysis of pulmonary sounds for the diagnosis of interstitial lung diseases secondary to rheumatoid arthritis[J]. Comput Biol Med, 2018,96: 91-97.
[24] CHRISTENSON S A, SMITH B M, BAFADHEL M, et al. Chronic obstructive pulmonary disease[J]. Lancet, 2022,399(10342): 2227-2242.
[25] OLIVEIRA A, RODRIGUES J, MARQUES A. Enhancing our understanding of computerised adventitious respiratory sounds in different COPD phases and healthy people[J]. Respir Med, 2018,138: 57-63.
[26] FERNANDEZ-GRANERO M A, SANCHEZ-MORILLO D, LEON-JIMENEZ A. Computerised analysis of telemonitored respiratory sounds for predicting acute exacerbations of COPD[J]. Sensors, 2015,15(10): 26978-26996.
[27] SEN I, SARACLAR M, KAHYA Y P. Differential diagnosis of asthma and COPD based on multivariate pulmonary sounds analysis[J]. IEEE Trans Biomed Eng, 2021,68(5): 1601-1610.
[28] SHIMODA T, NAGASAKA Y, OBASE Y, et al. Prediction of airway inflammation in patients with asymptomatic asthma by using lung sound analysis[J]. J Allergy Clin Immunol Pract, 2014,2(6): 727-732.
[29] SHIMODA T, OBASE Y, NAGASAKA Y, et al. Lung sound analysis can be an index of the control of bronchial asthma[J]. Allergol Int, 2017,66(1): 64-69.
[30] ISLAM M A, BANDYOPADHYAYA I, BHATTACHARYYA P, et al. Multichannel lung sound analysis for asthma detection[J]. Comput Methods Programs Biomed, 2018,159: 111-123.
[31] NAQVI S Z H, CHOUDHRY M A. An automated system for classification of chronic obstructive pulmonary disease and pneumonia patients using lung sound analysis[J]. Sensors, 2020,20(22): 6512.
[32] SGALLA G, LARICI A R, SVERZELLATI N, et al. Quantitative analysis of lung sounds for monitoring idiopathic pulmonary fibrosis: a prospective pilot study[J]. Eur Respir J, 2019,53(3): 1802093.