经内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography, ERCP)是一种利用消化内镜实施的微创介入诊疗技术,常用于消化内科和肝胆外科,主要方法是由操作医师将造影导管插入十二指肠乳头开口部并注入造影剂后显示胆胰管。我国的ERCP技术起步于20世纪70年代初,目前已成为胆胰疾病诊断和治疗的重要手段[1]。过去由于内镜操作常常为患者带来焦虑和疼痛,在美国及许多其他国家,内镜医师已经在治疗性内镜手术中常规使用清醒镇静[2],而在这个过程中,约有33%![]() 50%患者表示在清醒镇静下仍有疼痛和不适[3],并且清醒镇静下的操作失败率较高,主要是由于患者在镇静剂不足的情况下无法耐受手术而过早终止手术[4],因此为ERCP治疗的患者提供深度镇静对患者体验及治疗效果都是有益的。目前门诊短小手术中应用最广泛的静脉麻醉药为丙泊酚,常与小剂量阿片类镇痛药物联用,以达到无痛诊疗的效果,然而丙泊酚使用中常出现明显的注射痛,加深麻醉时出现的呼吸循环抑制等不良反应也不容忽视[5-6]。环泊酚是一类静脉麻醉新药,为(R)-构型异构体小分子化合物,属于短效GABAA受体激动剂,具有效价高、呼吸抑制轻及注射痛发生率低等优点,适用于各类检查术的镇静或麻醉、外科手术的全身麻醉及ICU镇静等[7]。目前环泊酚用于ERCP的麻醉暂无报道,为探究环泊酚用于ERCP镇静麻醉的有效性、安全性及最佳剂量,本研究将实验组的环泊酚剂量分为较小剂量[0.4 mg/kg诱导,1.0 mg/(kg·h)维持]和较大剂量[0.5 mg/kg诱导,1.5 mg/(kg·h)维持],观察和比较联合舒芬太尼时丙泊酚与不同剂量环泊酚的应用效果,记录不良事件发生情况,为临床麻醉提供参考。
50%患者表示在清醒镇静下仍有疼痛和不适[3],并且清醒镇静下的操作失败率较高,主要是由于患者在镇静剂不足的情况下无法耐受手术而过早终止手术[4],因此为ERCP治疗的患者提供深度镇静对患者体验及治疗效果都是有益的。目前门诊短小手术中应用最广泛的静脉麻醉药为丙泊酚,常与小剂量阿片类镇痛药物联用,以达到无痛诊疗的效果,然而丙泊酚使用中常出现明显的注射痛,加深麻醉时出现的呼吸循环抑制等不良反应也不容忽视[5-6]。环泊酚是一类静脉麻醉新药,为(R)-构型异构体小分子化合物,属于短效GABAA受体激动剂,具有效价高、呼吸抑制轻及注射痛发生率低等优点,适用于各类检查术的镇静或麻醉、外科手术的全身麻醉及ICU镇静等[7]。目前环泊酚用于ERCP的麻醉暂无报道,为探究环泊酚用于ERCP镇静麻醉的有效性、安全性及最佳剂量,本研究将实验组的环泊酚剂量分为较小剂量[0.4 mg/kg诱导,1.0 mg/(kg·h)维持]和较大剂量[0.5 mg/kg诱导,1.5 mg/(kg·h)维持],观察和比较联合舒芬太尼时丙泊酚与不同剂量环泊酚的应用效果,记录不良事件发生情况,为临床麻醉提供参考。
1 资料与方法
1.1 一般资料
选择2022年9月—2023年2月于同济大学附属东方医院行ERCP治疗胆总管结石的患者,性别不限,年龄18![]() 65周岁,BMI为18
65周岁,BMI为18![]() 30 kg/m2,美国麻醉医师协会(American Society of Anesthesiologists, ASA)分级Ⅰ
30 kg/m2,美国麻醉医师协会(American Society of Anesthesiologists, ASA)分级Ⅰ![]() Ⅱ级,操作医师预计时长30
Ⅱ级,操作医师预计时长30![]() 60 min。排除标准: 术前存在血流动力学不稳定的患者;术前急性呼吸道感染患者;术前严重肝肾功能不全患者;术前急性上消化道出血的患者;既往有镇静镇痛类药物滥用史的患者;有精神疾病或意识障碍不能配合的患者;经操作医师预计手术时间<30 min或>1 h的患者。采用随机数字表法将患者分成3组。C组: 诱导用舒芬太尼0.1 μg/kg复合丙泊酚2 mg/kg后术中维持丙泊酚6 mg/(kg·h);R1组: 诱导用舒芬太尼0.1 μg/kg复合环泊酚0.4 mg/kg后术中维持环泊酚1 mg/(kg·h);R2组: 诱导用舒芬太尼0.1 μg/kg复合环泊酚0.5 mg/kg后术中维持环泊酚1.5 mg/(kg·h),麻醉诱导时间均为30 s。
60 min。排除标准: 术前存在血流动力学不稳定的患者;术前急性呼吸道感染患者;术前严重肝肾功能不全患者;术前急性上消化道出血的患者;既往有镇静镇痛类药物滥用史的患者;有精神疾病或意识障碍不能配合的患者;经操作医师预计手术时间<30 min或>1 h的患者。采用随机数字表法将患者分成3组。C组: 诱导用舒芬太尼0.1 μg/kg复合丙泊酚2 mg/kg后术中维持丙泊酚6 mg/(kg·h);R1组: 诱导用舒芬太尼0.1 μg/kg复合环泊酚0.4 mg/kg后术中维持环泊酚1 mg/(kg·h);R2组: 诱导用舒芬太尼0.1 μg/kg复合环泊酚0.5 mg/kg后术中维持环泊酚1.5 mg/(kg·h),麻醉诱导时间均为30 s。
1.2 方法
术前准备: 患者或其家属于术前签署诊疗知情同意书以及麻醉同意书;常规术前禁食8 h,禁水4 h;嘱患者进入ERCP诊间前10 min口服盐酸利多卡因胶浆5 mL,患者进入ERCP诊室后使用静脉留置针开放右上肢外周静脉通路,常规监测心率、无创血压、血氧饱和度,患者取左侧俯卧位,给予鼻导管吸氧4 L/min。麻醉诱导: 3组均给予注射用舒芬太尼(宜昌人福药业有限责任公司,国药准字H20054171,规格50 μg)0.1 μg/kg;C组复合丙泊酚乳状注射液(江苏盈科生物制药有限公司,国药准字H20203504,规格200 mg)2 mg/kg缓慢静脉推注后,以6 mg/(kg·h)维持输注至诊疗结束;R1组复合注射用环泊酚(辽宁海思科制药有限公司,规格50 mg)0.4 mg/kg缓慢静脉注射后,以1.0 mg/(kg·h)维持输注至诊疗结束;R2组复合注射用环泊酚(辽宁海思科制药有限公司,规格50 mg)0.5 mg/kg缓慢静脉注射后,以1.5 mg/(kg·h)维持输注至诊疗结束。若患者在内镜操作时出现呛咳、体动,则允许C组患者单次追加0.5 mg/kg丙泊酚,R1、R2组患者单次追加环泊酚0.1 mg/kg,患者未出现呛咳、体动则视为镇静成功。若患者在术中和苏醒期出现SpO2<90%视为发生呼吸抑制,需增加氧气流量并轻托下颌或调整患者体位,必要时停止内镜操作并予以面罩加压辅助呼吸;若出现低血压(平均动脉压降幅超过基础值20%)时予以麻黄碱6 mg静脉推注;若出现心动过缓(心率<50次/min)予以0.5 mg静脉推注。
1.3 观察指标
监测心率、平均动脉压、血氧饱和度,分别记录各组患者进入检查室时(T0)、麻醉诱导后(T1)、十二指肠乳头插管时(T2)、手术结束时(T3)及转入复苏室时(T4)各指标变化。麻醉诱导后记录患者的改良警觉-镇静评分(modified observer’s assessment of alertness/sedation scale, MOAA/S),诱导完成后30 s再次记录患者MOAA/S评分,记录麻醉记录患者低氧血症、低血压、心动过缓、术后恶心、体动、呃逆、呛咳及停药后苏醒时间。
1.4 统计学处理
应用SPSS 27.0软件分析数据,对所有患者数据进行正态性及方差齐性检验,符合正态分布的计量资料以均值±标准差![]() 表示,组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。非正态分布的计量资料使用Kruskal-Wallis H检验进行组间比较,计数资料以n(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
表示,组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。非正态分布的计量资料使用Kruskal-Wallis H检验进行组间比较,计数资料以n(%)表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
2.1 3组患者基线资料比较
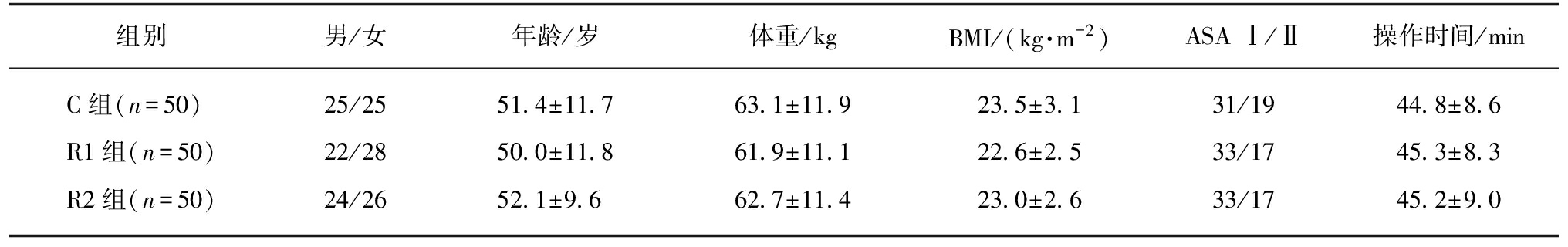
本研究共纳入患者150例,3组患者性别、年龄、体重、BMI、ASA分级、操作时间差异均无统计学意义,见表1。
表1 患者一般情况
Tab.1 Comparison of general conditions in three groups![]()
组别男/女年龄/岁体重/kgBMI/(kg·m-2)ASA Ⅰ/Ⅱ操作时间/minC组(n=50)25/2551.4±11.763.1±11.923.5±3.131/1944.8±8.6R1组(n=50)22/2850.0±11.861.9±11.122.6±2.533/1745.3±8.3R2组(n=50)24/2652.1±9.662.7±11.423.0±2.633/1745.2±9.0
2.2 3组患者镇静成功率比较
3组患者麻醉诱导后即刻MOAA/S评分、诱导完成30 s后MOAA/S评分、呛咳发生率、苏醒时间差异均无统计学意义;与C组比较,R1组、R2组体动发生率、镇静成功率差异无统计学意义;与R1组比较,R2组的体动发生率更低(P<0.05),镇静成功率更高(P<0.05),见表2。
表2 3组患者镇静效果及苏醒时间比较
Tab.2 Comparison of sedation effect and recovery time in three groups![]()

组别诱导后即刻MOAA/S评分诱导后30sMOAA/S评分呛咳体动镇静成功苏醒时间/minC组0.87±0.120.32±0.712(4%)5(10%)43(86%)8.26±2.08R1组0.92±0.130.36±0.804(8%)11(22%)38(76%)8.16±2.34R2组0.85±0.120.26±0.661(2%)2(4%)b48(96%)b9.04±2.38
与C组比较,aP<0.05;与R1组比较,bP<0.05
2.3 3组患者不良事件发生率比较
3组患者心动过缓、呃逆、术后恶心发生率的差异无统计学意义;与C组比较,R1组低血压发生率更低(P<0.05),R1组、R2组呼吸抑制发生例数更少(P<0.05),R1组、R2组注射痛更少(P<0.05),见表3。
表3 3组患者不良事件发生率比较
Tab.3 Comparison of adverse event rates among three groups [n(%)]

组别心动过缓呼吸抑制低血压注射痛恶心呃逆C组2(4%)8(16%)14(28%)5(10%)9(18%)1(2%)R1组2(4%)1(2%)a5(10%)a0(0%)a10(20%)1(2%)R2组3(6%)2(4%)a7(14%)0(0%)a6(12%)2(4%)
与C组比较,aP<0.05;与R1组比较,bP<0.05
2.4 3组患者血流动力学变化比较
3组患者各时间段心率变化无统计学意义;3组患者进入检查室时、转入苏醒室时平均动脉压差异无统计学意义;与C组相比,在麻醉诱导后R1组、R2组平均动脉压更高(P<0.05),十二指肠乳头插管后R1组平均动脉压更高(P<0.05),手术结束时R1组平均动脉压更高(P<0.05);与R1组相比,十二指肠乳头插管后R2组平均动脉压更低(P<0.05),见表4。
表4 血流动力学变化
Tab.4 Comparison of hemodynamic changes among three groups

组别T0T1T2T3T4hr/(次·min-1)mbp/mmHghr/(次·min-1)mbp/mmHghr/(次·min-1)mbp/mmHghr/(次·min-1)mbp/mmHghr/(次·min-1)mbp/mmHgC组75.1±9.292.7±9.267.4±10.078.0±6.476.7±1.491.7±10.968.4±12.287.1±10.670.3±8.692.5±8.7R1组73.6±6.894.5±9.566.2±7.183.0±6.7a74.9±9.596.5±10.2a66.6±9.7194.7±8.6a70.1±7.693.8±6.6R2组76.6±10.897.0±10.868.1±10.384.0±10.8a73.1±11.591.5±12.7b69.2±11.291.1±11.471.4±8.393.5±6.6
hr: 心率;mbp: 平均动脉压;与C组比较,aP<0.05;与R1组比较,bP<0.05
3 讨 论
21世纪以来,为保障消化内镜医疗质量和安全,我国逐步健全消化内镜质量控制体系[8],进一步促进了消化内镜技术的迅速发展。ERCP因治疗效果确切、创伤较小、术后恢复快在国内外应用广泛,逐渐成为临床上肝胆胰疾病诊断和治疗的重要方式[9-10]。在早期的ERCP诊疗中,常进行清醒镇静以减少患者的不适感并实现抗焦虑的效果[11]。虽然ERCP操作的创伤较小,但清醒镇静下的患者仍然会感受到不适和疼痛,甚至因不能耐受疼痛被迫终止手术操作,对于伴有多种疾病的老年患者容易加重原有疾病或诱发潜在的并发症[12]。因此,在ERCP操作时需要保证一定的镇痛、镇静水平来减轻应激反应,除清醒镇静外,还可在保留患者自主呼吸的情况下,联合应用足够的镇静、镇痛药物来实施静脉麻醉[13]。足够的镇静镇痛不仅可以改善患者的就诊体验,还可以增加取石成功率,一项回顾性分析显示,在深度镇静态下行胆总管取石的成功率明显高于单纯镇痛状态下的成功率,且术后胰腺炎发生率较低[14]。
在新版消化内镜检查中的镇静和麻醉指南中将镇静麻醉分为: 基础镇静、中度镇静、深度镇静和气管插管全身麻醉,指南中推荐将丙泊酚作为基础麻醉药物[15]。在《中国消化内镜诊疗镇静/麻醉专家共识》[16]和《中国消化内镜诊疗镇静/麻醉操作技术规范》[17]中明确指出,实施ERCP可在非气管内插管下采用丙泊酚镇静。也有临床研究验证了丙泊酚联合镇痛药物在ERCP中能提供较满意的镇静效果[18-19]。但既往的临床研究及经验均显示了丙泊酚对呼吸及循环系统的抑制作用,且其通过静脉注射产生不同程度的注射痛会给患者造成较差的就诊体验[20]。目前在胃镜和结肠镜中,环泊酚已有广泛应用,ERCP同样属于消化内镜操作但体位特殊且操作刺激较大,因此可考虑应用环泊酚,在满足镇静深度的同时减少不良事件的发生。
在本研究中,为探究环泊酚在ERCP中的应用效果,设置了丙泊酚对照组和两组不同剂量环泊酚实验组,记录到3组患者在诱导后即刻MOAA/S与诱导完成30 s后MOAA/S评分无统计学意义,表明0.4![]() 0.5 mg/kg环泊酚与2 mg/kg丙泊酚在麻醉诱导的镇静效果相当,而与R1组相比R2组患者体动发生率更低且镇静成功率更高,表明在ERCP镇静中R2组镇静方案比R1组镇静方案具有更好的镇静效果。既往也有多项研究也对丙泊酚和环泊酚镇静效果做出评估,Hu等[21]的研究结果显示丙泊酚与环泊酚2组药效动力学参数相似,安全性和耐受性相同,因此环泊酚同样适于作为长时间麻醉维持用药。在一项无痛胃镜和结肠镜检查的临床研究中,随机分配的2组受试者分别接受1.5 mg/kg丙泊酚和0.4 mg/kg环泊酚进行麻醉诱导,结果显示在无痛胃镜检查或无痛结肠镜检查的成功率方面环泊酚镇静效果不劣于丙泊酚[22],Teng等[23]发现使用0.4
0.5 mg/kg环泊酚与2 mg/kg丙泊酚在麻醉诱导的镇静效果相当,而与R1组相比R2组患者体动发生率更低且镇静成功率更高,表明在ERCP镇静中R2组镇静方案比R1组镇静方案具有更好的镇静效果。既往也有多项研究也对丙泊酚和环泊酚镇静效果做出评估,Hu等[21]的研究结果显示丙泊酚与环泊酚2组药效动力学参数相似,安全性和耐受性相同,因此环泊酚同样适于作为长时间麻醉维持用药。在一项无痛胃镜和结肠镜检查的临床研究中,随机分配的2组受试者分别接受1.5 mg/kg丙泊酚和0.4 mg/kg环泊酚进行麻醉诱导,结果显示在无痛胃镜检查或无痛结肠镜检查的成功率方面环泊酚镇静效果不劣于丙泊酚[22],Teng等[23]发现使用0.4![]() 0.5 mg/kg环泊酚麻醉诱导时的镇静效果与使用2 mg/kg丙泊酚相当,可将0.4
0.5 mg/kg环泊酚麻醉诱导时的镇静效果与使用2 mg/kg丙泊酚相当,可将0.4![]() 0.5 mg/kg环泊酚作为无痛结肠镜检查的推荐诱导剂量。
0.5 mg/kg环泊酚作为无痛结肠镜检查的推荐诱导剂量。
本研究统计了3组患者不良事件的发生率及血流动力学变化,3组患者心动过缓、呃逆、术后恶心的发生率无明显异常,R1和R2组均未出现注射痛,且呼吸抑制发生率明显低于C组,R1组低血压发生率明显低于C组,而R2组低血压发生率低于C组但无统计学意义,诱导完成后3组患者血压均有所下降,R1,R2组患者下降幅度较C组低,表明环泊酚对患者循环抑制较轻,本研究观察到R1组患者在十二指肠乳头插管后及手术结束时平均动脉压高于入室平均动脉压,这可能与R1组环泊酚剂量的镇静效果不足有关。在其他临床应用中的研究也明确指出环泊酚注射痛发生率明显低于丙泊酚[24-25]。在Li等[22]在无痛胃镜和结肠镜的研究中环泊酚组注射痛发生率为4.9%,丙泊酚组为52.4%,这可能是环泊酚受试者满意度更高的原因;另外,研究中最常出现的药物不良反应包括低血压、窦性心动过缓、头晕、结合胆红素升高、QT间期延长、呼吸抑制、呼吸暂停和低氧血症,环泊酚组和丙泊酚组药物不良反应的发生率分别为31.3%和62.8%,表明环泊酚在胃镜和结肠镜检查中比丙泊酚更具优势。在新版《气管镜诊疗的镇静/麻醉专家共识》中提到环泊酚与丙泊酚在气管镜诊疗中应用效果的对比,表示前者在使用过程中呼吸系统不良事件发生率、低血压和心动过缓发生率均有降低趋势[26],这也与本研究得出的结果接近。
本研究存在一些不足之处。(1) 本试验因复苏区条件限制未能完整统计术后并发症、离院时间。(2) 所有患者均在深度镇静下完成诊疗,在西方国家,适度镇静是接受诊断性内镜检查患者的镇静目标水平,而在中国,大多数无痛诊疗是在深度镇静下进行的,然而对于最合适的镇静方法尚未达成共识。(3) 受试对象ASA分级为Ⅰ![]() Ⅱ级,年龄限制为18
Ⅱ级,年龄限制为18![]() 65岁,但有大量需要行ERCP诊疗的患者为65岁以上的老年人,老年患者往往存在合并疾病多、药物耐受差等问题,故关于环泊酚在老年患者及一般情况较差的患者行ERCP诊疗中的镇静效果仍需进一步研究。(4) 本研究中R1组和R2组采用了不同剂量环泊酚进行诱导,后续研究会增加舒芬太尼0.1 μg/kg复合0.4
65岁,但有大量需要行ERCP诊疗的患者为65岁以上的老年人,老年患者往往存在合并疾病多、药物耐受差等问题,故关于环泊酚在老年患者及一般情况较差的患者行ERCP诊疗中的镇静效果仍需进一步研究。(4) 本研究中R1组和R2组采用了不同剂量环泊酚进行诱导,后续研究会增加舒芬太尼0.1 μg/kg复合0.4![]() 0.5 mg/kg环泊酚诱导,以通过控制诱导用药剂量来控制镇静深度,更能准确对比不同剂量环泊酚术中维持的应用效果。
0.5 mg/kg环泊酚诱导,以通过控制诱导用药剂量来控制镇静深度,更能准确对比不同剂量环泊酚术中维持的应用效果。
综上所述,以0.1 μg/kg舒芬太尼联合0.5 mg/kg环泊酚诱导及1.5 mg/(kg·h)环泊酚术中维持方案在无痛ERCP中应用效果较好,兼具了镇静成功率高及不良事件发生率低的优点,可作为ERCP深度镇静的推荐剂量。
[1] 李鹏,王拥军,王文海.中国经内镜逆行胰胆管造影术指南(2018版)[J].临床肝胆病杂志,2018,34(12): 2537-2554.
[2] LICHTENSTEIN D R, JAGANNATH S, BARON T H, et al. Sedation and anesthesia in GI endoscopy[J].Gastrointest Endosc, 2008,68(5): 815-826.
[3] JEURNINK S M, STEYERBERG E W, KUIPERS E J, et al. The burden of endoscopic retrograde cholangiopancreatography(ERCP) performed with the patient under conscious sedation[J].Surg Endosc, 2012,26(8): 2213-2219.
[4] RAYMONDOS K, PANNING B, BACHEM I, et al. Evaluation of endoscopic retrograde cholangiopancreatography under conscious sedation and general anesthesia[J]. Endoscopy, 2002,34(9): 721-726.
[5] SNEYD J R, ABSALOM A R, BARENDS C R M, et al. Hypotension during propofol sedation for colonoscopy: a retrospective exploratory analysis and meta-analysis[J].Br J Anaesth, 2022,128(4): 610-622.
[6] STOGIANNOU D, PROTOPAPAS A, PROTOPAPAS A, et al. Is propofol the optimal sedative in gastrointestinal endoscopy?[J]. Acta Gastroenterol Belg, 2018,81(4): 520-524.
[7] 刘进,王东信,左云霞,等.环泊酚临床应用指导意见[J].中华麻醉学杂志,2021,41(2): 129-132.
[8] 姜元喜,陈莹,许树长.中国消化内镜质量控制现状、思考及未来[J].同济大学学报(医学版),2020,41(6): 805-810.
[9] FLORESCU V, P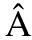 RVULE
RVULE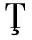 U R, ARDELEAN M, et al. The emergency endoscopic treatment in acute cholangitis[J]. Chirurgia, 2021,116(1): 42-50.
U R, ARDELEAN M, et al. The emergency endoscopic treatment in acute cholangitis[J]. Chirurgia, 2021,116(1): 42-50.
[10] ASGE Standards of Practice Committee, BUXBAUM J L, ABBAS FEHMI S M, et al. ASGE guideline on the role of endoscopy in the evaluation and management of choledocholithiasis[J]. Gastrointest Endosc, 2019,89(6): 1075-1105.e15.
[11] ETZKORN K P, DIAB F, BROWN R D, et al. Endoscopic retrograde cholangiopancreatography under general anesthesia: indications and results[J]. Gastrointest Endosc, 1998,47(5): 363-367.
[12] EBRU T K, RESUL K. Comparison of ketamine-propofol mixture(ketofol) and midazolam-meperidine in endoscopic retrograde cholangiopancretography(ERCP) for oldest old patients[J]. Ther Clin Risk Manag, 2019,15: 755-763.
[13] AKHTER A, PATEL R, NELSEN E, et al. Prospective comparison of moderate conscious sedation and anesthesia assistance for the performance of endoscopic retrograde cholangiopancreatography(ERCP)[J]. Can J Gastroenterol Hepatol, 2021,2021: 8892085.
[14] LIANG C M, KUO C M, LU L S, et al. A comparison between non-sedation and general endotracheal anesthesia for retrograde endoscopic common bile duct stone removal: a tertiary center experience[J]. Biomed J, 2019,42(2): 131-136.
[15] ASGE Standards of Practice Committee, EARLY D S, LIGHTDALE J R, et al. Guidelines for sedation and anesthesia in GI endoscopy[J]. Gastrointest Endosc, 2018,87(2): 327-337.
[16] 李兆申,邓小明,张澍田,等.中国消化内镜诊疗镇静麻醉专家共识意见[J].中国实用内科杂志,2014,34(8): 0254-1432.
[17] 国家消化内镜质控中心,国家麻醉质控中心.中国消化内镜诊疗镇静/麻醉操作技术规范[J].临床麻醉学杂志,2019,35(1): 81-84.
[18] 刘文超,梁淑娟,王现雷.丙泊酚联合艾司氯胺酮在内镜逆行胰胆管造影术中镇静有效性及安全性[J].世界临床药物,2022,43(9): 1124-1129.
[19] 孙永梅,张盼盼,孙国强,等.艾司氯胺酮在高龄患者ERCP中的有效性及安全性研究[J].中国现代普通外科进展,2023,26(10):807-809.
[20] LU Y Y, GU Y P, LIU L H, et al. Intravenous dexmedetomidine administration prior anesthesia induction with propofol at 4 ℃ attenuates propofol injection pain: a double-blind, randomized, placebo-controlled trial[J]. Front Med, 2021,8: 590465.
[21] HU C, OU X, TENG Y,et al.Sedation Effects Produced by a Ciprofol Initial Infusion or Bolus Dose Followed by Continuous Maintenance Infusion in Healthy Subjects: A Phase 1 Trial.[J].Adv Ther, 2021,38(11): 5484-5500.
[22] LI J X, WANG X, LIU J, et al. Comparison of ciprofol(HSK3486) versus propofol for the induction of deep sedation during gastroscopy and colonoscopy procedures: a multi-centre, non-inferiority, randomized, controlled phase 3 clinical trial[J]. Basic Clin Pharmacol Toxicol, 2022,131(2): 138-148.
[23] TENG Y, OU M C, WANG X, et al. Efficacy and safety of ciprofol for the sedation/anesthesia in patients undergoing colonoscopy: phase Ⅱa and Ⅱb multi-center clinical trials[J]. Eur J Pharm Sci, 2021,164: 105904.
[24] WANG X, WANG X, LIU J, et al. Effects of ciprofol for the induction of general anesthesia in patients scheduled for elective surgery compared to propofol: a phase 3, multicenter, randomized, double-blind, comparative study[J]. Eur Rev Med Pharmacol Sci, 2022,26(5): 1607-1617.
[25] CHEN X Q, GUO P, YANG L, et al. Comparison and clinical value of ciprofol and propofol in intraoperative adverse reactions, operation, resuscitation, and satisfaction of patients under painless gastroenteroscopy anesthesia[J]. Contrast Media Mol Imaging, 2022,2022: 9541060.
[26] 邓小明,王月兰,冯艺,等.(支)气管镜诊疗镇静/麻醉专家共识(2020版)[J].国际麻醉学与复苏杂志,2021,42(8): 785-794.