近年来,人们生活水平的不断提高,由于各种不良生活习惯及工作压力的增加,导致人们的消化道健康逐渐下降,消化道肿瘤的发病率则逐年上升[1]。内镜检查是早期消化道肿瘤诊断的最佳方法,广泛应用于临床诊断、治疗消化道肿瘤疾病中[2]。与手术相比,内镜切除术的侵袭性更小,住院时间短,出院时间快,成本更低。内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)是指利用各种电刀对大于2 cm的病变进行黏膜下剥离的内镜微创技术。近年来,术前口服碳水化合物缩短禁饮禁食时间在临床众多科室得到广泛应用,碳水化合物来源可选用单糖、双糖、低聚糖或多糖、麦芽糊精、葡萄糖聚合物或其他国标批准的原料,渗透压不宜高于320 mOsmol/kg[3]。根据加速康复外科(enhanced recovery after surgery, ERAS)和欧洲肠内肠外营养协会(European Society for Parenteral and Enteral Nutrition, ESPEN)2021的建议,术前口服碳水化合物可缩短禁食时间,术后早期开始口服喂养是可取的,可以改善预后,且不会增加术后再入院率[4]。迄今为止,术前口服碳水化合物被广泛使用,并已被证明有益,但是在内镜检查及治疗中的应用较少,目前也没有相关共识及指南供参考,尤其是ESD等新型领域的相关文献资料极为有限。随着内镜微创技术不断进展,临床开展ESD治疗早期胃癌趋于成熟。因此,本研究对ESD患者术前口服12.5%麦芽糊精果糖溶液的有效性、适用性及术后并发症情况进行分析,以期为早期胃癌患者行ESD围手术期提供更科学的营养方案,促进患者术后恢复。
1 资料与方法
1.1 一般资料
选取2022年7月—2023年4月同济大学附属第十人民医院消化内镜中心收治的行ESD手术的早期胃癌患者作为研究对象,进行单中心、前瞻性的随机对照研究。纳入标准: (1) 年龄为18![]() 70岁;(2) BMI为 18.5
70岁;(2) BMI为 18.5![]() 23.9 kg/m2;(3) 早期胃癌并准备行ESD手术;(4) 影像学资料未发现远处淋巴结及血液转移,满足手术及麻醉适应证;(5) ASA分级为Ⅰ
23.9 kg/m2;(3) 早期胃癌并准备行ESD手术;(4) 影像学资料未发现远处淋巴结及血液转移,满足手术及麻醉适应证;(5) ASA分级为Ⅰ![]() Ⅲ级。排除标准: (1) 胃肠功能受损、胃排空障碍、幽门梗阻、胃食管反流或误吸风险者;(2) 有严重的心肺疾病、血液病、凝血功能障碍以及服用抗凝剂的患者;(3) 糖尿病患者。本研究项目获得同济大学附属第十人民医院伦理委员会审核批准(SHYS-IEC-5.0/22K169/P01),并在中国临床试验注册中心注册(注册号: ChiCTR2200063748)。
Ⅲ级。排除标准: (1) 胃肠功能受损、胃排空障碍、幽门梗阻、胃食管反流或误吸风险者;(2) 有严重的心肺疾病、血液病、凝血功能障碍以及服用抗凝剂的患者;(3) 糖尿病患者。本研究项目获得同济大学附属第十人民医院伦理委员会审核批准(SHYS-IEC-5.0/22K169/P01),并在中国临床试验注册中心注册(注册号: ChiCTR2200063748)。
1.2 研究方法
符合纳入排除标准的患者签署知情同意书后,纳入本试验。按照1∶1比例随机的方法分为试验组及对照组。随机方法: 中心负责随机化的人员(不参与纳入受试者)登录中央随机系统获得随机号,最终形成随机分配表。两组患者均采用同种麻醉方法及用药方案。对照组患者行常规的术前准备,术前8 h禁食,4 h禁饮。试验组患者于术前8 h口服12.5%麦芽糊精果糖溶液(枢能特殊医学用途配方食品,渗透压约为290 mOsmol/kg,营养成分表: 能量213 kJ/100 mL、碳水化合物12.5 g/100 mL、钠50 mg/100 mL、钾66.7 mg/100 mL、磷63 mg/100 mL、氯65 mg/100 mL)800 mL,并禁食其他任何食物,术前2 h口服12.5%麦芽糊精果糖溶液400 mL。12.5%麦芽糊精果糖溶液中包含80%麦芽糊精、10%食用葡萄糖和10%结晶果糖。
1.3 观察指标
1.3.1 一般资料 记录两组患者年龄、性别、BMI、幽门螺旋杆菌感染情况、手术时间、住院时间及住院费用。
1.3.2 血生化指标及血清炎症因子 抽取患者术前、术后当日及术后第2天的空腹静脉血。实验室检查包括总蛋白(total protein, TP)、白蛋白(albumin, Alb)、前白蛋白(prealbumin, PA)、血红蛋白(hemoglobin, Hb)、淋巴细胞计数(lymphocyte count, LY)、空腹血糖(fasting blood glucose, FBG)、胰岛素、C反应蛋白(C-reactive protein, CRP)及电解质(包括钾、钠、氯、钙、磷、镁)水平。采用酶联免疫吸附法检测白细胞介素6(interleukin-6, IL-6)水平。
1.3.3 主观舒适度比较 采用视觉模拟评分法(visual analogue scale, VAS)对患者术前和术后24 h内进行评价,包括饥饿感、口渴感、疼痛感和焦虑感。
1.3.4 创伤后成长评定 治疗前后采用创伤后成长评定量表(post-traumatic growth inventory, PTGI)进行评估,PTGI共有21个条目,包括改善人际关系、获得新生活的可能性、自我成长、精神变化和欣赏生活5个维度[5]。采用6级评分法(0![]() 5分),调查个体在经历过创伤事件后的变化。量表总分105分,分值越高说明创伤后成长越多。
5分),调查个体在经历过创伤事件后的变化。量表总分105分,分值越高说明创伤后成长越多。
1.4 统计学处理
应用SPSS 25.0统计软件对研究数据进行分析和处理。计数资料以n(%)表示,行χ2或Fisher精确概率检验;符合正态分布的计量资料以均值±标准差![]() 表示,非正态分布或方差不齐采用Wilcoxon Mann-Whitney U秩和检验。重复测量的计量资料,采用重复测量方差分析,进行Mauchly’s球形假设检验,两两比较采用Bonferoni法对检验水准进行校正。组间比较采用t检验,P<0.05表示差异具有统计学意义。
表示,非正态分布或方差不齐采用Wilcoxon Mann-Whitney U秩和检验。重复测量的计量资料,采用重复测量方差分析,进行Mauchly’s球形假设检验,两两比较采用Bonferoni法对检验水准进行校正。组间比较采用t检验,P<0.05表示差异具有统计学意义。
2 结 果
2.1 患者基线资料比较
本研究选取消化内镜中心收治住院的行ESD手术的早期胃癌患者,按照纳入纳排标准共收集研究对象共120例,随机分成两组,每组60例。试验期间共脱落4例,试验组脱落3例,原因为患者未能按要求服用12.5%麦芽糊精果糖溶液,对照组1例患者因临时取消手术脱落。最终纳入116例,其中试验组57例,对照组59例。试验组中男27例,女30例,平均年龄(55.26±10.02)岁;对照组中男28例,女31例,平均年龄(58.20±10.37)岁。两组患者年龄、性别、BMI、手术时长、幽门螺旋杆菌感染情况比较差异均无统计学意义(P>0.05),具有可比性,见表1。
表1 两组患者一般资料比较
Tab.1 Comparison of general data between the two groups![]()
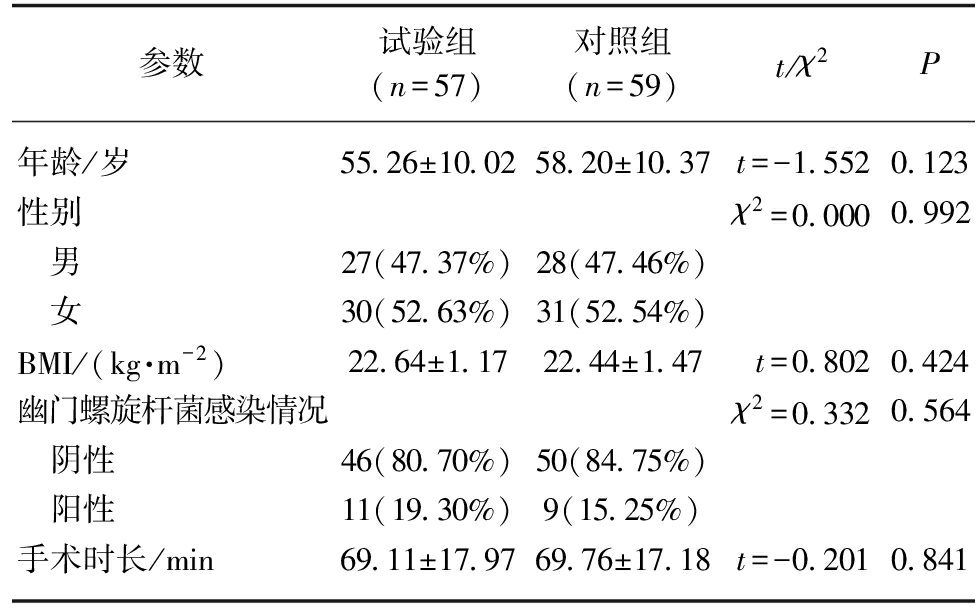
参数试验组(n=57)对照组(n=59)t/χ2P年龄/岁55.26±10.0258.20±10.37t=-1.5520.123性别χ2=0.0000.992 男27(47.37%)28(47.46%) 女30(52.63%)31(52.54%)BMI/(kg·m-2)22.64±1.1722.44±1.47t=0.8020.424幽门螺旋杆菌感染情况χ2=0.3320.564 阴性46(80.70%)50(84.75%) 阳性11(19.30%)9(15.25%)手术时长/min69.11±17.9769.76±17.18t=-0.2010.841
2.2 两组患者围手术期实验室指标比较
两组患者术前、术后第1天和术后第3天的实验室生化指标比较,使用重复测量方差分析判断口服12.5%麦芽糊精果糖溶液随着时间变化对患者血糖、胰岛素、电解质指标、营养指标和炎症因子指标的影响。
重复测量资料方差分析两组FBG与胰岛素水平,显示时间因素差异(P<0.001)及分组因素差异有统计学意义(P<0.05);时间因素与分组因素有交互作用(P<0.05)。两组患者术前指标比较差异无统计学意义(P>0.05)。在术后第1天两组的FBG和胰岛素水平较术前都有提高,但试验组升高幅度明显小于对照组(P<0.05),术后第3天都有下降,血糖下降后两组差异无统计学意义,胰岛素水平在术后第1天和第3天存在差异(P<0.05)。术后第1天两组均未见低血糖发生(FBG<4.2 mmol/L),对照组有36例(61.02%)血糖高于6.1 mmol/L,试验组有8例(14.04%)血糖高于6.1 mmol/L,差异有统计学意义(P<0.05)。术后第3天两组患者FBG均在正常范围内。
电解质指标、营养指标及炎症指标均随时间因素显著变化(P<0.05)。术前试验组与对照组电解质的差异无统计学意义(P>0.05);术后第1天和术后第3天两组患者血钾、钙和磷指标的差异具有统计学意义(P<0.05),分组效应表明术前口服12.5%麦芽糊精果糖溶液对患者术后电解质的水平有影响。交互效应提示干预因素和时间因素对两组患者的电解质水平(钾、钠、钙、磷和镁)是相互影响的(P<0.05),说明两组电解质水平在各时间点上的变化趋势不同,分组因素和时间因素对两组患者行ESD手术前后电解质水平的变化同时起作用,见表2。
表2 两组患者围手术期血糖、电解质、营养指标及炎症指标比较
Tab.2 Comparison of perioperative blood glucose, electrolyte, nutritional indexes and inflammatory indexes between the two groups![]()
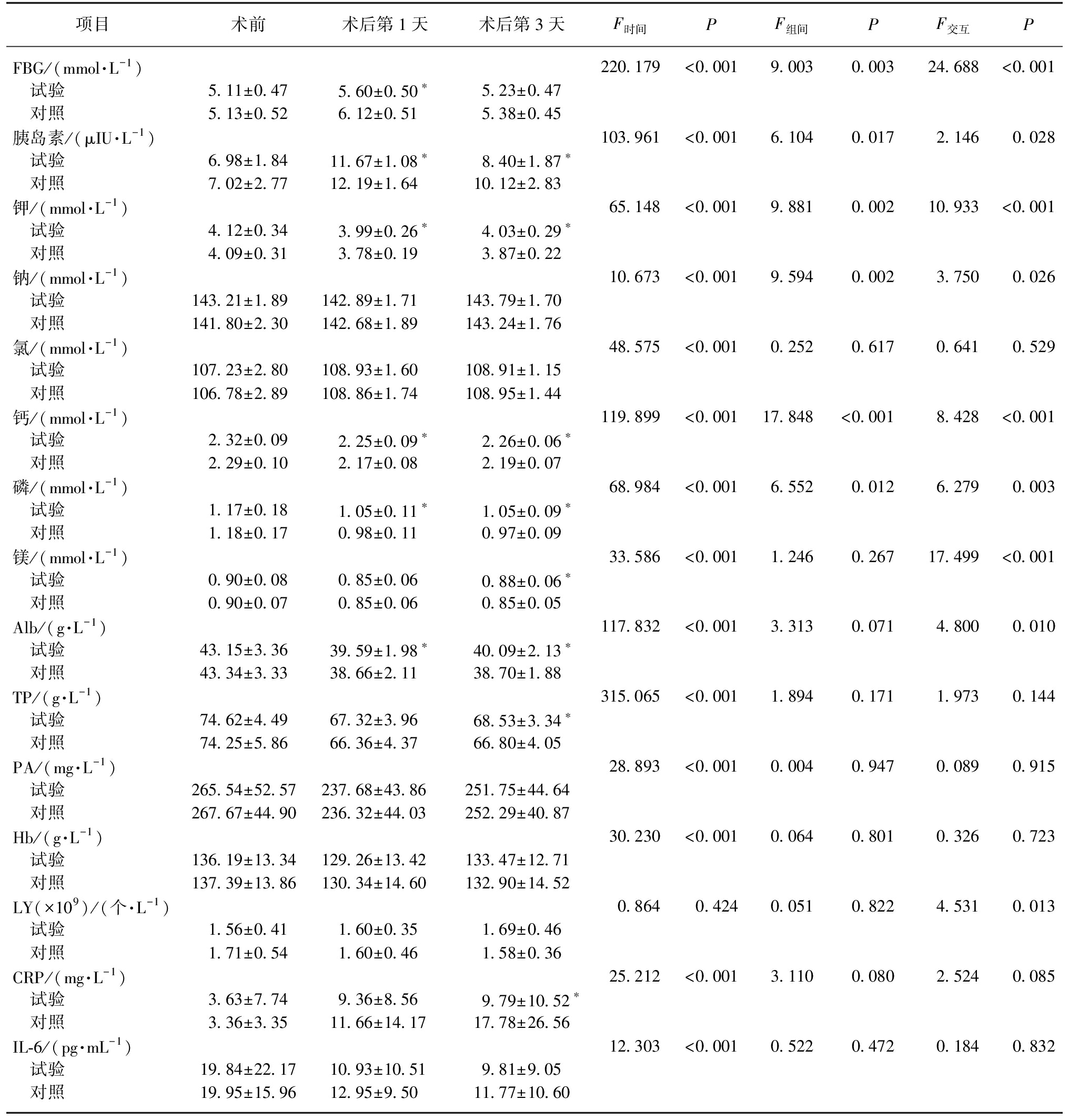
项目术前术后第1天术后第3天F时间PF组间PF交互PFBG/(mmol·L-1)220.179<0.0019.0030.00324.688<0.001 试验5.11±0.475.60±0.50∗5.23±0.47 对照5.13±0.526.12±0.515.38±0.45胰岛素/(μIU·L-1)103.961<0.0016.1040.0172.1460.028 试验6.98±1.8411.67±1.08∗8.40±1.87∗ 对照7.02±2.7712.19±1.6410.12±2.83钾/(mmol·L-1)65.148<0.0019.8810.00210.933<0.001 试验4.12±0.343.99±0.26∗4.03±0.29∗ 对照4.09±0.313.78±0.193.87±0.22钠/(mmol·L-1)10.673<0.0019.5940.0023.7500.026 试验143.21±1.89142.89±1.71143.79±1.70 对照141.80±2.30142.68±1.89143.24±1.76氯/(mmol·L-1)48.575<0.0010.2520.6170.6410.529 试验107.23±2.80108.93±1.60108.91±1.15 对照106.78±2.89108.86±1.74108.95±1.44钙/(mmol·L-1)119.899<0.00117.848<0.0018.428<0.001 试验2.32±0.092.25±0.09∗2.26±0.06∗ 对照2.29±0.102.17±0.082.19±0.07磷/(mmol·L-1)68.984<0.0016.5520.0126.2790.003 试验1.17±0.181.05±0.11∗1.05±0.09∗ 对照1.18±0.170.98±0.110.97±0.09镁/(mmol·L-1)33.586<0.0011.2460.26717.499<0.001 试验0.90±0.080.85±0.060.88±0.06∗ 对照0.90±0.070.85±0.060.85±0.05Alb/(g·L-1)117.832<0.0013.3130.0714.8000.010 试验43.15±3.3639.59±1.98∗40.09±2.13∗ 对照43.34±3.3338.66±2.1138.70±1.88TP/(g·L-1)315.065<0.0011.8940.1711.9730.144 试验74.62±4.4967.32±3.9668.53±3.34∗ 对照74.25±5.8666.36±4.3766.80±4.05PA/(mg·L-1)28.893<0.0010.0040.9470.0890.915 试验265.54±52.57237.68±43.86251.75±44.64 对照267.67±44.90236.32±44.03252.29±40.87Hb/(g·L-1)30.230<0.0010.0640.8010.3260.723 试验136.19±13.34129.26±13.42133.47±12.71 对照137.39±13.86130.34±14.60132.90±14.52LY(×109)/(个·L-1)0.8640.4240.0510.8224.5310.013 试验1.56±0.411.60±0.351.69±0.46 对照1.71±0.541.60±0.461.58±0.36CRP/(mg·L-1)25.212<0.0013.1100.0802.5240.085 试验3.63±7.749.36±8.569.79±10.52∗ 对照3.36±3.3511.66±14.1717.78±26.56IL-6/(pg·mL-1)12.303<0.0010.5220.4720.1840.832 试验19.84±22.1710.93±10.519.81±9.05 对照19.95±15.9612.95±9.5011.77±10.60
与对照组比较,*P<0.05;采用两因素重复检测方差分析;组间为分析组间效应;时间为针对组内不同时间点
分组效应说明术前口服12.5%麦芽糊精果糖溶液对患者的TP、Alb、PA、Hb、LY、CRP、IL-6均无影响。分组因素和时间因素对两组患者Alb和LY指标的作用是相互影响的(P<0.05),说明两组患者的Alb和LY指标在各时间点上的变化趋势不同。比较两组患者在3个时间点的营养指标及免疫指标的变化,分析数值显示,试验组患者Alb水平在术后持续高于对照组,差异具有统计学意义(P<0.05)。TP在行ESD手术后先降低后升高,试验组术后第3天的指标与对照组相比,差异有统计学意义(P<0.05)。
2.3 两组患者主观舒适度指标比较
与对照组相比,试验组术前及术后口渴感明显低于对照组(P<0.05)。与对照组相比,术前口服12.5%麦芽糊精果糖溶液能显著降低患者术后的饥饿感(P<0.001),但对疼痛感和焦虑感并无影响。见表3。
表3 两组患者主观舒适度指标比较
Tab.3 Comparison of subjective comfort indexes between the two groups![]()

组别饥饿感口渴感疼痛感焦虑感术前术后术前术后术前术后术前术后试验组(n=57)1.88±1.503.53±1.430.98±1.302.04±1.560.51±0.911.39±1.412.51±1.871.74±1.59对照组(n=59)1.92±1.455.49±1.411.54±1.432.90±1.820.49±1.011.51±1.792.85±1.962.34±1.73t-0.139-7.467-2.206-2.7430.097-0.409-0.095-1.953P0.890<0.0010.0290.0070.9230.6830.3440.053
2.3 两组患者术前术后PTGI情况比较
试验组术后PTGI评分高于对照组,差异具有统计学意义(P<0.05)。两组患者经历创伤后成长更多,对待人际关系的态度、精神状态及生活向往度明显改善(P<0.05),见表4。
表4 两组患者术前术后PTGI比较
Tab.4 Comparison of preoperative PTGI and postoperative PTGI between the two groups![]()
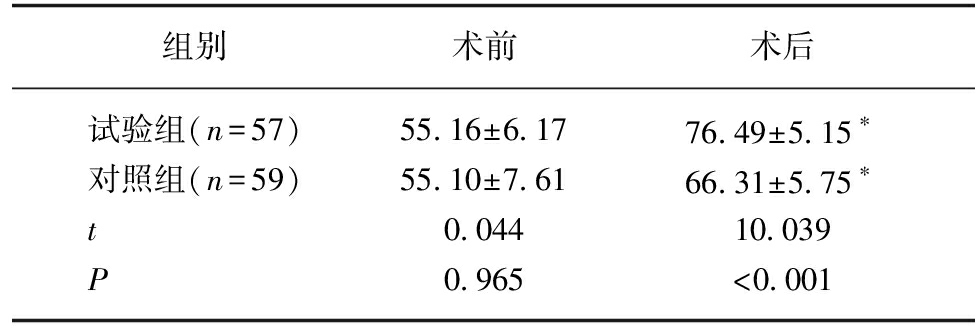
组别术前术后试验组(n=57)55.16±6.1776.49±5.15∗对照组(n=59)55.10±7.6166.31±5.75∗t0.04410.039P0.965<0.001
与术前比较,*P<0.05
2.4 两组患者术后并发症情况比较
所有患者围手术期均未出现反流误吸、肺部感染、穿孔。两组患者术后出血、恶心呕吐、腹胀腹痛的发生率比较,由于预测频次<5,采用Fisher精确概率检验,结果显示P>0.05,差异无统计学意义,见表5。
表5 两组患者并发症发生率比较
Tab.5 Comparison of complication rates between the two groups [n(%)]

并发症试验组(n=57)对照组(n=59)P术后出血2(3.51%)4(6.78%)0.679腹胀4(7.02%)3(5.08%)0.714腹痛02(3.39%)0.496恶心呕吐4(7.02%)7(11.86%)0.529
2.5 两组患者住院情况比较
试验组患者自手术当日到术后出院的时间较对照组相比缩短0.5 d,差异有统计学意义(P<0.001)。两组患者住院费用比较,差异无统计学意义(P>0.05),见表6。
表6 两组患者住院时间、住院费用比较
Tab.6 Comparison of hospital stay and hospital expenses between the two groups![]()

参数试验组(n=57)对照组(n=59)tP住院费用/元24213.01±5400.0026127.18±6260.71-1.761 0.081住院时间/d3.21±0.593.73±0.89-3.692<0.001
住院时间: 手术当日到出院
3 讨 论
ESD作为新型消化道微创技术,已广泛应用于临床早期癌症的治疗。ERAS的理念是指在患者围手术期应用一系列有效的措施,减少患者应激反应,快速恢复机体内环境平衡,减少术后并发症的发生率,加速患者康复,术前口服碳水化合物则是重要的代谢调控方式[4]。本研究探讨了ESD患者术前口服12.5%麦芽糊精果糖溶液的有效性、适用性及术后并发症情况。上消化道ESD患者术中及术后常见的不良反应包括恶心呕吐、腹痛、腹胀、反流误吸等,出血、穿孔则是上消化道ESD最常见的并发症。本研究中,两组患者术中均未发生反流、误吸或吸入性肺炎。两组患者术后出血、恶心呕吐、腹痛、腹胀情况无差异,证实术前实行口服12.5%麦芽糊精果糖溶液的方案是安全、可行的。
研究表明术前口服碳水化合物可以促进胰岛素的释放,减少术后分解代谢,改善机体氮平衡,从而达到改善胰岛素抵抗的目的[6-7]。《加速康复外科中国专家共识及路径管理指南(2018版)》推荐“术前10 h给予患者饮用12.5%的碳水化合物饮品800 mL,术前2 h饮用≤400 mL”,术后胰岛素抵抗发生率的降低有助于机体内环境的稳定,可以降低感染等并发症的发生率、围手术期死亡率及术后再入院率[8]。正常情况下,人体血糖波动处于正常范围,但当手术创伤、长时间禁食禁饮等应激条件下可出现胰岛素抵抗和血糖水平紊乱,不利于患者术后的恢复。本研究发现,术前两组患者的血糖值和胰岛素水平比较无差异,术后第1天两组指标较术前都有提高,但试验组升高幅度明显小于对照组,术后第3天都有下降,血糖下降后两组无差异,而胰岛素水平仍有差别,表明术前口服12.5%麦芽糊精果糖溶液可以减轻患者术后的胰岛素抵抗。两组均未见低血糖发生,术后第1天对照组出现高血糖的患者显著低于试验组,证明术前口服12.5%麦芽糊精果糖溶液能减缓围手术期应激性高血糖的发生,其原因认为在术前2 h口服12.5%麦芽糊精果糖溶液有助于机体产生合成代谢状态,减少糖原丢失,通过增加骨骼肌对葡萄糖的摄取从而控制高血糖发生[6-11]。
大多数研究只调查了不同体积、剂量或浓度下的碳水化合物的功效,尚未有研究针对补充含有电解质的12.5%麦芽糊精果糖溶液对ESD术后患者电解质变化的情况[12]。He等[13]报告了手术患者由于禁食和液体流失,通常会出现电解质紊乱,如低钠血症。本研究未有患者在围手术期出现电解质紊乱,术后第1天和第3天两组患者血钾、钙和磷指标的差异具有统计学意义,研究选用的12.5%麦芽糊精果糖溶液中含有钠(50 mg/100 mL)、钾(66.7 mg/100 mL)、磷(63 mg/100 mL)、氯(65 mg/100 mL),术前补充能有效维持体内水与电解质平衡,调节酸碱平衡。对于可能在围手术期出现的血红蛋白、前白蛋白等营养指标的下降[12],本研究也进行了分析,分组效应说明术前口服12.5%麦芽糊精果糖溶液对患者的TP、Alb、PA、Hb和LY均无影响,术后第3天,PA、Hb和LY恢复良好。这可能与纳入的患者本身不存在营养不良状态,及手术耐受能力较好相关。细胞因子CRP是评估应激严重程度的标志物,在创伤、感染等应激情况下,血清标志物升高。本研究结果显示,试验组的CRP水平在行ESD手术后升高,试验组术后第3天的指标与对照组相比,差异有统计学意义,说明术前口服12.5%麦芽糊精果糖溶液能够帮助降低应激反应。
本次研究表明术前口服12.5%麦芽糊精果糖溶液可以改善ESD患者的术后舒适度及感受。Meta分析发现术前口服12.5%麦芽糊精果糖溶液可改善患者主观舒适度VAS中的口干程度、饥饿感和口渴感[14]。Njoroge等[15]对择期手术患者进行的术前主观感受调查显示,当禁食时间超过15 h,禁饮时间超过12 h,出现重度饥饿的患者占35.4%,中度到重度口渴的患者占80%,27.7%的患者出现重度焦虑。术前长时间禁食禁饮会导致患者口腔中唾液腺的分泌失衡而引起口渴,同时对饥饿中枢的刺激影响表现为乏力和饥饿感的加重。行ESD术前禁食、禁饮时间过长,会导致机体内环境稳态被损坏,降低了患者的主观舒适度,出现口渴、疲劳乏力、焦虑等心理不适。本研究结果显示,两组患者随着禁食禁饮时间的增加,试验组患者在术前出现口渴感的比率低于对照组,且术前口服12.5%麦芽糊精果糖溶液能显著降低患者术后的口渴感和饥饿感,增加围手术期舒适度,这与其他研究中的结论一致。消化道早癌在行ESD围手术期会出现胃肠功能的紊乱,并通过脑-肠轴影响患者的中枢神经系统和日常行为能力,继而引发焦虑、抑郁等负面心理问题[16-17]。本次研究未显示两组焦虑感的VAS评分存在显著差异,但运用PTGI量表结果显示患者术后机体出现应激反应,试验组的患者PTGI评分明显高于对照组,患者在经历手术创伤后成长更多,其自身认知功能、社会功能及精神状态明显改善,这可能与碳水化合物摄入后血清素的分泌密切相关[18]。炎症因子IL-6水平被发现可能是胃肠道早癌术后胃肠功能紊乱及焦虑抑郁的诱发机制,可能与大量炎性细胞被激活而致使海马神经元凋亡相关[16]。但本研究未发现口服12.5%麦芽糊精果糖溶液对于IL-6在术后的变化差异,这可能与样本量较少、量表评估方式较单一相关。
Amer等[19]进行的Meta分析结果显示,术前口服碳水化合物可以缩短择期腹部手术患者的住院时间;国内研究也有同样报道[20]。本研究发现口服碳水化合物可以使患者术后住院时间缩短0.5 d,但由于ESD本身属于微创手术,对机体的创伤小,术后患者普遍住院天数为3![]() 4 d,总体住院时间不长,口服12.5%麦芽糊精果糖溶液对其效果并不突出。对照组和试验组住院费用虽然无显著性差异,但高于实验组,这可能与患者出现感染导致的护理天数增加有关,但由于本研究样本量较少,对统计有影响。
4 d,总体住院时间不长,口服12.5%麦芽糊精果糖溶液对其效果并不突出。对照组和试验组住院费用虽然无显著性差异,但高于实验组,这可能与患者出现感染导致的护理天数增加有关,但由于本研究样本量较少,对统计有影响。
目前术前口服12.5%麦芽糊精果糖溶液应用在早期胃癌ESD术式方面的报道较少,可能是由于胃手术部位的特殊性,容易引起误吸及反流等手术不良反应,临床对待术前口服碳水化合物的态度比较谨慎。本研究观察了术前口服12.5%麦芽糊精果糖溶液这一方式在早期胃癌中ESD术式中应用的有效性、适用性及术后并发症情况,为临床早癌患者提供了一种新选择。样本量较少是本研究的不足,在未来的研究中将纳入更多病例数,并进一步从患者依从性、不同时间段胃排空情况、住院费用等临床结局方面进行深入探讨。
综上所述,在行ESD术式的早期胃癌患者中,ERAS理念下的术前口服12.5%麦芽糊精果糖溶液方式能减轻患者应激反应,有助于机体内环境的稳定,维持电解质平衡,减少并发症的发生率,帮助改善患者术后的饥饿感、口渴感及精神状态。在不增加并发症和经济负担的情况下改善患者舒适度及创伤成长评分,值得临床推广。
[1] 曲默,邵楠,赵红彦,等.消化内镜技术对消化道肿瘤的早期诊断治疗意义[J].影像研究与医学应用,2019,3(9): 231-232.
[2] 滕晓琨,王国品,黄晓丽,等.内镜窄带成像技术对早期消化道肿瘤及癌前病变的诊断价值[J].中国临床研究,2017,30(1): 126-128.
[3] 中华人民共和国国家卫生和计划生育委员会.食品安全国家标准特殊医学用途配方食品通则: GB 29922—2013[S].北京: 中国标准出版社,2014.
[4] KEHLET H, WILMORE D W. Multimodal strategies to improve surgical outcome[J]. Am J Surg, 2002,183(6): 630-641.
[5] 耿亚琴,许勤,刘惠贤,等.中文版创伤后成长量表在多发伤幸存者中应用的信效度分析[J].中华护理杂志,2011,46(10): 1003-1005.
[6] LI J L, KANG G L, LIU T X, et al. Feasibility of enhanced recovery after surgery protocols implemented perioperatively in endoscopic submucosal dissection for early gastric cancer: a single-center retrospective study[J]. J Laparoendosc Adv Surg Tech A, 2023,33(1): 74-80.
[7] NOBA L, WAKEFIELD A. Are carbohydrate drinks more effective than preoperative fasting: a systematic review of randomised controlled trials[J]. J Clin Nurs, 2019,28(17-18): 3096-3116.
[8] 陈凛,陈亚进,董海龙,等.加速康复外科中国专家共识及路径管理指南(2018版)[J].中国实用外科杂志,2018,38(1): 1-20.
[9] POGATSCHNIK C, STEIGER E. Review of preoperative carbohydrate loading[J]. Nutr Clin Pract, 2015,30(5): 660-664.
[10] LIN M W, CHEN C I, CHENG T T, et al. Prolonged preoperative fasting induces postoperative insulin resistance by ER-stress mediated Glut4 down-regulation in skeletal muscles[J]. Int J Med Sci, 2021,18(5): 1189-1197.
[11] ONALAN E, ANDSOY I I, ERSOY O F. The effect of preoperative oral carbohydrate administration on insulin resistance and comfort level in patients undergoing surgery[J]. J Perianesth Nurs, 2019,34(3): 539-550.
[12![]() BA
BA ER M. Effect of preoperative oral liquid carbohydrate intake on blood glucose, fasting-thirst, and fatigue levels: a randomized controlled study[J]. Braz J Anesthesiol, 2021,71(3): 247-253.
ER M. Effect of preoperative oral liquid carbohydrate intake on blood glucose, fasting-thirst, and fatigue levels: a randomized controlled study[J]. Braz J Anesthesiol, 2021,71(3): 247-253.
[13] HE Y, TANG X M, NING N, et al. Effects of preoperative oral electrolyte-carbohydrate nutrition supplement on postoperative outcomes in elderly patients receiving total knee arthroplasty: a prospective randomized controlled trial[J]. Orthop Surg, 2022,14(10): 2535-2544.
[14] CHENG P L, LOH E W, CHEN J T, et al. Effects of preoperative oral carbohydrate on postoperative discomfort in patients undergoing elective surgery: a meta-analysis of randomized controlled trials[J]. Langenbecks Arch Surg, 2021,406(4): 993-1005.
[15] NJOROGE G, KIVUTI-BITOK L, KIMANI S. Preoperative fasting among adult patients for elective surgery in a Kenyan referral hospital[J]. Int Sch Res Notices, 2017,2017: 2159606.
[16] 申利敏,马用江,常卫华,等.微生态制剂联合帕罗西汀对ESD术后合并焦虑抑郁的胃肠道早癌患者的效果[J].国际精神病学杂志,2022,49(6): 1070-1073.
[17] 鲁花,范秀平.早期上消化道肿瘤患者内镜下黏膜剥离术前后心理焦虑和抑郁变化及影响因素[J].中国健康心理学杂志,2019,27(5): 715-718.
[18] NONOGAKI K. The regulatory role of the central and peripheral serotonin network on feeding signals in metabolic diseases[J]. Int J Mol Sci, 2022,23(3): 1600.
[19] AMER M A, SMITH M D, HERBISON G P, et al. Network meta-analysis of the effect of preoperative carbohydrate loading on recovery after elective surgery[J]. Br J Surg, 2017,104(3): 187-197.
[20] 李伟,陈一秋,郭盼盼,等.全程营养管理模式在泌尿系统恶性肿瘤手术患者加速康复中的应用[J].同济大学学报(医学版),2020,41(4): 487-491.