肝纤维化是指多种原因引起的肝细胞发生持续反复的坏死和修复,导致肝脏内广泛的细胞外基质过度沉积,主要为胶原蛋白,最终导致肝纤维化的发生,后期可发展为肝硬化甚至肝细胞癌[1]。肝纤维化早期诊断和及时干预可以逆转至正常,但是目前临床上针对性治疗肝纤维化的药物很少并且治疗效果因人而异[2-3]。近年来,越来越多的中药药理学研究发现中药有效成分对肝纤维化治疗十分有效,这成为了临床应对肝纤维化有力武器,且应用中药防治肝纤维化成本低患者易接受[4]。
铁皮石斛是我国的传统中药,其具有滋阴清热,养生保健,益胃生津等功效。多种药理研究已证明铁皮石斛具有广泛的抗肿瘤、抗氧化、提高免疫、降血糖、减轻急慢性肝损伤等作用[5]。异佛莱心苷(isoviolanthin)是一种黄酮苷类化合物,提取自铁皮石斛叶中。在肝癌细胞中,异佛莱心苷可通过调控TGF-β1/Smad和PI3K-AKT/mTOR通路抑制上皮间质转化,从而显著抑制TGF-β1介导的肿瘤迁移和侵袭[6]。黄芩素是一种研究广泛的黄酮苷类化合物,研究表明其可通过抑制NF-κB/NLRP3介导的上皮间质转化改善小鼠肺纤维化[7]。黄酮苷类化合物已经成为抗纤维化有前景的备选药物,然而,黄酮苷类化合物异佛莱心苷对肝纤维化及肝硬化的作用仍然未知,目前未见相关的报道。AKT/Smad2作为经典的纤维化相关信号通路,异佛莱心苷能否通过调控这一信号通路进而干预肝纤维化有待进一步探究。基于此,本研究通过腹腔注射四氯化碳(carbon tetrachloride, CC14)建立小鼠肝纤维化模型,在造模6周后,通过腹腔注射给药,观察异佛莱心苷对小鼠肝纤维化的保护作用及机制,以期为异佛莱心苷的临床应用提供研究基础。
1 材料与方法
1.1 实验动物
SPF级雄性C57BL6J小鼠24只,体重(22±1) g,购自常州卡文斯实验动物公司[许可证号: SCXK(苏)2021-0013],在温度22 ℃±1 ℃、湿度55%±5%的清洁级动物饲养室饲养,小鼠自由进食饮水。
1.2 试剂与仪器
CCl4和玉米油购自国药集团化学试剂有限公司;异佛莱心苷(isoviolanthin)购自美国Selleck公司;水飞蓟素胶囊购自德国Madaus GmbH公司;兔抗小鼠TGF-β1抗体购自美国Proteintech公司(21898-1-AP);AF-488标记的山羊抗兔二抗购自英国Abcam公司(ab150077);用于检测小鼠的白细胞介素(interleukin, IL)-1β、IL-6、肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)和转化生长因子-β1(transforming growth factor-β1, TGF-β1)ELISA试剂盒购自武汉伊莱瑞特公司;酶标仪和台式高速低温离心机为美国Thermo公司产品。
1.3 实验分组及干预措施
小鼠购入后观察并适应性饲养7 d,随机分为空白对照组(Control)、肝纤维化模型组(CCl4)、异佛莱心苷治疗组(CCl4+Iso)和水飞蓟素治疗组(CCl4+Sil),每组6只。纤维化模型组(CCl4)、异佛莱心苷组(CCl4+Iso)制备肝纤维化模型,具体方法为: 腹腔注射浓度为15%的CCl4玉米油溶液,每周2次,连续12周。从第6周起,CCl4+Iso组每日灌胃异佛莱心苷1次(10 mmol/L),CCl4+Sil组每日灌胃水飞蓟素100 mg/kg,连续给药6周。
1.4 血清肝功能指标测定
末次给药第2天,各组小鼠眼球采血,4 ℃离心(1 800×g,10 min)收集血清,使用全自动生化分析仪检测各组小鼠血清丙氨酸氨基转移酶(alanine aminotransferase, ALT)和天冬氨酸氨基转移酶(aspartate aminotransferase, AST)水平。
1.5 肝病理组织HE染色、Masson染色、Sirius Red染色
采血后处死小鼠,取肝组织于4%多聚甲醛溶液中固定24 h,常规脱水包埋切片,经脱蜡、水化、染色、分化、透明、封片、光学显微镜下观察并拍照。
1.6 组织免疫荧光染色
肝组织4%多聚甲醛固定24 h,蔗糖脱水后切冰冻片。3%H2O2室温避光孵育10 min,PBS洗3次(每次5 min),滴加5%山羊血清室温封闭2 h。滴加稀释好的一抗,4 ℃过夜,PBS洗3次(每次5 min),滴加稀释好的AF-488标记的山羊抗兔二抗,室温避光孵育30 min;PBS洗3次(每次5 min),滴加含DAPI的抗荧光猝灭封片剂。荧光显微镜拍照。
1.7 ELISA 法检测各组小鼠血清中TGF-β1、L-1β、IL-6、TNF-α水平
末次给药第2天,各组小鼠眼球采血,4 ℃离心(1 800×g,10 min)收集血清,血清中TGF-β1、IL-1β、IL-6和TNF-α的检测采用ELISA法,操作步骤严格按照试剂盒说明书进行。
1.8 Western印迹法
肝组织裂解后离心(1 800×g,10 min)离心10 min提取蛋白,加上样缓冲液后煮蛋白5 min。以10% SDS-PAGE凝胶进行电泳,电转至PVDF膜,经5%的BSA封闭1 h,稀释好的Smad2、p-Smad2、AKT、p-AKT和β-actin抗体4 ℃过夜孵育,TBST洗膜,室温孵育二抗1 h,TBST洗膜,ECL发光显色,Image J对条带进行灰度相对定量分析。
1.9 统计学处理
采用Graphpad软件进行数据统计学处理。呈正态分布的计量资料以均值±标准差![]() 表示,两组间比较采用t检验,多组间比较采用单因素方差分析,P<0.05为差异有统计学意义。
表示,两组间比较采用t检验,多组间比较采用单因素方差分析,P<0.05为差异有统计学意义。
2 结 果
2.1 造模后小鼠肝组织病理学和TGF-β1改变
首先检测造模后小鼠的肝组织病理情况来评估治疗效果。空白对照组小鼠HE染色中肝组织肝小叶结构完整正常,细胞整齐有规律,未见有肝细胞水肿和脂肪变,Masson和Sirius Red染色未见纤维化。肝纤维化模型组小鼠肝小叶结构破坏,细胞排列紊乱,可见严重的肝细胞水肿和脂肪变性并有明显的假小叶形成,汇管区炎细胞浸润。Masson和Sirius Red染色阳性区域较多。异佛莱心苷治疗组和水飞蓟素治疗组小鼠肝组织与纤维化模型比可见较为轻微的肝细胞水肿、脂肪变性,未见明显的假小叶形成,炎细胞浸润较少。Masson和Sirius Red染色表明有少量肝纤维形成(图1)。两组小鼠虽有比较严重的肝脏炎症,但纤维化水平较肝纤维化造模组明显改善,提示异佛莱心苷和水飞蓟素都具有良好的肝纤维化治疗作用。此外组织免疫荧光表明异佛莱心苷治疗组和水飞蓟素治疗组小鼠肝脏TGF-β1表达明显降低(图1D),提示异佛莱心苷和水飞蓟素对肝纤维化的改善作用可能和下调TGF-β1在肝组织中的表达相关。

图1 小鼠肝组织病理学和TGF-β1改变
Fig.1 Changes of liver histopathology and TGF-β1 level in mice
A: 肝组织HE染色(×200);B: 肝组织Masson染色(×100;×400);C: 肝组织Sirius Red染色(×100;×400);D: 肝组织TGF-β1组织免疫荧光染色(×200);E: 肝组织Masson染色、Sirius Red染色、TGF-β1组织免疫荧光染色结果定量分析;*P<0.05,**P<0.01,***P<0.001
2.2 造模小鼠血清肝功能检测结果
肝纤维化模型组小鼠血清ALT和AST较空白对照组显著升高(P<0.05),异佛莱心苷和水飞蓟素治疗后ALT、AST显著降低(P<0.05,图2A、B),而异佛莱心苷治疗组和水飞蓟素治疗组之间差异没有统计学意义(P>0.05)。此外,异佛莱心苷和水飞蓟素治疗可显著降低小鼠肝重和肝重/体重(P<0.05,图2C、E),但各组小鼠体重没有显著变化(P>0.05,图2D)。以上结果表明异佛莱心苷可有效改善CCl4导致的肝脏损伤,且治疗效果与水飞蓟素相当。
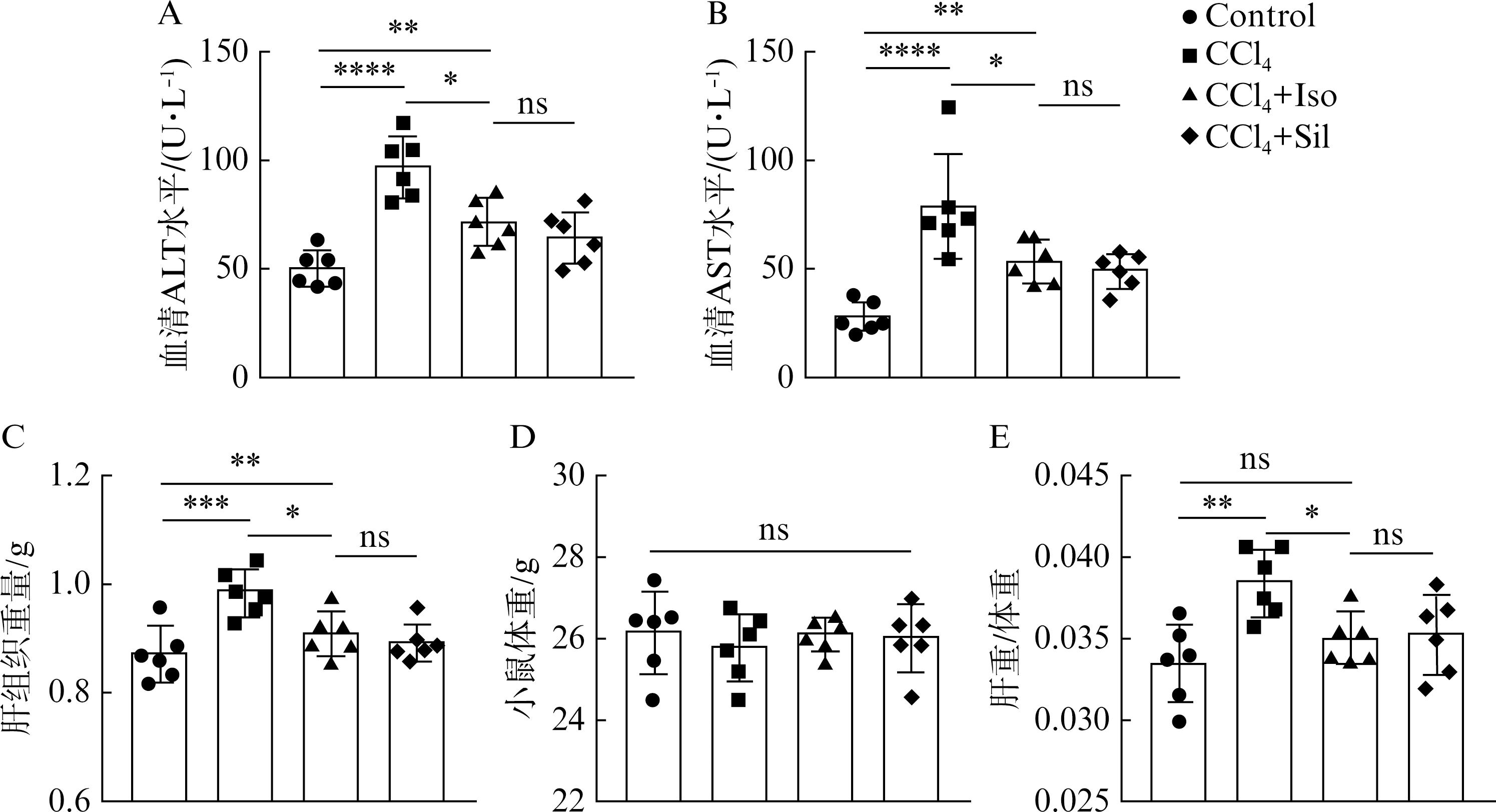
图2 小鼠肝功检测
Fig.2 Liver function tests of mice
A: 血清ALT;B: 血清AST;C: 肝组织重量;D: 小鼠体重;E: 肝重/体重;*P<0.05,**P<0.01,***P<0.001,****P<0.000 1,ns: P>0.05
2.3 小鼠血清炎症因子TGF-β1、IL-1β、IL-6、TNF-α变化
由于炎症参与了慢性肝纤维化的发生发展,本次实验检测了血清中4种主要的炎症因子TGF-β1、IL-1β、IL-6、TNF-α变化。结果证实肝纤维化模型组小鼠血清中TGF-β1、IL-1β、IL-6和TNF-α均高于空白对照组,差异有统计学意义(P<0.05)。通过异佛莱心苷的治疗,小鼠血清TGF-β1、IL-1β、IL-6和TNF-α较肝纤维化模型组均显著降低(P<0.05)。进一步比较异佛莱心苷治疗组和水飞蓟素治疗组之间的差异: 两组间IL-1β、IL-6水平没有差异(P>0.05),而异佛莱心苷治疗组的TGF-β1低于水飞蓟素治疗组(P<0.05),同时异佛莱心苷治疗组的TNF-α高于水飞蓟素治疗组未见明显差异(P<0.05),见图3。这一结果提示异佛莱心苷可明显下调CCl4所致的肝纤维化小鼠肝脏炎症水平,这可能是异佛莱心苷改善肝纤维化的潜在机制之一。

图3 血清中炎症因子变化
Fig.3 Changes of serum inflammatory factors in mice
A: 血清TGF-β1水平;B: 血清IL-1β水平;C: 血清IL-6水平;D: 血清TNF-α水平;*P<0.05,**P<0.01,***P<0.001,****P<0.000 1,ns: P>0.05
2.4 小鼠肝组织AKT/Smad2通路变化
目前已知AKT/Smad2通路在肝纤维化发生发展中起到重要的作用,Western印迹法检测肝组织AKT/Smad2通路蛋白表达。结果表明,肝纤维化模型组小鼠肝脏p-Smad、Smad2及p-AKT/AKT明显上升,提示AKT/Smad2信号通路被激活。异佛莱心苷治疗后p-Smad、Smad2及p-AKT/AKT较肝纤维化模型组显著降低(P<0.05),提示异佛莱心苷可抑制AKT/Smad2通路的激活,进而抑制肝纤维化的形成,见图4。
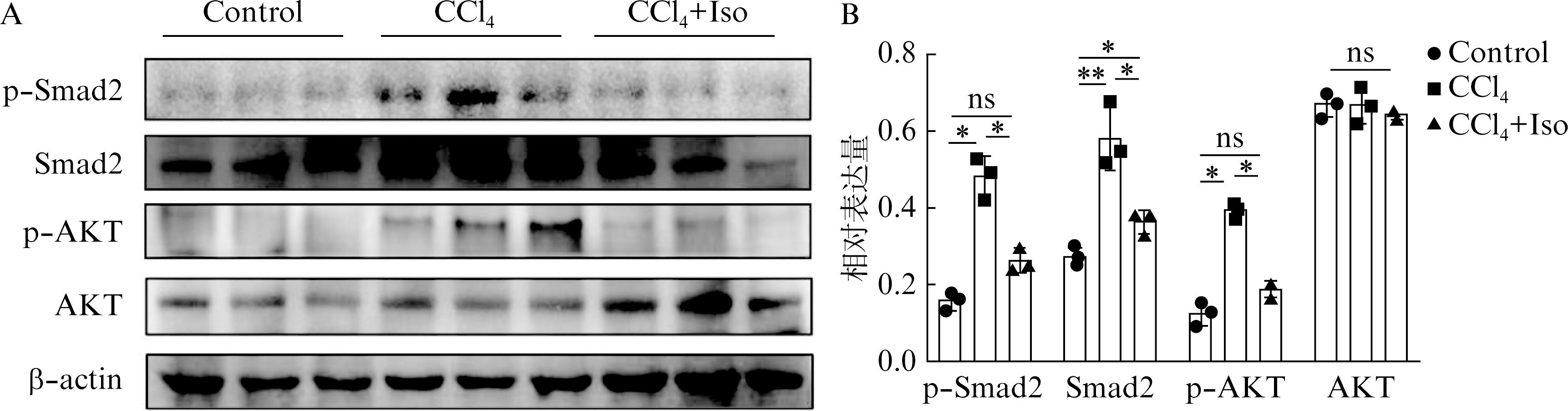
图4 肝组织AKT/Smad2通路变化
Fig.4 Changes of AKT/Smad2 pathway in mice liver tissue
A: Western印迹法检测肝组织AKT/Smad2表达;B: Western印迹法结果统计;ns: P>0.05,*P<0.05,**P<0.01
3 讨 论
肝纤维化是个慢性发展的过程,如果不及时干预阻止疾病进展,患者最终会发展为肝硬化和肝癌,造成极大的家庭和社会负担[8]。近年来,针对中药提取物的药理学研究非常广泛,中药和中药有效成分在解决许多临床问题中提供了更多的选择。CCl4可引起肝细胞的损伤,进而逐渐形成肝纤维化改变。本次研究通过对小鼠进行CCl4造模成功构建了肝纤维化模型,研究小鼠的肝脏组织病理、血清生化指标、血清炎症指标以及AKT/Smad2信号通路的表达变化。结果表明,异佛莱心苷的治疗可有效地改善肝脏的纤维化水平、降低血清肝功能中的ALT和AST水平、减轻肝脏的炎症水平、下调AKT/Smad2信号通路,进而改善CCl4导致的肝纤维化的发生。
目前已知诸多细胞因子及信号通路参与肝纤维化的调节,其中TGF-β1是目前已知最强的促纤维化细胞因子。当肝纤维化发生时,肝脏细胞中大量的TGF-β1分子及其下游的Smad通路在肝细胞胶原沉积中发挥关键促进作用[9]。本实验结果显示CCl4诱导的小鼠肝纤维模型中小鼠血清主要炎症因子TGF-β1、IL-1β、IL-6和TNF-α的水平显著升高,经异佛莱心苷组治疗后上述炎症因子水平显著降低,尤其是TGF-β1蛋白表达量。本次实验同时使用水飞蓟素治疗肝纤维化作为阳性对照,异佛莱心苷不亚于水飞蓟素的治疗效果,证实了异佛莱心苷具备良好的抗肝脏炎症作用,从而改善肝纤维化。
异佛莱心苷是一种黄酮类化合物,已有许多基础研究表明黄酮类化合物具有抗纤维化的作用。Li等[10]报道了一种天然的黄酮类化合物生松素,可以在体内或体外通过抑制TGF-β1通发挥抗皮肤纤维化的作用,这种机制提示了其抗纤维化作用可能与TGF-β1相关。AKT/Smad2通路广泛参与肝纤维化中肝细胞的增殖和分化[11]。2019年,幸尚平等[6]报道了在肝癌细胞中,异佛莱心苷可通过调控TGF-β1/Smad和PI3K-AKT/mTOR通路抑制上皮间质转化,从而显著抑制TGF-β1介导的肝癌细胞的增殖迁移。本研究发现异佛莱心苷治疗可显著抑制肝纤维化相关通路AKT/Smad2蛋白的表达的上升,其对肝纤维化的抑制效果可能与该通路相关。
本研究中设置了阳性对照组,通过比较发现异佛莱心苷对肝纤维化的抑制效果与水飞蓟素的治疗效果相当。但本研究仍存在一定的不足,本次未做体外实验探究异佛莱心苷对肝星状细胞活化的影响,后续的研究需针对这一问题进行探究。总之,本研究通过小鼠模型探究异佛莱心苷治疗肝纤维化,为黄酮类化合物在肝纤维化的临床应用提供的一定的研究基础。
[1] KISSELEVA T, BRENNER D. Molecular and cellular mechanisms of liver fibrosis and its regression[J]. Nat Rev Gastroenterol Hepatol, 2021,18(3): 151-166.
[2] GIN S P, KRAG A, ABRALDES J G, et al. Liver cirrhosis[J]. Lancet, 2021,398(10308): 1359-1376.
S P, KRAG A, ABRALDES J G, et al. Liver cirrhosis[J]. Lancet, 2021,398(10308): 1359-1376.
[3] 唐琴林,祝峻峰,王灵台,等.新清开方联合醒脑鼻嗅剂防治乙肝后肝硬化合并轻微型肝性脑病的临床研究[J].同济大学学报(医学版),2022,43(2): 209-215.
[4] SHAN L, LIU Z N, CI L L, et al. Research progress on the anti-hepatic fibrosis action and mechanism of natural products[J]. Int Immunopharmacol, 2019,75: 105765.
[5] 王治丹,代云飞,罗尚娟,等.铁皮石斛化学成分及药理作用的研究进展[J].华西药学杂志,2022,37(4): 472-476.
[6] 幸尚平.异佛莱心苷对肝癌细胞EMT的作用及其机制研究[D].广州: 广州中医药大学,2019.
[7] PENG L, WEN L, SHI Q F, et al. Scutellarin ameliorates pulmonary fibrosis through inhibiting NF-κB/NLRP3-mediated epithelial-mesenchymal transition and inflammation[J]. Cell Death Dis, 2020,11(11): 978.
[8] PAROLA M, PINZANI M. Liver fibrosis: Pathophysiology, pathogenetic targets and clinical issues[J]. Mol Aspects Med, 2019,65: 37-55.
[9] ROEHLEN N, CROUCHET E, BAUMERT T F. Liver fibrosis: mechanistic concepts and therapeutic perspectives[J]. Cells, 2020,9(4): 875.
[10] LI X H, ZHAI Y Q, XI B R, et al. Pinocembrin ameliorates skin fibrosis via inhibiting TGF-β1 signaling pathway[J]. Biomolecules, 2021,11(8): 1240.
[11] PARK S J, KIM T H, LEE K, et al. Kurarinone attenuates BLM-induced pulmonary fibrosis via inhibiting TGF-β signaling pathways[J]. Int J Mol Sci, 2021,22(16): 8388.