基于大数据的人工智能(artificial intelligence, AI)技术近年来得到快速发展。在医疗领域,随着数据资源的积累和技术的发展,AI也越来越多的在临床中得到应用,尤其是在医学影像领域,包括对病灶区域的分割及检测定位、疾病类型的分类及分级诊断、诊疗方法的推荐等。AI能够辅助临床医生进行诊断,提升医生的工作效率。
前列腺癌(prostate cancer, PCa)是男性中常见的恶性肿瘤,每年的新增发病率占男性癌症的第一位,死亡率在男性中仅次于肺癌排名第2[1]。前列腺磁共振成像(magnetic resonance imaging, MRI)技术由于其无创性和软组织分辨率高的优点在PCa的检测和诊断中发挥着越来越重要的作用[2-3]。通常临床医生是综合MRI图像和临床检查信息进行诊断,但由于精准的PCa诊断需要结合多参数MRI图像,这个过程极其的耗时且耗费精力,同时极大的依赖于医生的经验水平。利用AI的方法对前列腺MRI进行研究可以辅助临床医生进行诊断,提升其工作效率。本文将就AI在前列腺癌MRI诊断方向的研究进行综合性的总结分析。
1 人工智能的相关研究方法
机器学习(machine learning, ML)是AI的一个重要分支,可以通过计算机算法从大量历史数据中学习数据的特征和规律,从而实现对新样本进行预测。大多数的ML算法可以看作数学模型,将数据样本的观测变量(称为“特征”)映射到一组结果变量中(称为“标签”)[4]。ML主要是对算法的研究,算法通过训练过程进行优化得到模型,利用得到的模型可以进行结果预测,根据是否需要标签数据,其通常可以分为有监督学习和无监督学习。
有监督学习是利用专家标记的显式数据集进行模型训练得到预测模型,通常有监督学习可以得到较好的训练结果,但需要大量昂贵的标签数据。常见的有监督算法包括k-近邻算法,朴素贝叶斯分类,线性和逻辑回归,支持向量机(support vector ma-chine, SVM)和决策树等。
无监督学习仅根据训练数据的特征将样本最佳地分为不同的类别而无需使用标签,因为不需要专家的标记,此类算法通常可以利用大量数据的特征进行学习。常见的无监督学习算法包括k-means聚类,主成分分析(principal component analysis, PCA)和自编码器等。
深度学习(deep learning, DL)由Hinton等[5]于2006年提出,是ML的一个特殊应用领域,既可以应用在有监督学习方向,也可以应用在无监督学习方向,其通过构建含有多个处理层的人工神经网络、训练大量数据获取数据特征、预测新趋势、确定新模式,从而提高分类及预测的准确性。近年来因为大数据资源的汇集和使用,DL得到了广泛的发展。
卷积神经网络(convolutional neural networks, CNN)属于DL范畴,其结构较为简单,适用性较强,是目前计算机视觉和模式识别中较为高效的算法。CNN尤其是深度CNN在计算机视觉领域得到了快速发展,其在应用于数字化图像处理和模式识别时结果较好。CNN通常将原始图像作为输入,并通过模型训练获取数据的基本特征,进一步实现数字图像的分类、检测、定位等目标功能。
CNN本质是一种带有卷积结构的多层神经网络,但区别于传统的层与层之间的全连接架构模式,CNN采用稀疏的连接方式,具有局部连接和参数共享的重要特征。这样的连接方式可以深入分析该神经网络层与层之间的相关性,在提取具有因果关系数据的过程中效果显著[6]。
CNN通常是由卷积层、池化层组合构建而成,其基本结构如图1。
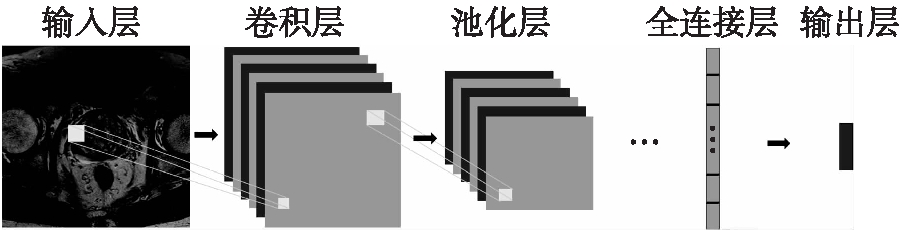
图1 CNN的结构成分
Fig.1 The structure of CNN
2 人工智能在前列腺MRI诊断中的临床应用
ML方法近年来在辅助临床医生进行诊断方面得到了快速发展,其研究方向涉及多个医学领域,包括乳腺癌、肺结节、皮肤病、PCa等。DL的方法能够有效的利用影像以及其他相关联数据信息,实现对感兴趣区(region of interest, ROI)的分割、检测和定位,完成不同疾病类型的分类和分级,辅助医生进行临床诊断。
目前,已有很多人工智能尤其是ML的方法应用在前列腺肿瘤的研究上。首先是利用AI的方法实现对前列腺器官的分割和对前列腺病灶区域的分割、检测和定位,帮助临床医生对ROI进行进一步的定性、定量分析,辅助其更好地进行前列腺肿瘤的诊断。其次是利用ML的方法对前列腺肿瘤的良恶性进行分类判别,识别临床显著癌,帮助临床医生提升其诊断效率,在这些研究中,充分利用前列腺临床检查中的不同检验数据能够提升模型的准确率,尤其是利用多参数MRI,能够显著地提升分类精度[7]。ML的方法还进一步应用在PCa的Gleason评分、病理分析、放疗计划以及治疗方案制订上。
2.1 前列腺器官分割
准确的前列腺器官分割对于前列腺临床研究具有重要作用。前列腺体积的测量计算、放疗计划的制定、活检穿刺和前列腺疾病的智能随访等实际场景应用中都需要前列腺器官的勾画,自动化的前列腺器官分割能够节省临床医生的工作时间,提升其工作效率,而且可以提高整个前列腺临床工作流的自动化程度。
目前流行的分割网络有U-Net、RCNN、SegNet、DeepLab、GAN等,而且有很多已应用于前列腺器官的自动分割,Zhu等[8]提出了一个深度监督CNN,利用卷积信息精确的从MRI图像中分割前列腺组织,该模型通过额外的深度监督层能够有效地检测前列腺器官。Milletari等[9]引入V-Net作为3D前列腺图像分割模型,此方法是基于体积的全卷积神经网络实现对前列腺图像的3D分割,通过一个端到端的网络模型可以实现一次性对整个前列腺MRI图像进行分割。Zhu等[10]还提出了一个递归神经网络(recursive neural network, RNN)URNet模型,他们将前列腺图像切片视为数据序列,并使用切片内的特征来改善前列腺分割的性能。此外,在临床工作中,第二版前列腺影像报告和数据系统(prostate imaging reporting and data system version 2, PI-RADSv2)已经得到了广泛应用[11-12],PI-RADSv2中对前列腺不同区域的评价标准不同[13],因此,前列腺不同区域的分割对于疾病的进一步诊断非常重要。在Zhu等[14]的研究中,利用级联U-Net结构网络对前列腺的外周带和移行带进行自动分割并且取得了整个前列腺器官平均Dice系数(dice similarity coefficient, DSC)为92.7,外周带平均DSC为79.3的令人满意的性能结果。
2.2 前列腺病灶检测
在腹腔的整个解剖结构中,前列腺是位于下腹部膀胱下方的器官,前列腺内病灶是前列腺的一部分,精确的前列腺病灶区域的检测定位是目前基于AI的计算机辅助诊断(computer aided diagnosis, CAD)的研究热点之一,因为它有助于提升放射科医生的诊断能力和可重复性。此外,病灶分割、检测是其他算法模型研究尤其是分类、分级等算法研究中的基础。可以通过病灶区域的检测定位有效的提取感兴趣可能发病区域和病变区域,从而作为后续分类模型训练数据的有效限定区域。
对前列腺病灶区域的检测方法有两种。一种是直接对病灶区域进行分割实现精准定位,Giannini等[15]提出了全自动的CAD系统实现了对PCa病灶区域的分割,其通过手动的特征提取方法对多参数MRI进行特征提取,然后通过分类器实现对于前列腺病灶区域的分割。Cao等[16]提出了一种改进的CNN,其利用多参数MRI实现PCa的检测和病灶轮廓的精确分割。另一种方法是直接对前列腺病灶进行识别,即如果存在PCa,则进一步定位病变区域。Ishioka等[17]利用CNN算法开发的CAD系统实现了对MRI图像的全自动PCa检测,该系统具有更高水平的标准化和一致性,还具有提供可再现解释的潜力。Yang等[18]提出了一种新颖的PCa检测系统,该系统利用弱监督CNN的方法学习整个前列腺图像的代表性病变特征,进而实现病灶区域的检测定位。该方法不同于大多数PCa自动检测系统需要依赖体素级别的分类标签,其只需要图像级别标注是否存在PCa,该系统首先通过自动识别是否存在PCa,一旦识别则进一步进行病变定位。
2.3 前列腺病灶的分类
MRI检查由于其无创性和软组织分辨率高在PCa检测和诊断方面发挥着越来越重要的作用,对PCa MRI图像进行辅助诊断研究则是目前前列腺MRI研究的重要方向之一,利用ML的方法进行PCa分类研究能够帮助临床医生提升其诊断效率,尤其是利用多参数MRI影像数据[19],能够显著提升分类精度。
Tsehay等[20]提出了一种基于多参数MRI使用CNN自动诊断PCa的CAD系统,通过他们的CAD系统在假阳性率20%时可以达到86%的检测率,而采用手工特征分析的传统技术的CAD系统在同样假阳性率下检测率只达到80%。Reda等[21]提出了基于CNN的全自动CAD系统,利用弥散加权成像(diffusion weight imaging, DWI)进行PCa早期诊断,该系统首先对前列腺进行分割,然后对分割出的区域进行特征提取,最后利用提取出的特征训练CNN分类器实现前列腺肿瘤恶性和良性划分。在更进一步的研究中,他们利用K近邻分类器将临床生物标志物PSA检查包含进来进行决策融合,最终达到了94.4%的诊断精度[22]。缺乏高质量的标注影像数据将会阻碍AI算法的研究,因此现在也有很多在自然图像的研究基础上进一步进行医疗影像研究,Yuan等[23]提出基于迁移学习的方法对PCa进行自动分类研究,他们的模型利用从ImageNet上学习到的知识促进多参数MRI特征的学习,并且进行特征联合提升PCa分类的鲁棒性。
2.4 Gleason评分分级
当临床检查中有迹象表明患者患有PCa,则需要对患者进行活检完成病理分级评价。Gleason评分系统是目前使用最普遍的PCa病理分级系统,该系统采用组织学分级的方法对PCa的危险程度进行评估,是PCa诊疗方案制订和疗效评价的重要指标。Gleason评分为主要结构类型评分加次要结构类型评分的总分值,通常Gleason评分<7为低危情况,Gleason评分=7为中危情况,Gleason评分>7为高危情况,其中对于Gleason评分=7的情况,则需要对其中3+4和4+3的情况做进一步分析,不同评分结果对于后续的诊疗处理有很大差别。目前已经分析了利用AI的方法对MRI影像进行检测、定位和分类的研究,未来将进一步看到基于ML和基因组学方法研究多参数MRI在Gleason评分系统中的应用。
PI-RADSv2中将Gleason评分≥7分定义为临床显著癌,Gleason评分<7分定义为临床非显著癌。Kiraly等[24]使用具有两个输出通道的CNN实现了对临床显著癌和临床非显著癌的体素级别标签预测,双通道输出可以实现检测和分类的同时进行。来自纽约斯隆·凯特琳纪念癌症中心的Fehr等[25]基于多参数MRI图像实现了对前列腺Gleason评分的自动分类,他们基于ML和特征选择的方法,联合表面弥散系数(apparent diffusion coefficient, ADC)和T2加权(T2 weighted imaging, T2WI)图像对Gleason评分=6(3+3)和≥7以及7(3+4)和7(4+3)情况进行自动分类,通过优化特征选择,最终对Gleason评分=6和≥7分类,在外周带和移行带都发生癌变情况下达到了93%的准确度,而对仅在外周带发生癌变情况下为92%的准确度;对Gleason评分为7(4+3)和7(3+4)分类,在外周带和移行带都发生癌变的情况下达到92%的准确度,仅在外周带发生癌变情况下为93%的准确率。Cao等[26]提出一个新颖的多分类CNN网络FocalNet,其联合检测PCa病灶和依据GS预测它们的侵袭性,FocalNet对病理证实为最具标志性病灶和临床显著癌的检出灵敏度分别为89.7%和87.9%,这个结果已经可与临床医生的诊断水平相媲美。
2.5 其他应用
除了在PCa病灶识别、分类、分级等方面的应用研究,AI近年来已经扩展到临床实践的各个阶段。ML的方法进一步应用在PCa的放疗计划制定[27]、治疗方案推荐[28]、术前干预[29]、疾病监测以及患者随访等多方面。
Nguyen等[27]修改卷积深度网络模型U-net,根据患者靶体积和风险器官的图像轮廓来预测放疗剂量,结果显示他们能够准确预测PCa患者的强度从而调控放射治疗的剂量。术前预测PCa生化复发(biochemical recurrence, BCR)的可能性具有明确的临床意义,最近的一项研究[29]利用SVM算法开发出一种基于图像的方法,预测PCa根治术后3年内的BCR,使用单变量和多变量分析来评估MRI结果和3年内BCR之间的关联,结果显示SVM方法优于基于常规的Logistic回归方法,实际上,与线性回归79%的准确度相比,ML的总体准确率为92.2%。不同模态的影像数据在临床诊断、治疗方案制订等临床场景中具有不同的应用效果,图像生成可以利用一种模态的数据生成更多模态的影像数据,拓展临床应用。Shafai-Erfani等[30]利用成对的CT和MRI数据集训练ML算法以便生成用于患者放射治疗设置和剂量计算的合成CT图像,事实证明,ML能够产生可靠的CT图像。
3 展 望
大量的研究表明,AI尤其是ML方法的快速发展,有很大的潜力可以改善前列腺MRI的诊断性能并且扩大其临床应用。目前AI在前列腺MRI的应用范围从分割、病变检测、侵袭性评估到之后的局部分期评估都已得到广泛发展。当前很多的应用研究都没有使用动态对比增强(dynamic contrast enha-nced, DCE)图像,正如指南建议的那样,AI可以避免将造影剂应用于前列腺检查[31]。当然目前AI的应用也存在很多问题,如模型的普适性问题需要更多外部数据进行更加强大的验证,尤其是不同扫描仪、扫描环境及扫描条件下的数据。其次是临床效果尤其是患者生存状况改善等实际场景验证,还需要投入更多的研究。最后是AI软件的使用,需要得到临床使用的许可,需要更加规范化的开发和使用环境。当然,近年来关于AI研究的数量和质量的增长也是不可否认的,而且也慢慢的在临床实践中帮助医生进行诊断和治疗,很难相信没有AI的前列腺MRI的未来,也期望AI在MRI临床实际应用中得到快速发展。
[1] SIEGEL R L, MILLER K D, JEMAL A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019,69(1): 7-34.
[2] 邓明,王良,胡道予,等.前列腺影像报告和数据系统指南(PI-RADS)解读及典型病例分析[J].放射学实践,2013,28(10): 998-1001.
[3] 邵志红,王伟,刘卫英,等.双参数与多参数MRI对不同PSA水平前列腺癌诊断的对比研究[J].同济大学学报(医学版),2020,41(4): 437-442.
[4] LARRY GOLDENBERG S, NIR G, SALCUDEAN S E. A new era: artificial intelligence and machine learning in prostate cancer[J]. Nat Rev Urol, 2019,16(7): 391-403.
[5] HINTON G E, SALAKHUTDINOV R R. Reducing the dimensionality of data with neural networks[J]. Science, 2006,313(5786): 504-507.
[6] 李晓坤,郑永亮,邵娜,等.基于AI技术在医学影像处理的应用[J].软件,2019,40(3): 46-51.
[7] AHMED H U, EL-SHATER BOSAILY A, BROWN L C, et al. Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer(PROMIS): a paired validating confirmatory study[J]. Lancet, 2017,389(10071): 815-822.
[8] ZHU Q, DU B, TURKBEY B, et al. Deeply-supervised CNN for prostate segmentation[C]∥2017 International Joint Conference on Neural Networks(IJCNN). Anchorage: IEEE, 2017: 178-184.
[9] MILLETARI F, NAVAB N, AHMADI S A. V-net: fully convolutional neural networks for volumetric medical image segmentation[C]∥2016 Fourth International Conference on 3D Vision(3DV). Stanford: IEEE, 2016: 565-571.
[10] ZHU Q K, DU B, TURKBEY B, et al. Exploiting interslice correlation for MRI prostate image segmentation, from recursive neural networks aspect[J]. Complexity, 2018,2018: 1-10.
[11] 王伟,邵志红,黄兴鸿,等.动态对比增强对第二版前列腺影像报告与数据系统中外周带扩散加权成像评分3分的影响[J].中华医学杂志,2020,100(13): 1002-1006.
[12] 王伟,邵志红,曾嘉齐,等.不同计算化高扩散敏感系数对外周带前列腺癌第二版前列腺影像和数据报告系统中弥散加权成像评分的影响[J].中华医学杂志,2017,97(43): 3401-3405.
[13] PURYSKO A S, ROSENKRANTZ A B, BARENTSZ J O, et al. PI-RADS version 2: a pictorial update[J]. Radiographics, 2016,36(5): 1354-1372.
[14] ZHU Y, WEI R, GAO G, et al. Fully automatic segmentation on prostate MR images based on cascaded fully convolution network[J]. J Magn Reson Imaging, 2019,49(4): 1149-1156.
[15] GIANNINI V, MAZZETTI S, VIGNATI A, et al. A fully automatic computer aided diagnosis system for peripheral zone prostate cancer detection using multi-parametric magnetic resonance imaging[J]. Comput Med Imaging Graph, 2015,46(Pt 2): 219-226.
[16] CAO R, ZHONG X, SHAKERI S, et al. Prostate Cancer Detection and Segmentation in Multi-parametric MRI via CNN and Conditional Random Field[C]∥2019 IEEE 16th International Symposium on Biomedical Imaging(ISBI 2019) . Venice: IEEE,2019: 1900-1904.
[17] ISHIOKA J, MATSUOKA Y, UEHARA S, et al. Computer-aided diagnosis of prostate cancer on magnetic resonance imaging using a convolutional neural network algorithm[J]. BJU Int, 2018,122(3): 411-417.
[18] YANG X, LIU C Y, WANG Z W, et al. Co-trained convolutional neural networks for automated detection of prostate cancer in multi-parametric MRI[J]. Med Image Anal, 2017,42: 212-227.
[19] SONG Y, ZHANG Y D, YAN X, et al. Computer-aided diagnosis of prostate cancer using a deep convolutional neural network from multiparametric MRI[J]. J Magn Reson Imaging, 2018,48(6): 1570-1577.
[20] TSEHAY Y K, LAY N S, ROTH H R, et al. Convolutional neural network based deep-learning architecture for prostate cancer detection on multiparametric magnetic resonance images[C]∥SPIE Medical Imaging. Proc SPIE 10134, Medical Imaging 2017: Computer-Aided Diagnosis, Orlando, Florida, USA. 2017, 1013: 1013405.
[21] REDA I, GHAZAL M, SHALABY A, et al. A novel ADCs-based CNN classification system for precise diagnosis of prostate cancer[C]∥2018 24th International Conference on Pattern Recognition(ICPR). Beijing: IEEE, 2018: 3923-3928.
[22] REDA I, KHALIL A, ELMOGY M, et al. Deep learning role in early diagnosis of prostate cancer[J]. Technol Cancer Res Treat, 2018,17: 153303461877-5530.
[23] YUAN Y X, QIN W J, BUYYOUNOUSKI M, et al. Prostate cancer classification with multiparametric MRI transfer learning model[J]. Med Phys, 2019,46(2): 756-765.
[24] KIRALY A P, NADER C A, TUYSUZOGLU A, et al. Deep convolutional encoder-decoders for prostate cancer detection and classification[M]∥Medical Image Computing and Computer Assisted Intervention-MICCAI 2017. Cham: Springer International Publishing, 2017: 489-497.
[25] FEHR D, VEERARAGHAVAN H, WIBMER A, et al. Automatic classification of prostate cancer Gleason scores from multiparametric magnetic resonance images[J]. Proc Natl Acad Sci USA, 2015,112(46): E6265-E6273.
[26] CAO R M, MOHAMMADIAN BAJGIRAN A, AFSHARI MIRAK S, et al. Joint prostate cancer detection and gleason score prediction in mp-MRI via FocalNet[J]. IEEE Trans Med Imaging, 2019,38(11): 2496-2506.
[27] NGUYEN D, LONG T, JIA X, et al. A feasibility study for predicting optimal radiation therapy dose distributions of prostate cancer patients from patient anatomy using deep learning[J]. Sci Rep, 2019,9(1): 1076.
[28] NEZHAD M Z, SADATI N, YANG K, et al. A Deep Active Survival Analysis approach for precision treatment recommendations: Application of prostate cancer[J]. Expert Syst Appl, 2019,115: 16-26.
[29] ZHANG Y D, WANG J, WU C J, et al. An imaging-based approach predicts clinical outcomes in prostate cancer through a novel support vector machine classification[J]. Oncotarget, 2016,7(47): 78140-78151.
[30] SHAFAI-ERFANI G, WANG T H, LEI Y, et al. Dose evaluation of MRI-based synthetic CT generated using a machine learning method for prostate cancer radiotherapy[J]. Med Dosim, 2019,44(4): e64-e70.
[31] CUOCOLO R, CIPULLO M B, STANZIONE A, et al. Machine learning applications in prostate cancer magnetic resonance imaging[J]. Eur Radiol Exp, 2019,3(1): 35.