随着人口老龄化的进程,目前我国已经步入人口老龄化程度较高的国家之列。在上海,每三个户籍人口中就有1个是60岁以上老人。到2040—2050年,上海60岁以上老人占比将达44.5%,老龄化比例将超过日本的42.7%,成为全球老龄化程度最高的城市之一[1]。而痴呆作为一种年龄相关性疾病,在我国患病率约为5.56%[2]。痴呆已经成为威胁老年人健康的重要病因之一,成为越来越严重的公共卫生问题和社会问题。然而,目前还没有行之有效的控制痴呆疾病发展的方法。轻度认知功能障碍(mild cognitive impairment, MCI)是介于正常老龄与轻度痴呆之间的一种过渡状态,是指与当前年龄和教育程度不相符的认知低下,但并不影响正常的日常生活,因此容易被忽视。研究表明,MCI患者正在以每年10%~15%的速度进展为痴呆,远远高于认知正常老人1%~2%的进展速度,并且早期被识别诊断为MCI的患者中有50%会在3~4年进展为痴呆[3]。研究证明,早期对MCI患者进行运动、饮食、社交、认知训练等干预措施可以明显改善MCI患者的认知和记忆功能,从而延缓其向痴呆转变的进程。因此,对MCI进行早期筛查和干预已经成为延缓其向痴呆转变的重要突破口。MCI的Petersen诊断金标准以专业的神经心理学量表测评为主,对操作者要求高,需要具备专业的神经内科学知识[4],且目前临床上还没有明确的生物标记物或是大脑的影像学检查可以直接判定MCI的发生[5-6]。对于中国这样一个人口大国而言,每一位老人都能接受医院神经心理专科医生的认知评估几乎是不可能的。在大力推行分级诊疗的今天,MCI的早期筛查和诊断的任务就落在了社区卫生服务中心及全科医生。因此,探索一种操作简易、灵敏度高的MCI筛查工具迫在眉睫[7]。
全科医生认知功能评估量表(general practitioner cognitive function assessment scale, GPCOG)由澳大利亚学者BRODATY等于2002年编制,是专门为初级卫生保健实践设计的一种新型认知评估量表,具有简便、高效、对量表操作者专业要求低,耗时短等优点[8]。然而,对于GPCOG中文版能否有效筛查中国老年人群MCI,能否满足全科医生的使用需要,知之甚少。本研究对GPCOG中文版评分在MCI筛查中的信度及效度进行分析,并与MCI诊断金标准进行对比,寻求GPCOG中文版在社区老年人群中进行MCI筛查的最佳截断值,为实现全科医生应用GPCOG中文版量表进行社区MCI患者的筛查打下基础。
1 资料与方法
1.1 研究对象
选择2019年 3月—8月在上海市杨浦区定海社区卫生服务中心进行体检的65岁以上老年人群中通过筛查确诊为MCI老年患者110例(病例组)和认知正常老人112 例(对照组)。病例组入组标准: 所有MCI患者由2名神经心理学专科医师按照MCI的诊断标准筛选入组。(1) 符合MCI的Petersen诊断标准(a: 主诉记忆力减退≥3个月;b: 简易精神状态检查量表(MMSE)评分: 初中及以上24~26分,小学20~26分,文盲17~26分; c: 日常生活能力评定量表(ADL)评分≤18分;d: 全面衰退量表(GDS)评分为2~3级;e: 未达到痴呆诊断标准,临床痴呆评定量表(CDR)评分=0.5分;(2) 近期未服用对认知功能有影响的药物。对照组入组标准: 选取同期进行认知功能评估结果为正常的老人,(MMSE评分≥27分,CDR评分=0分,ADL评分≤16分)。排除标准: 有严重脏器疾病可影响脑功能者;近期(3个月内)有急性脑血管疾病史;脑肿瘤疾病者;有狂躁、谵妄等精神类疾病者;因听力、视力等身体障碍无法完成本调查者。本次研究得到了研究对象或者家属书面形式的知情同意,并通过杨浦区定海社区卫生服务中心伦理委员会的审批同意,编号: 伦审(2019)第1号。
1.2 研究方法
本次研究主要使用的认知评估量表及功能评定量表包括: GPCOG中文版、简易精神状态量表(mini-mental state examination, MMSE)、蒙特利尔认知评估基础量表(Montreal cognitive assessment-basic, MoCA-B)、临床痴呆评定量表(clinical dementia rating, CDR)等。GPCOG中文版量表总共分为两部分,一部分是对患者测试部分,另一部分是知情者测试部分。患者测试部分包括4个认知任务: 时间定位(日期)、视觉空间技能(时钟绘制测试)、情景记忆(报告最近的新闻事件)和延迟回忆(姓名和地址),知情者测试部分由6个关于患者当前日常功能的问题组成(记住最近发生的事情、回忆最近的谈话、在说话时找到正确的词语、管理财务和药物能力以及是否需要交通援助)[9]。患者测评部分总分为9分,分数越高表示损伤越小; 得分为9分时,提示无明显认知障碍;得分为5~8分时,应进行GPCOG知情者测评;得分为0~4分时,则需进行标准认知功能调查。GPCOG知情者测评部分总分为6分,得分为所有回答为“否”的条目的总和;4~6分提示无明显认知障碍;0~3分提示有认知障碍,应该进行标准的认知功能调查。国内外的研究均表明GPCOG量表用于认知功能评估具有较好的内部一致性和重测信度。[8]
MoCA-B 是一项总分为30分的认知功能测试,内容包含延迟回忆、视空间功能、执行能力、词语抽象概括能力、计算能力和注意力、语言能力、时间和地点定向力功能,完成测试大约需要10~15 min。MMSE评估了5个认知领域: 时间定向、地点定向、注意力和计算、回忆和语言,总分为30分。MMSE和MoCA-B是目前临床上广泛用于检测认知功能障碍的两种筛查工具[10]。
所有参与此次老年人体检过程中认知功能量表筛查的医师均为社区全科医生,全部参与神经心理评估的全科医生需要接受统一的认知功能筛查相关量表培训,在培训达标后方可对受评者进行认知功能量表评估。
1.3 统计学处理
按照上述入组标准筛选研究对象并进行分组,整理并收集研究对象的一般资料、量表数据等,录入电脑进行统计学分析。计量资料采用![]() 表示,计数资料用率来表示,组间差异分别用χ2检验和t检验进行分类变量和连续变量的比较。利用皮尔逊相关系数计算GPCOG中文版评分与MMSE、MoCA-B分值间的相关性,判断GPCOG中文版评分与MMSE、MoCA-B量表评分是否具有相关性及一致性;将年龄、性别和教育程度作为协变量和GPCOG、MMSE及MoCA-B评分进行探索性线性回归分析,以确定GPCOG、MMSE及MoCA-B评分是否受到参与者的人口统计学因素的影响。以Peterson诊断标准为金标准绘制ROC曲线,得到曲线下面积(AUC)以及GPCOG中文版评分各截断值所对应的灵敏度、特异度,选择最大约登指数(Youden index)对应的GPCOG中文版评分数为最佳截断值,判断GPCOG中文版量表在社区MCI筛查中的诊断价值。P<0.05为差异有统计学意义。
表示,计数资料用率来表示,组间差异分别用χ2检验和t检验进行分类变量和连续变量的比较。利用皮尔逊相关系数计算GPCOG中文版评分与MMSE、MoCA-B分值间的相关性,判断GPCOG中文版评分与MMSE、MoCA-B量表评分是否具有相关性及一致性;将年龄、性别和教育程度作为协变量和GPCOG、MMSE及MoCA-B评分进行探索性线性回归分析,以确定GPCOG、MMSE及MoCA-B评分是否受到参与者的人口统计学因素的影响。以Peterson诊断标准为金标准绘制ROC曲线,得到曲线下面积(AUC)以及GPCOG中文版评分各截断值所对应的灵敏度、特异度,选择最大约登指数(Youden index)对应的GPCOG中文版评分数为最佳截断值,判断GPCOG中文版量表在社区MCI筛查中的诊断价值。P<0.05为差异有统计学意义。
2 结 果
2.1 两组一般资料及MMSE、MoCA-B评分对比
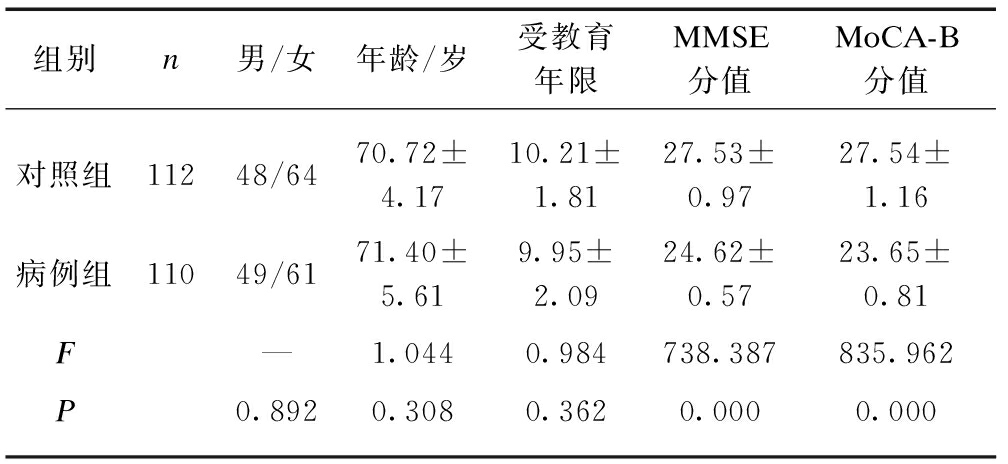
对病例组的年龄、性别、受教育年限与对照组差异无统计学意义(P>0.05);对照组的MMSE、MoCA-B量表评分高于病例组,差异有统计学意义(P<0.05),见表1。
表1 两组一般资料及MMSE、MoCA-B分值比较
Tab.1 Comparison of general data, MMSE and MoCA-B scores between the two groups ![]()
组别n男/女年龄/岁受教育年限MMSE分值MoCA-B分值对照组11248/6470.72±4.1710.21±1.8127.53±0.9727.54±1.16病例组11049/6171.40±5.619.95±2.0924.62±0.5723.65±0.81F—1.0440.984738.387835.962P0.8920.3080.3620.0000.000
2.2 量表的信度分析
2.2.1 内部一致性 GPCOG中文版量表患者部分各项目及知情者部分的Cronbach’s α系数为0.832,标准化后Cronbach’s α系数为0.834。
2.2.2 重测信度 从研究对象中随机抽取一组,在首次进行GPCOG中文版量表测试后的2~4周进行量表的重测。并对两次测试的结果进行相关性分析,结果显示两次测试的相关系数为0.908(P<0.01)。
2.3 量表的效度分析
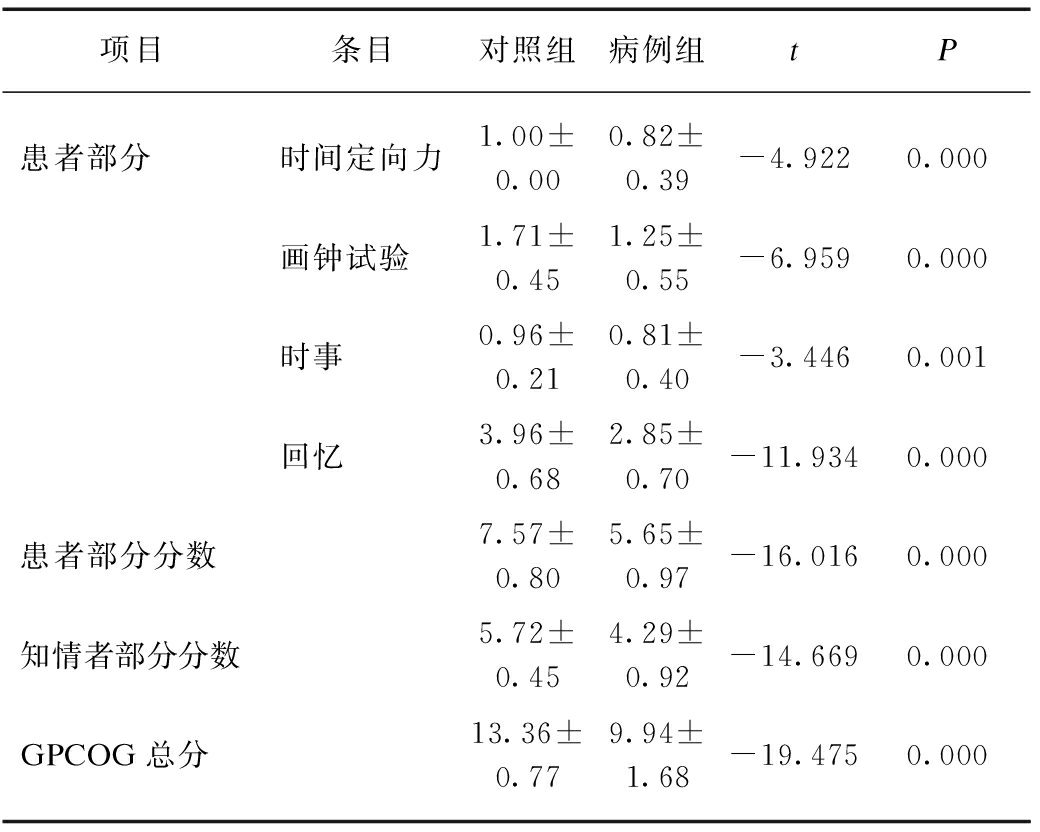
2.3.1 两组间GPCOG 总分和各项目评分对比对照组的患者部分分数、知情者部分分数以及 GPCOG总分均高于病例组,差异具有统计学意义(P<0.05);患者测试部分的时间定向力、画钟试验、时事、回忆,对照组评分亦均高于病例组,差异有统计学意义(P<0.05),见表2。
表2 两组GPCOG总分和各条目分对比
Tab.2 Comparison of GPCOG total scores and entries in the two groups ![]()
项目条目对照组病例组tP患者部分时间定向力1.00±0.000.82±0.39-4.9220.000画钟试验1.71±0.451.25±0.55-6.9590.000时事0.96±0.210.81±0.40-3.4460.001回忆3.96±0.682.85±0.70-11.9340.000患者部分分数7.57±0.805.65±0.97-16.0160.000知情者部分分数5.72±0.454.29±0.92-14.6690.000GPCOG总分13.36±0.779.94±1.68-19.4750.000
2.3.2 GPCOG总分与MMSE、MoCA-B 评分的相关性利用皮尔逊相关系数对两组研究对象的GPCOG中文版量表的评分与MMSE、MoCA-B 量表评分进行相关性分析,得出相关系数(r)分别为0.807、0.866,呈显著系相关(P<0.01)。
2.4 年龄、性别、受教育年限对GPCOG、MMSE、MoCA-B评分的影响
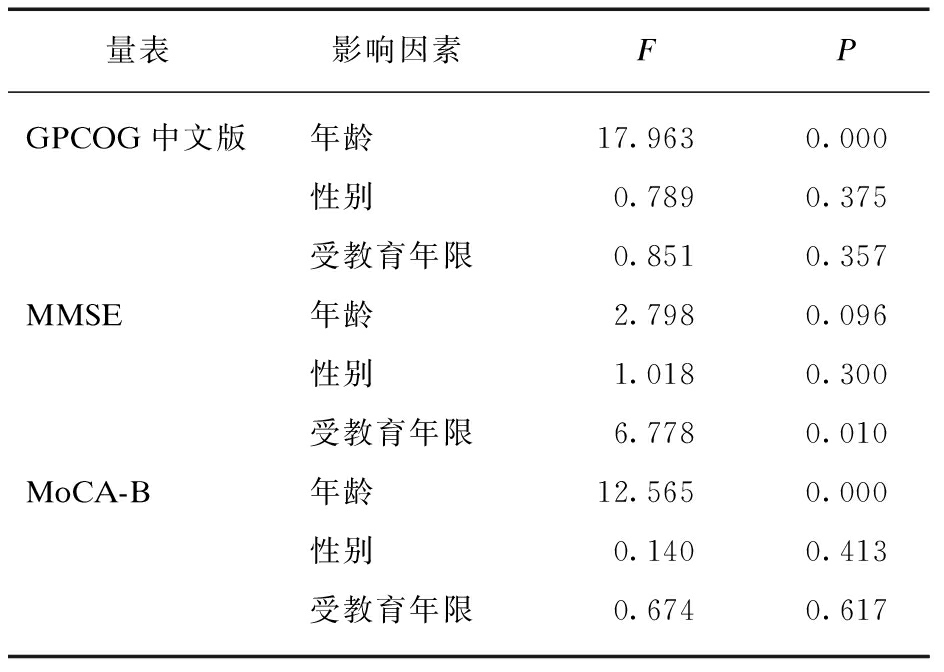
以 GPCOG、MMSE、MoCA-B评分为因变量,被试者年龄、受教育年限为协变量,性别及分组为固定因子,进行GLM分析,结果显示: 对于 GPCOG 总分的影响,被测试者的性别及受教育年限差异均无统计学意义(F分别为0.789、0.851,P>0.05); 而年龄相关的评分差异则具有统计学意义(F=17.963,P<0.05)。对于MMSE评分的影响,被测试者的受教育年限差异具有统计学意义(F=6.778,P<0.05); 而年龄和性别相关的评分差异则无统计学意义(F分别为2.798、1.018,P>0.05);对于MoCA-B评分的影响,被测试者的性别及受教育年限差异均无统计学意义(F值分别为0.140、0.674,P>0.05); 而年龄相关的评分差异则具有统计学意义(F=12.565,P<0.05),见表3。
表3 年龄、性别、受教育年限对GPCOG、MMSE、MoCA-B评分的影响分析
Tab.3 Influence analysis of age, gender and years of education on GPCOG, MMSE and MoCA-B scores
量表影响因素FPGPCOG中文版年龄17.9630.000性别0.7890.375受教育年限0.8510.357MMSE年龄2.7980.096性别1.0180.300受教育年限6.7780.010MoCA-B年龄12.5650.000性别0.1400.413受教育年限0.6740.617
2.5 GPCOG 对MCI的诊断价值
以Peterson诊断作为诊断金标准绘制GPCOG 中文版进行MCI诊断的ROC曲线,得出曲线下面积(AUC)为0.954,同时得出以GPCOG中文版量表评分总分12分作为截断值时,存在最大约登指数(Youden index),对应的灵敏度为86.6%,特异度为89.1%,见图1。

图1 GPCOG中文版量表筛查MCI的ROC曲线
Fig.1 The ROC of MCI was screened by GPCOG Chinese scale
3 讨 论
由于缺乏社会认知以及医疗资源的不足,MCI及痴呆目前还没有被列入到我国老年人的常规体检筛查及慢性病管理项目中。初级卫生保健实践往往会忽视这些记忆力减退的早期信号,直到各项认知功能障碍变得明显。全科医生作为社区老年人认知状况的最初接触者,有义务对其早期认知衰退信号进行识别和评估[11]。MMSE和MoCA是目前临床应用最为广泛的认知筛查工具,但在社区基层实践中这两类认知评估量表并不是最好的选择,均存在着对操作者要求高、耗时以及评分受到被试的文化程度、语言及社会经济地位的影响[12]。在众多可用的认知筛查工具中,根据诸如测试时间短(一般<5 min)、使用简单(不需要专业设备)和患者可接受性好等因素,已经设计或推荐了一些专门用于初级卫生保健的认知评估量表,其中包括简易智力状态评估量表(Mini-cog)、6个项目认知受损测试(6-item cognitive impairment test, 6CIT)等。然而,这些评估量表都没有在初级保健环境中得到充分的验证,并且缺少敏感性、可靠性和效度方面的数据[13-14]。GPCOG是专门为初级卫生保健开发的一项认知筛查评估工具,综合其测试评估时间(4~6 min)、诊断准确性、预测价值以及最小的文化、语言及教育偏差,被多项研究积极推荐应用于初级卫生保健中。且GPCOG是一项免费的纸笔测试,并已被翻译成23种以上的语言[15],具有较高的灵敏度和特异度,相关研究已证明其与MMSE具有较好的一致性,而且执行速度更快[16-17]。
本研究结果表明,GPCOG中文版量表具有良好的内部一致性及重测信度,从两组间观察对象的GPCOG的各项评分结果可以看到,除患者测评部分中的时事一项评分区分不够明显外,其余各项目评分均存在着显著差异。因此,GPCOG中文版量表在进行MCI的筛查中具有较好的区分效度,对MCI老人与正常老人进行区分时具备效果显著的特征。另外,其评分与目前国内外专科临床应用最为广泛的MMSE、MoCA-B量表评分呈显著正相关,提示该工具具有较高的聚合效度。研究还表明,GPCOG中文版的评分不会受到性别及教育程度等因素的影响,且该量表对操作者要求低、简便、高效,值得在临床上进一步推广应用[18]。由于认知障碍是一种年龄相关性疾病,因此,GPCOG中文版评分受到年龄因素影响,被试的年龄越大,在测评过程时犯错的概率就越大。本次研究通过ROC曲线分析还证实了以GPCOG总分12分作为截断值时,存在最大约登指数,对应的灵敏度为86.6%,特异度为89.1%,对正常老人与MCI老人进行区分时,效果较为理想。通过此次研究结果得出结论,GPCOG中文版是一种可靠的认知筛查工具。
有必要进行进一步的研究,与使用GPCOG这样的组合量表相比,使用单独的、简短的基于患者表现的量表(如6CIT, MMSE, Mini-cog)和基于知情者调查的量表(如AD8),哪一种测试评估方式更好。另外,本研究还存在一些局限性,如此次研究选取的研究对象来自社区参加常规体检的老人,并对其增加了认知评估的项目,而不是在社区>65岁人群中进行随机抽取符合入组条件的人群。研究对象存在着年龄分布范围相对较窄、样本量少等局限性。进一步的研究应该包括不同年龄段、不同社会经济地位和教育背景的社区人群大样本来探讨和证实上述观点。
[1] 上海统计局.上海人口老龄化现状和预判[EB/OL].(2018-11-23).[2019-12-20].http:∥www.stats-sh.gov.cn
[2] 健康中国行动推进委员会.健康中国行动(2019—2030年) [EB/OL].(2019-07-09).[2019-12-20].http:∥www.nhc.gov.cn/guihuaxxs/s3585u/201907/e9275f-b95d5b4295be8308415d4cd1b2/files/470339610aea4a-7887d0810b4c00c9bd.pdf
[3] LIMONGI F, NOALE M, BIANCHETTI A, et al. The instruments used by the Italian centres for cognitive disorders and dementia to diagnose mild cognitive impairment(MCI)[J]. Aging Clin Exp Res, 2019,31(1): 101-107.
[4] CANNON P, LARNER A J. Errors in the scoring and reporting of cognitive screening instruments administered in primary care[J]. Neurodegener Dis Manag, 2016,6(4): 271-276.
[5] KOURTIS L C, REGELE O B, WRIGHT J M, et al. Digital biomarkers for Alzheimer & apos; s disease: the mobile/wearable devices opportunity[J]. Npj Digit Med, 2019,2(1): 1-9.
[6] DUBOIS B, HAMPEL H, FELDMAN H H, et al. Preclinical Alzheimer & apos; s disease: Definition, natural history, and diagnostic criteria[J]. Alzheimers Dement, 2016,12(3): 292-323.
[7] YANG Y, XIAO L D, DENG L, et al. Nurse-led cognitive screening model for older adults in primary care[J]. Geriatr Gerontol Int, 2015,15(6): 721-728.
[8] 朱敏捷,肖世富,林翔,等.GPCOG中文版对轻度认知功能障碍和正常老人的评分比较[J].东南大学学报(医学版),2018,37(2): 289-292.
[9] IATRAKI E, SIMOS P G, BERTSIAS A, et al. Cognitive screening tools for primary care settings: examining the ‘Test Your Memory’ and ‘General Practitioner assessment of Cognition’ tools in a rural aging population in Greece[J]. Eur J Gen Pract, 2017,23(1): 171-178.
[10] 陈阳,于德华,杨蓉,等.国内外认知功能障碍常用筛查量表及其社区应用[J].中国全科医学,2018,21(12): 1392-1396.
[11] TONG T, TONG T, THOKALA P, et al. Cost effectiveness of using cognitive screening tests for detecting dementia and mild cognitive impairment in primary care[J]. Int J Geriatr Psychiatry, 2017,32(12): 1392-1400.
[12] MATE K E, MAGIN P J, BRODATY H, et al. An evaluation of the additional benefit of population screening for dementia beyond a passive case-finding approach[J]. Int J Geriatr Psychiatry, 2017,32(3): 316-323.
[13] WOJTOWICZ A, LARNER A J. General Practitioner Assessment of Cognition: use in primary care prior to memory clinic referral[J]. Neurodegener Dis Manag, 2015,5(6): 505-510.
[14] YOKOMIZO J E, SEEHER K, OLIVEIRA G M, et al. Cognitive screening test in primary care: cut points for low education[J]. Rev Saude Publica, 2018,52: 88.
[15] RASHEDI V, FOROUGHAN M, NAZARI H, et al. Validity and reliability of the Persian version of general practitioner assessment of cognition(P-GPCOG)[J]. Aging Ment Health, 2019,23(8): 961-965.
[16] HUNT H A, VAN KAMPEN S, TAKWOINGI Y, et al. The comparative diagnostic accuracy of the Mini Mental State Examination(MMSE) and the General Practitioner assessment of Cognition(GPCOG) for identifying dementia in primary care: a systematic review protocol[J]. Diagn Progn Res, 2017. Doi: 10.1186/s41512-017-0014-1.
[17] BRODATY H, CONNORS M H, LOY C, et al. Screening for dementia in primary care: a comparison of the GPCOG and the MMSE[J]. Dement Geriatr Cogn Disord, 2016,42(5-6): 323-330.
[18] XU F, MA J J, SUN F, et al. The efficacy of general practitioner assessment of cognition in Chinese Elders aged 80 and older[J]. Am J Alzheimers Dis Other Demen, 2019,34(7-8): 523-529.