随着社会人口老龄化以及高血压、糖尿病等基础疾病的增加,世界范围内,终末期肾病(end-stage renal disease,ESRD)呈不断上升趋势。我国目前ESRD患者已超过150万,每年新增约12万人[1]。腹膜透析作为ESRD的替代疗法之一,由于其操作便利,对血流动力学影响小以及卫生经济学成本低,逐渐被众多肾病患者接受,并且成为了ESRD居家治疗的主要手段。持续非卧床腹膜透析(continuous ambulatory peritoneal dialysis,CAPD)是目前主要的腹膜透析方式,随着治疗技术的日渐成熟和规范应用,如何进一步改善ESRD患者的治疗结局,一直备受关注。ESRD透析前基线状态是否对腹膜透析后远期生存时间产生影响,目前国内尚无相关报道。本研究通过随访观察,了解ESRD透析前状况对CAPD患者结局的影响,以早期采取必要的干预措施和监测手段,提高ESRD患者的生存率。
1 资料与方法
1.1 一般资料
选取2008年3月—2013年2月在同济大学附属同济医院肾内科接受腹膜透析置管术并在肾内科腹膜透析门诊规律随访的CAPD患者进行跟踪随访。询问疾病史、个人史及治疗史,于腹膜置管术入院时采集首次腹膜透析前基线生化检验资料,患者的基本信息和临床特点摘自电子病案以及面对面的问卷调查。纳入标准:(1) 18~80岁终末期肾病患者;(2) 在同济大学附属同济医院接受腹膜透析置管手术;(3) 持续非卧床腹膜透析3个月以上,规律门诊随访;(4) 同意参与本次调查研究。剔除标准:(1) 首次腹膜透析前相关生化检验资料缺失者;(2) 腹膜透析门诊未规律随访者;(3) 透析前已并存其他器官功能衰竭者;(4) 认知功能障碍者。本研究经同济大学附属同济医院伦理委员会批准,调查均取得患者知情同意。
患者常规使用1.5%或2.5%葡萄糖乳酸盐透析液,白天留腹4~6h,夜间留腹10~12h,每日透析总量6~10L。透析液均为低钙透析液,由上海百特医疗用品有限公司提供。终末期肾病的原发病:肾小球肾炎47例,糖尿病肾病48例,高血压肾病38例,其他肾病15例(多囊性肾病5例,肾病综合征3例,IgA肾病2例,尿酸性肾病2例,缺血性肾病2例,反流性肾病1例)。
1.2 方法
1.2.1 患者随访 随访日期为2008年3月—2018年2月。以门诊随诊为主,结合电话随访和家庭访视,1年以上未至门诊随诊,且电话随访无回应者视为失访,随访期间转肾移植、维持性血透者计入删失数据。
1.2.2 合并症指数 查尔森合并症指数(Charlson comorbidities index,CCI),将查尔森合并症指数量表中19个可能显著影响生存时间的合并症,按疾病的严重程度分别赋予不同加权值,最后得分作为CCI。
1.2.3 临床指标计算标准 平均动脉压,住院24h内测量平静状态下血压,平均动脉压(mean arterial pressure,MAP)=舒张压+(收缩压-舒张压)/3;残余肾功能,透析前残余肾功能的计算,以肾脏疾病饮食修正计算公式(modification of diet in renal disease,MDRD)和慢性肾病流行病学合作(chronic kidney disease epidemiology collaboration,CKD-EPI,60岁以上)公式计算估计肾小球滤过率(estimated glomerular filtration rate,eGFR)。校正血清钙计算公式:校正血清钙(mmol/L)=实测血清钙(mmol/L)+0.02×[40-Alb(g/L)]。
1.2.4 生活习惯 当前吸烟,是指每天至少1支烟,吸烟6个月或以上,且入院前仍有吸烟者;当前饮酒,是指每周至少饮酒一次,饮酒6个月以上,且入院前仍有饮酒者。
1.2.5 生化指标检测 入院后于次日晨采集空腹(8h以上)静脉血。总淋巴细胞计数(total lym-phocyte count,TLC)采用全自动血液细胞分析仪,血清白蛋白(albumin,Alb)的测定采用溴甲酚紫比色法,前白蛋白(prealbumin,PA)的测定采用免疫比浊法,血清全段甲状旁腺激素(immunoreactive parathyroid hormone,IPTH)测定采用化学发光法,血清钙、磷的测定采用间接离子选择电极法,血清胆固醇(total cholesterol,TC)、三酰甘油(triglyceride,TG)的测定采用酶法。
1.3 统计学处理
生存时间定义为首次腹膜透析日期至死亡或末次随访时间,随访终止目标为患者死亡、接受肾移植、转血透或放弃腹膜透析治疗。后3种情况与失访患者统一归入截尾数据处理。应用SPSS 19.0统计软件包进行统计分析,正态分布连续性变量的描述采用![]() 表示,分类变量采用百分数表示,变量值差别的显著性检验分别采用F检验或χ2检验。采用Kaplan-Meier法绘制生存曲线,计算生存时间。危险因素分析采用Cox比例风险回归模型(向前逐步法),计算风险比(hazard ratio,HR)及其95%置信区间(confidence interval,CI)。P<0.05为差异有统计学意义。
表示,分类变量采用百分数表示,变量值差别的显著性检验分别采用F检验或χ2检验。采用Kaplan-Meier法绘制生存曲线,计算生存时间。危险因素分析采用Cox比例风险回归模型(向前逐步法),计算风险比(hazard ratio,HR)及其95%置信区间(confidence interval,CI)。P<0.05为差异有统计学意义。
2 结 果
2.1 观察对象的临床特点
本组观察对象共148例,其中男性97例,女性51例(男女人数之比为1.9∶1),开始腹膜透析年龄为(61.4±15.0)岁,见表1。透析前eGFR为(6.81±3.43) mL/(min·1.73m2),血清Alb(28.3±5.6) g/L,其中血清Alb<25g/L的患者占28.4%;TLC(1.34±0.59)×109/L,三分位值分别为T1:(0.10~1.00)×109/L,T2:(1.10~1.50)×109/L,T3:(1.60~2.70)×109/L。血清钙磷乘积(51.80±14.67) mg2/L2,三分位值分别为T1:(24.0~45.5) mg2/L2,T2:(46.1~55.4) mg2/L2,T3:(55.7~137.0) mg2/L2。本组CAPD患者中,原发病前3位分布:糖尿病肾病48例(32.4%),慢性肾小球肾炎47例(31.8%)以及高血压肾病38例(25.7%)。
表1 不同Alb水平患者的临床特点
Tab.1 Clinical characteristics of patients with different serum albumin level
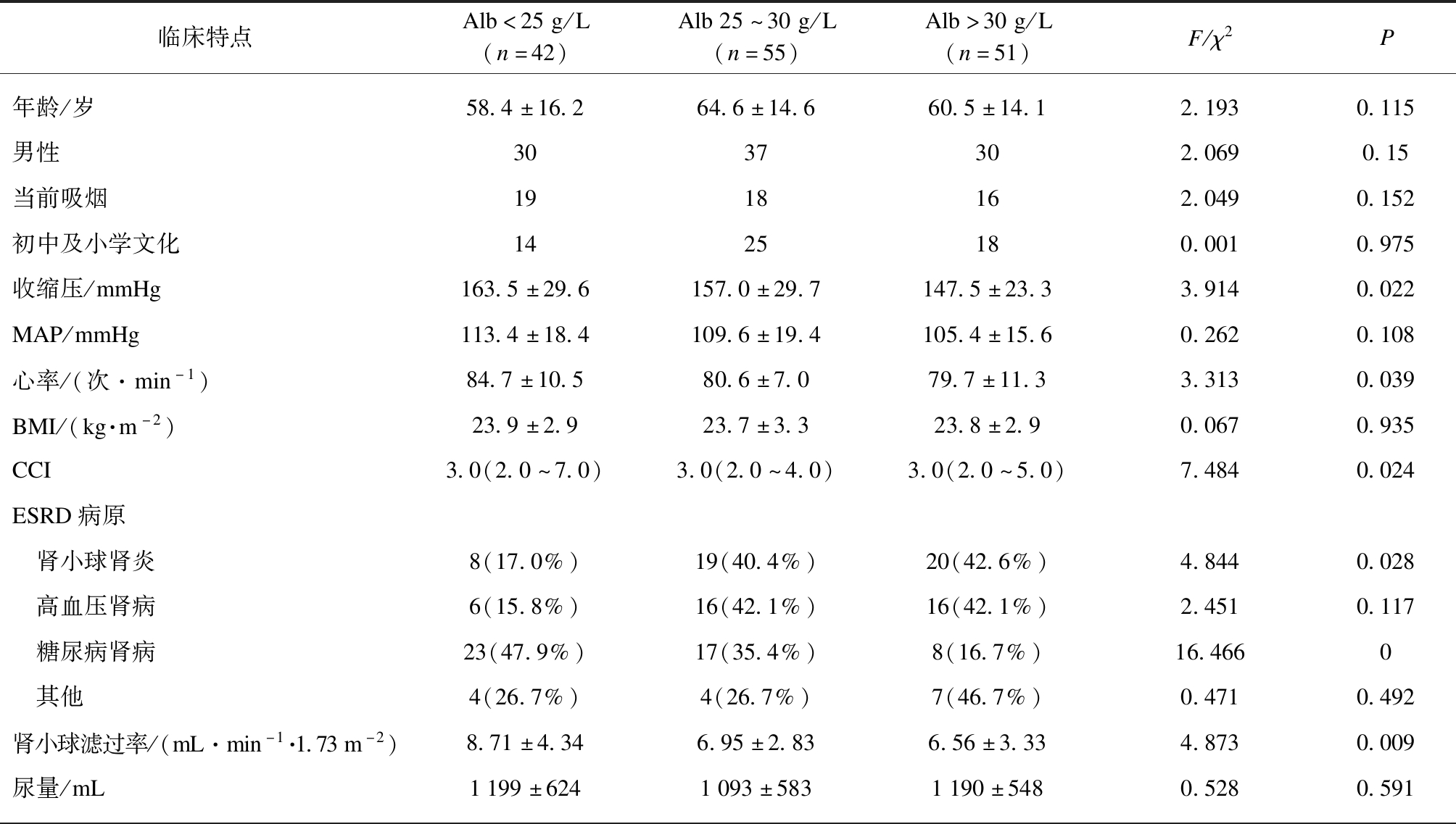
临床特点Alb<25g/L(n=42)Alb25~30g/L(n=55)Alb>30g/L(n=51)F/χ2P年龄/岁58.4±16.264.6±14.660.5±14.12.1930.115男性3037302.0690.15当前吸烟1918162.0490.152初中及小学文化1425180.0010.975收缩压/mmHg163.5±29.6157.0±29.7147.5±23.33.9140.022MAP/mmHg113.4±18.4109.6±19.4105.4±15.60.2620.108心率/(次·min-1)84.7±10.580.6±7.079.7±11.33.3130.039BMI/(kg·m-2)23.9±2.923.7±3.323.8±2.90.0670.935CCI3.0(2.0~7.0)3.0(2.0~4.0)3.0(2.0~5.0)7.4840.024ESRD病原 肾小球肾炎8(17.0%)19(40.4%)20(42.6%)4.8440.028 高血压肾病6(15.8%)16(42.1%)16(42.1%)2.4510.117 糖尿病肾病23(47.9%)17(35.4%)8(16.7%)16.4660 其他4(26.7%)4(26.7%)7(46.7%)0.4710.492肾小球滤过率/(mL·min-1·1.73m-2)8.71±4.346.95±2.836.56±3.334.8730.009尿量/mL1199±6241093±5831190±5480.5280.591
续表

临床特点Alb<25g/L(n=42)Alb25~30g/L(n=55)Alb>30g/L(n=51)F/χ2P生化指标 HB/(g·L-1)75.8±17.875.9±17.082.4±19.12.2320.111 TLC(×109)/(L-1)1.42±0.621.28±0.561.34±0.600.6510.523 PA/(g·L-1)0.299±0.0900.318±0.1060.349±0.0823.4060.036 Cr/(umol·L-1)726.1±407.2786.4±409.6842.5±353.01.0130.366 TC/(mmol·L-1)4.84±1.904.27±1.044.07±1.333.5120.032 TG/(mmol·L-1)1.41±0.941.63±1.361.42±0.850.6560.52 LDL/(mmol·L-1)2.89±1.442.37±0.692.33±0.983.9660.021 HDL/(mmol·L-1)1.08±0.461.01±0.370.95±0.351.0190.364 Ca/(mmol·L-1)1.88±0.241.92±0.252.02±0.402.540.082 P/(mmol·L-1)1.78±0.442.03±0.692.10±0.713.1920.044 CaxP/(mg2·dL-2)49.0±10.952.8±13.554.0±16.61.5380.218 IPTH/(pg·mL-1)221.8±2.5228.3±2.3297.6±2.41.5230.222
MAP:平均动脉压;CCI:查尔森合并症指数中位数(最小值~最大值);HB:血红蛋白;TLC:总淋巴细胞计数;PA:前白蛋白;Cr:肌酐;TC:胆固醇;LDL:低密度脂蛋白胆固醇;HDL:高密度脂蛋白胆固醇;CaxP:钙磷乘积(校正血清钙);IPTH:整分子甲状旁腺激素,为几何均数
2.2 随访结局分析
中位随访时间为78个月,随访期间有31例转入血透,3例接受了肾移植,死亡77例。3年生存率为71.2%,4年生存率为60.6%,5为年生存率53.7%,6年为生存率50.1%,见图1。死亡原因分析:心血管事件死亡25例、脑血管意外死亡16例、腹膜炎或肺部感染死亡10例、跌倒外伤死亡6例、癌症死亡5例,其他因放弃治疗死因不明15例。死亡原因中心脑血管占比达53.2%。
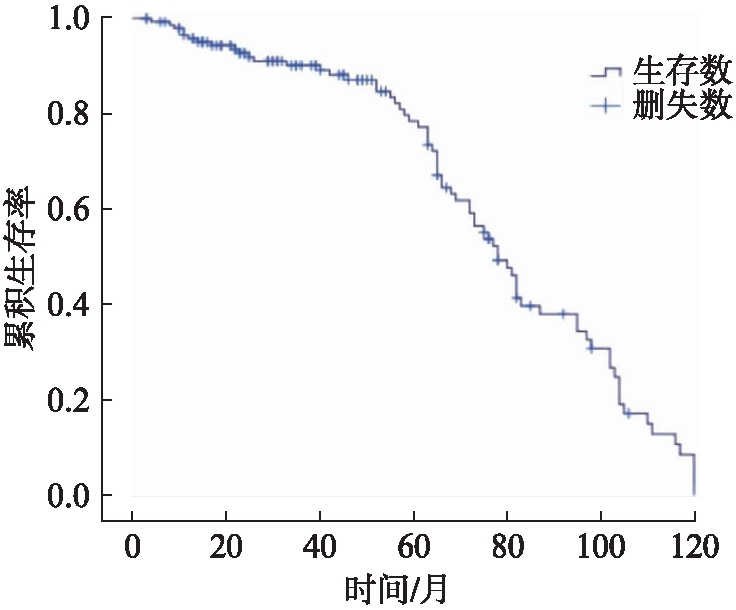
图1 本组观察对象的累积生存率
Fig.1 Cumulative survival of the subjects
2.3 心脑血管死因分析
以性别、年龄、MAP、吸烟、BMI、血清Alb、总胆固醇、钙磷乘积、CCI等作为协变量,Logistic回归分析显示,血清钙磷乘积是腹膜透析患者心脑血管死亡的独立危险因素。与高三分位血清钙磷乘积比较,中三分位血清钙磷乘积因心脑血管疾病死亡风险减少76.2%,(OR=0.238,95%CI:0.070~0.814,P=0.022),而低三分位钙磷乘积差异未显示出统计学意义(OR=0.859,95%CI:0.291~2.536,P=0.783),见表2。
表2 心脑血管死因的影响因素
Tab.2 Influencing factors of cardio-cerebrovascular death
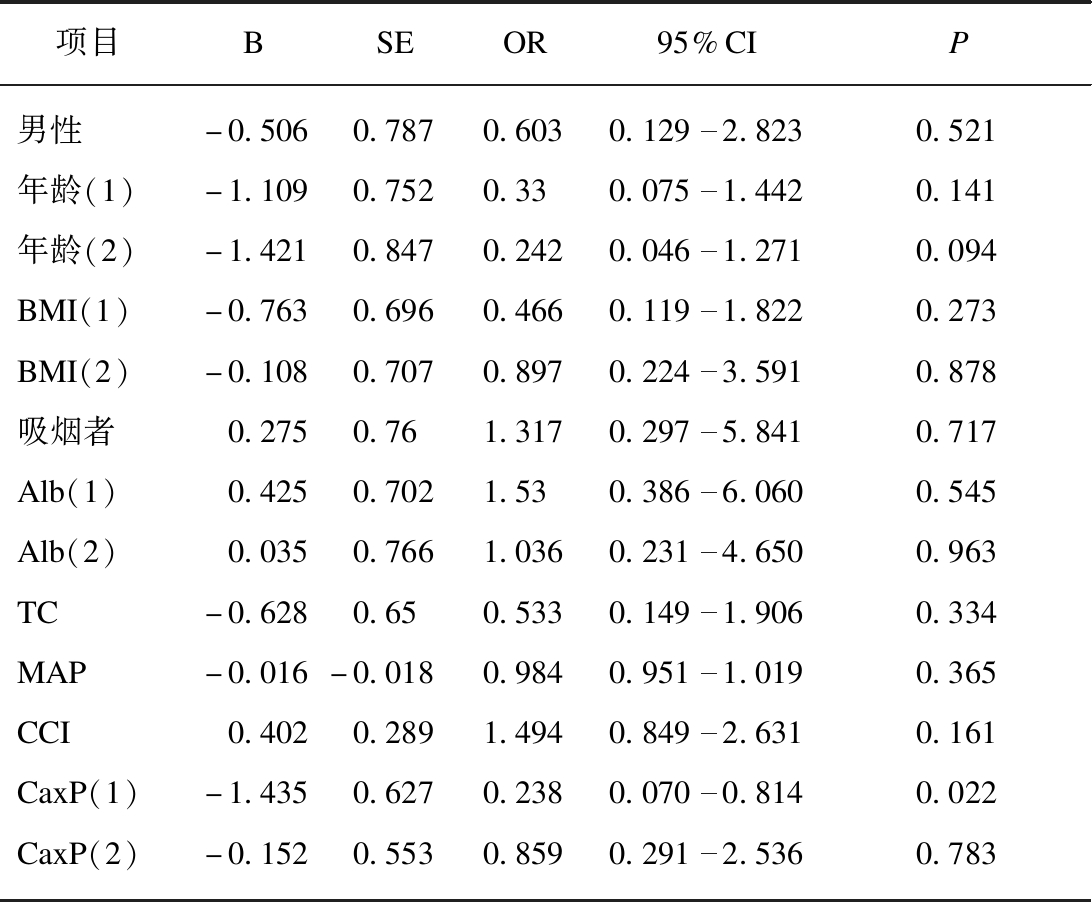
项目BSEOR95%CIP男性-0.5060.7870.6030.1292.8230.521年龄(1)-1.1090.7520.330.0751.4420.141年龄(2)-1.4210.8470.2420.0461.2710.094BMI(1)-0.7630.6960.4660.1191.8220.273BMI(2)-0.1080.7070.8970.2243.5910.878吸烟者0.2750.761.3170.2975.8410.717Alb(1)0.4250.7021.530.3866.0600.545Alb(2)0.0350.7661.0360.2314.6500.963TC-0.6280.650.5330.1491.9060.334MAP-0.016-0.0180.9840.9511.0190.365CCI0.4020.2891.4940.8492.6310.161CaxP(1)-1.4350.6270.2380.0700.8140.022CaxP(2)-0.1520.5530.8590.2912.5360.783
年龄(1):60~75岁;年龄(2):>75岁;BMI(1):体重指数中三分位;BMI(2):体重指数低三分位;Alb(1):血清白蛋白25~30g/L;Alb(2):血清白蛋白<25g/L;TC:总胆固醇;CaxP(1):钙磷乘积中三分位;CaxP(2):钙磷乘积低三分位
2.4 全因死亡风险影响因素分析
以基线性别、年龄、吸烟、文化程度、CCI、eGFR、MAP、血清Alb、BMI、钙磷乘积、TLC作为协变量,采用Cox比例风险回归模型分析CAPD患者生存时间影响因素。数据显示,年龄、血清Alb和TLC是死亡风险的预测因子,见表2。与<60岁的CAPD患者比较,年龄60~75岁和年龄>75岁的患者死亡风险分别是2.176倍和3.584倍。与血清Alb>30g/L 的CAPD患者比较,血清Alb为25~30g/L和<25g/L患者的死亡风险分别是1.753倍和2.075倍。与低三分位TLC比较,中三分位TLC的患者死亡风险减少50.8%,见表3。
表3 CAPD患者全因死亡率的Cox回归分析
Tab.3 Cox regression analysis of all-cause mortality in CAPD patients

项目BSEWaldHR95%CIP年龄(1)0.7770.2986.8092.1761.2133.9020.009年龄(2)1.2710.31716.0503.5841.9146.6360Alb(1)0.5610.2823.9611.7531.0093.0460.047Alb(2)0.7300.3135.4562.0751.1253.8290.02TLC(1)-0.7100.2925.7990.4920.2760.8760.016TLC(2)-0.5330.2833.5440.5870.3371.0220.06
协变量为性别、年龄、吸烟、GFR、文化程度、合并症指数、平均动脉压、血清白蛋白、体重指数、钙磷乘积、总淋巴细胞计数。年龄(1):60~75岁;年龄(2):>75岁。Alb(1):为血清白蛋白25~30g/L;Alb(2):血清白蛋白<25g/L。TLC(1):T2总淋巴细胞计数(1.10~1.50)×109/L;TLC(2):T3总淋巴细胞计数(1.60~2.70)×109/L
3 讨 论
腹膜透析是利用人体腹膜作为半透膜,借助腹膜两侧毛细血管内血浆与透析液中溶质的浓度梯度,达到超滤水分、清除毒素、纠正酸中毒和电解质紊乱的目的。据美国肾脏病数据系统2015发布的年度报告显示[2],腹膜透析患者的死亡率逐年下降,一项起自2008年的5年随访研究报道,腹膜透析3年生存率66.4%,5年生存率50.3%。本研究结果显示,CAPD患者3年和5年生存率分别为71.2%和53.7%,略高于美国同期报道结果,可能与近年来腹膜透析技术逐渐成熟有关。众多研究资料显示,年龄是CAPD患者死亡率的独立影响因素,高龄患者腹膜透析死亡风险增加[3]。本研究结果与之一致,60岁以上比60岁以下患者死亡风险明显增加。其主要原因可能与高龄患者合并症增加,器官系统老化,对炎症、氧化应激和营养不良的代偿修复能力减退有关。
心血管并发症是长期透析患者的主要死亡原因[4],而且这种心血管并发症无法用传统的危险因素来解释。目前,钙磷代谢紊乱被认为是ESRD患者心血管事件的主要原因。众多的研究显示,高磷血症、高钙磷乘积可引起转移性钙化,使透析患者心血管事件风险增加[5]。本研究显示,本组患者的死亡原因中,心脑血管死因占53.2%。校正多种混杂因素后,血清钙磷乘积是心脑血管死亡的独立影响因素。与高三分位血清钙磷乘积比较,中三分位血清钙磷乘积可减少死亡风险(OR=0.238),而低三分位钙磷乘积未显示出优势。可能由于本组患者腹膜透析期间使用的是低钙透析液,在一定程度上缓和了基线高钙磷乘积带来的风险。而且,ESRD患者血清钙磷水平并不是越低越好,对于ESRD患者不仅要重视高磷血症、高钙磷乘积,也要关注低钙、低磷水平的患者,积极处理钙磷代谢紊乱,将血清钙磷水平控制在合理范围是降低心脑血管死亡率的有效措施。
CAPD通过增加透析液交换次数或灌注量增加小分子溶质的清除,通过加大透析液的浓度增加水分超滤,由于腹膜透析液留置时间长,可较好改善中分子物质的清除。但与此同时,伴随着透析超滤过程不可避免会导致某些氨基酸、小分子肽和部分蛋白质的丢失。腹膜透析患者每天约有5~15g的蛋白质经腹膜透析液丢失[6-7]。有研究显示,CAPD患者80%~85%存在着不同程度的蛋白质-能量消耗[8]。本组患者透析前基线血清Alb水平偏低,严重低蛋白血症(Alb<25g/L)的发生率达28.4%。这一方面与ESRD引起的摄入减少、微炎症状态、代谢紊乱以及蛋白质合成减少有关;另一方面与本组患者年龄偏高以及使用溴甲酚紫比色法检测有关[9]。已有研究发现,低白蛋白血症是腹膜透析死亡率的独立预测因子[10-11]。本研究显示腹膜透析前基线低血清Alb水平是CAPD患者死亡率的独立预测因子,Alb<25g/L的患者死亡风险明显增加(HR=2.075)。可见,无论透析前后,均应重视蛋白质营养不良的干预。
随着ESRD病程的进展免疫系统也在发生复杂的改变。研究显示,慢性肾病患者外周TLC和淋巴细胞分型与CKD分期密切相关,随着肾功能下降,B细胞和CD3T细胞降低,NK细胞百分比升高[12-14]。一方面,由于尿毒症毒素、氧化应激、容量负荷等诱发肾脏清除率降低和/或炎细胞因子产生增加;另一方面,尿毒症毒素蓄积影响免疫感受细胞,引起免疫抑制,导致免疫激活与抑制并存[15-16]。因此,ESRD患者不仅感染高发,并且免疫激活可能导致心血管系统的炎症,增加心血管疾病发生发展的风险[17-18]。本研究显示,透析前基线低TLC是CAPD患者死亡的独立预测因子,中三分位TLC比低三分位死亡风险减少50.8%。目前认为尿毒症通过改变共刺激分子(CD80、CD86)来降低树突状细胞和巨噬细胞的抗原提呈能力[19]。在腹膜透析患者中发现的Th淋巴细胞成熟受损也会导致免疫反应和感染易感性的缺陷[20]。此外,ESRD免疫功能改变的另一个重要原因,可能与PEW的存在有关,PEW与淋巴细胞减少和T淋巴细胞功能受损有关[21]。
本研究不足之处:(1) 研究为单中心前瞻性队列研究,纳入病例为透析后定期门诊随访3个月以上的患者,总病例数不够多;(2) 透析前基线状态的生化指标可能受合并症以及临床药物治疗的影响;(3) 有 部分CAPD患者因各种原因放弃治疗,无法获得确切的生存时间和死亡原因,影响数据分析的完整性。
总之,CAPD患者的生存率受多种因素影响,透析前基线高龄、低血清Alb和TLC是CAPD患者全因死亡风险的预测因子。心脑血管事件是CAPD患者的主要死亡原因,而血清钙磷乘积是心脑血管死因的独立影响因素。因此,应加强ESRD患者蛋白质营养评价和免疫监测,维持合理的血清钙磷水平,早期采取适当的干预措施可能是降低透析患者死亡率的重要措施。
[1] 倪兆慧,金海姣.中国腹膜透析发展70年[J].中国血液净化,2019,18(10):661-663.
[2] The United States Renal Data System(USRDS) 2015 annual data report.[R/OL].[2020-03-02].http:∥www.usrds.org.
[3] ABE M,HAMANO T,HOSHINO J,et al.Predictors of outcomes in patients on peritoneal dialysis:a 2-year nationwide cohort study[J].Sci Rep,2019,9(1):3967.
[4] SUSANTITAPHONG P,ALTAMIMI S,ASHKAR M,et al.GFR at initiation of dialysis and mortality in CKD:a meta-analysis[J].Am J Kidney Dis,2012,59(6):829-840.
[5] SARNAK M J.Cardiovascular complications in chronic kidney disease[J].Am J Kidney Dis,2003,41(5 Suppl):11-17.
[6] DULANEY J T,HATCH F E.Peritoneal dialysis and loss of proteins:a review[J].Kidney Int,1984,26(3):253-262.
[7] CHUNG S H,CARRERO J J,LINDHOLM B.Causes of poor appetite in patients on peritoneal dialysis[J].J Ren Nutr,2011,21(1):12-15.
[8] KRISHNAMOORTHY V,SUNDER S,MAHAPATRA H S,et al.Evaluation of protein-energy wasting and inflammation on patients undergoing continuous ambulatory peritoneal dialysis and its correlations[J].Nephrourol Mon,2015,7(6):e33143.
[9] 黄小华,方照舟,黄益楚,等.溴甲酚绿与溴甲酚紫法测定白蛋白的差异比较[J].检验医学,2013,28(1):88-89.
[10] NDLOVU K C Z,CHIKOBVU P,MOFOKENG T,et al.Serum albumin and mortality in patients with HIV and end-stage renal failure on peritoneal dialysis[J].PLoS One,2019,14(6):e0218156.
[11] SINGH T,ASTOR B C,WAHEED S.End-stage renal disease patients with low serum albumin:is peritoneal dialysis an option?[J].Perit Dial Int,2019,39(6):562-567.
[12] KIM S M,KIM H W.Relative lymphocyte count as a marker of progression of chronic kidney disease[J].Int Urol Nephrol,2014,46(7):1395-1401.
[13] TIAN N,PENMAN A D,MANNING R D,et al.Association between circulating specific leukocyte types and incident chronic kidney disease:the Atherosclerosis Risk in Communities (ARIC) study[J].J Am Soc Hypertens,2012,6(2):100-108.
[14] LITJENS N H R,VAN DRUNINGEN C J,BETJES M G H.Progressive loss of renal function is associated with activation and depletion of naive T lymphocytes[J].Clin Immunol,2006,118(1):83-91.
[15] KIMMEL P L,PHILLIPS T M,SIMMENS S J,et al.Immunologic function and survival in hemodialysis patients[J].Kidney Int,1998,54(1):236-244.
[16] STENVINKEL P,KETTELER M,JOHNSON R J,et al.IL-10,IL-6,and TNF-alpha:central factors in the altered cytokine network of uremia:the good,the bad,and the ugly[J].Kidney Int,2005,67(4):1216-1233.
[17] JEGATHEESAN D,CHO Y,JOHNSON D W.Clinical studies of interventions to mitigate cardiovascular risk in peritoneal dialysis patients[J].Semin Nephrol,2018,38(3):277-290.
[18] CAI K D,LUO Q,ZHU B X,et al.Neutrophil-lymphocyte ratio is associated with arterial stiffness in patients with peritoneal dialysis[J].BMC Nephrol,2016,17(1):191.
[19] GIRNDT M,SESTER M,SESTER U,et al.Defective expression of B7-2(CD86) on monocytes of dialysis patients correlates to the uremia-associated immunedefect[J].Kidney Int,2001,59(4):1382-1389.
[20] ANDO M,SHIBUYA A,YASUDA M,et al.Impairment of innate cellular response toin vitro stimuli in patients on continuous ambulatory peritoneal dialysis[J].Nephrol Dial Transplant,2005,20(11):2497-2503.
[21] FOUQUE D,KALANTAR-ZADEH K,KOPPLE J,et al.A proposed nomenclature and diagnostic criteria for protein-energy wasting in acute and chronic kidney disease[J].Kidney Int,2008,73(4):391-398.