伴随手术技术和人工晶状体的发展,白内障手术步入屈光手术时代。与正视眼相比,高度近视白内障术后前囊口更容易发生收缩,易引起IOL(intraocularlens, IOL)有效位置的改变[1]。另外,高度近视是晚期囊袋内IOL脱位的最常见的危险因素,发生率为7.7%~40%[2-4],这大大降低了术后屈光度的预测准确性。近年来,飞秒激光作为辅助技术手段逐步应用于白内障手术中。飞秒激光对前囊口的精确把控,使其可在屈光性白内障手术中获得潜在的临床优势[5-6]。然而,目前尚无关于高度近视白内障患者在飞秒激光辅助白内障术后囊袋及IOL稳定性的研究。本研究通过比较高度近视患者在飞秒激光辅助白内障和传统超声乳化白内障吸除术后不同时间段晶状体前囊口直径及IOL囊袋内稳定性的差异,为飞秒激光辅助白内障手术在高度近视患者中应用提供临床参考。
1 资料与方法
1.1 一般资料
收集2019年7月—10月上海新视界眼科医院收治的高度近视合并白内障患者。纳入标准: (1) 眼 轴长度≥26mm,屈光度≥-6.00D;(2) 无糖尿病、严重心、肺、肾、肝脏等基础疾病;(3) 选择同一IOL(Rayner920H)植入的患者。排除标准: (1) 随访期内行Nd: YAG激光囊膜切开术;(2) 术中或随访期发生并发症者,如晶状体脱位、后囊膜破裂、眼内炎、迟发性葡萄膜炎等;(3) 合并如角膜病、青光眼、葡萄膜炎、假性囊膜剥脱综合征、视网膜色素变性以及视神经疾病等;(4) 眼外伤及眼手术史;(5) 晶状体脱位及悬韧带异常(虹膜震颤、前房深);(6) 严重眼底病患者,如视网膜出血、脱离及裂孔等;(7) 术后无法按期随访者。本研究共纳入39例60眼。按患者手术意愿分组,行飞秒激光辅助白内障手术为飞秒组,男7例12眼,女9例14眼,年龄44~77岁,平均(61.69±9.62)岁,平均眼轴(28.31±1.43) mm;行传统白内障超声乳化吸除术为对照组,男9例15眼,女14例19眼,年龄40~72岁,平均(61.79±7.17)岁,平均眼轴(28.37±1.72) mm。两组年龄、性别构成比、眼轴比较差异无统计学意义(P>0.05)。
1.2 手术方法
所有手术均由同一位经验丰富的眼科医生进行。术前3d局部应用非甾体抗炎药物。术前1h充分散瞳,飞秒组应用LenSX飞秒激光系统(Alcon公司,美国)完成截囊及预劈核操作。截囊直径5.5mm,输出能量5~6μJ,预劈核直径范围5mm,输出能量10μJ。10:30点位做2.8mm透明角膜切口,3:00点位做角膜缘侧切口(1mm)。撕囊镊游离并取出前囊膜片,使用Infiniti超声乳化仪(Alcon公司,美国)乳化晶体核并注吸皮质,I/A注吸手柄行后囊膜抛光。对照组做相同主侧切口,撕囊镊连续环形撕囊,撕囊直径约5.5mm,行超声乳化白内障吸除。两组均于囊袋内植入同型亲水丙烯酸IOL(Rayner920H,英国),水密切口。术后前2周局部应用左氧氟沙星滴眼液,3次/d,妥布霉素地塞米松眼膏,每晚1次。妥布霉素地塞米松滴眼液,术后第1周4次/d,术后第2周改为2次/d后停用。术后第3~4周普拉洛芬滴眼液滴术眼,4次/d。如有干眼症状,加用玻璃酸钠滴眼液。
1.3 观测指标
术后1周,1、3个月随访。充分散瞳后由同一位眼科医师使用Pentacam三维眼前节成像系统进行检查,按照文献[7]描述的方法测量,见图1。测量参数包括前囊口水平及垂直方向直径、人工晶状体倾斜角和偏心量、术后前房深度。取90°和180°方向的Scheimpflug图像,应用Image Pro Plus软件得到IOL前、后表面的最佳拟合曲线,以此确定IOL光学部中心轴。以散瞳后的瞳孔轴线为基线,IOL中心轴与基线相交的夹角即倾斜角,IOL光学区中心点距瞳孔轴垂直距离即偏心量。两侧前囊膜前缘连线即前囊口直径。上述指标均测量3次,取平均值。术后前房深度指角膜后顶点到IOL前表面的距离,系统可以直接读取。
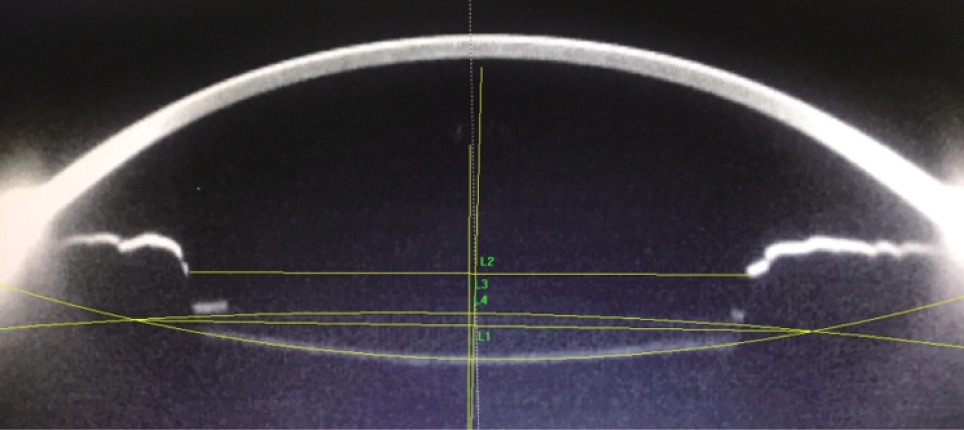
图1 充分散瞳后的Scheimpflug图像
Fig.1 The Scheimpflug image after mydriasis L1为IOL平面,即IOL前后表面拟合曲线交点连线,L2为L1中点垂直线,即IOL中心轴;L3为瞳孔平面,L4为L3中点垂直线,即瞳孔中心轴;L2与L4的角度即IOL倾斜角,L1中点到瞳孔中心轴垂直距离即IOL偏心量
1.4 统计学处理
应用SPSS 22.0软件统计分析,计量资料经K-S正态性检验,以![]() 表示。术后不同时点计数资料采用重复测量方差分析。组间不同时间点计数资料采用t检验。分类变量资料比较采用χ2检验。非正态分布资料组间比较采用Mann-Whitney U检验,P<0.05为差异有统计学意义。
表示。术后不同时点计数资料采用重复测量方差分析。组间不同时间点计数资料采用t检验。分类变量资料比较采用χ2检验。非正态分布资料组间比较采用Mann-Whitney U检验,P<0.05为差异有统计学意义。
2 结 果
本项前瞻性研究共纳入39例60眼,无失访及行Nd: YAG激光囊膜切开术病例。术中IOL放置位置分别为垂直位(飞秒组17眼,对照组23眼)、倾斜位(飞秒组9眼,对照组11眼),经χ2检验两组差异无统计学意义(P=0.854)。
2.1 两组术后不同时间段各指标比较
对术后各指标进行重复测量方差分析,处理因素统计量差异见表1,若处理因素与时间因素有交互作用,对两组同一时间数据作简单效应检验。两组术后前囊口垂直直径差异有统计学意义,水平直径处理因素与时间存在交互作用(P=0.01)。两组前囊口垂直直径、水平直径随时间缩短,术后1周和1个月飞秒组前囊口水平、垂直直径显著低于对照组(1周P=0.012,0.011,1个月P=0.030,0.032)。水平偏心量处理因素与时间有交互效应(P<0.001)。术后1周、1、3个月飞秒组水平偏心量明显低于对照组(P=0.029,0.002,<0.001)。重复测量方差分析显示两组IOL垂直偏心量差异无统计学意义。IOL水平和垂直倾斜角,处理因素与时间具有交互效应(P均<0.001)。术后1、3个月飞秒组水平倾斜角明显低于对照组(P=0.008,0.006),垂直倾斜角差异均无统计学意义(P>0.05)。术后偏心量及倾斜角均随时间增加(P<0.01)。两组术后前房深度加深(P<0.01),组间前房深度差异无统计学意义,见表1。
2.2 术后各指标变化程度比较
变化量为术后3个月随访指标与术后1周随访时的差值。飞秒组前囊口水平直径变化量低于对照组(0.10±0.04,0.14±0.06,P=0.009),垂直直径变化量差异无统计学意义(0.11±0.05,0.14±0.06,P=0.058)。飞秒组水平偏心变化量低于对照组(0.11±0.02,0.16±0.03,P<0.01),垂直偏心变化量差异无统计学意义(0.03±0.03,0.03±0.25,P=0.961)。飞秒组水平倾斜角变化量低于对照组(0.36±0.07,0.44±0.10,P<0.01),垂直倾斜角变化量低于对照组(0.16±0.08,0.23±0.06,P=0.01)。飞秒组前房深度变化量显著低于对照组(0.16±0.13,0.21±0.14,P=0.046)。
表1 两组术后不同时间段各指标比较
Tab.1 Comparison of postoperative parameters in different time between two groups![]()
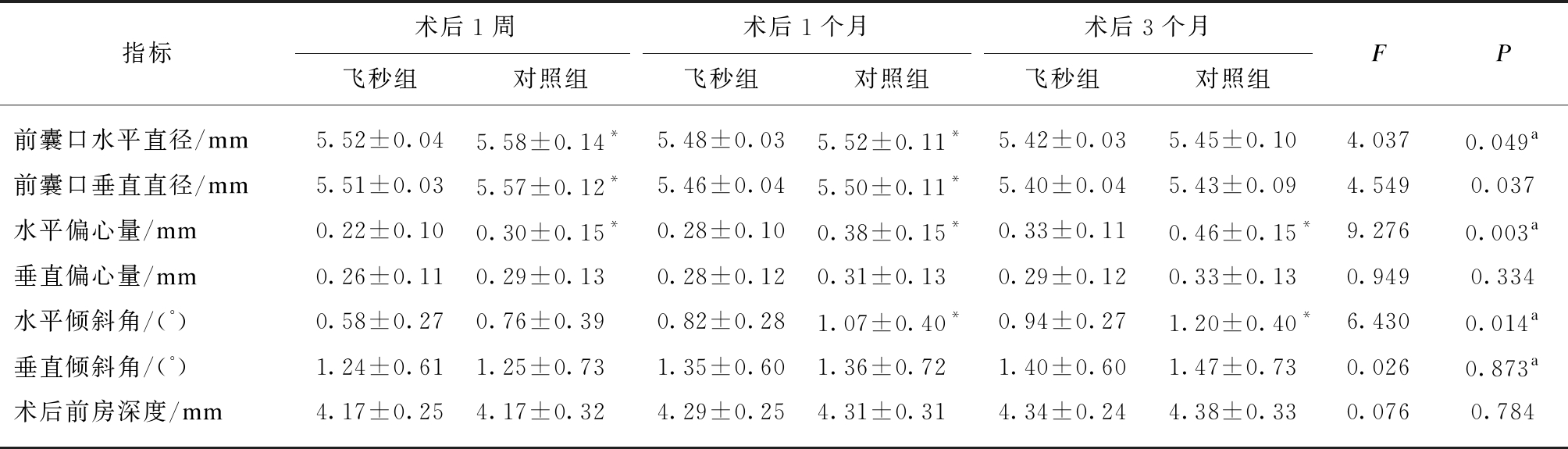
指标术后1周术后1个月术后3个月飞秒组对照组飞秒组对照组飞秒组对照组FP前囊口水平直径/mm5.52±0.045.58±0.14*5.48±0.035.52±0.11*5.42±0.035.45±0.104.0370.049a前囊口垂直直径/mm5.51±0.035.57±0.12*5.46±0.045.50±0.11*5.40±0.045.43±0.094.5490.037水平偏心量/mm0.22±0.100.30±0.15*0.28±0.100.38±0.15*0.33±0.110.46±0.15*9.2760.003a垂直偏心量/mm0.26±0.110.29±0.130.28±0.120.31±0.130.29±0.120.33±0.130.9490.334水平倾斜角/(°)0.58±0.270.76±0.390.82±0.281.07±0.40*0.94±0.271.20±0.40*6.4300.014a垂直倾斜角/(°)1.24±0.611.25±0.731.35±0.601.36±0.721.40±0.601.47±0.730.0260.873a术后前房深度/mm4.17±0.254.17±0.324.29±0.254.31±0.314.34±0.244.38±0.330.0760.784
组间重复测量方差分析,F、P值为处理因素主效应统计值及显著性,a示处理因素*时间P<0.05,有交互作用;同一时间组间比较,*P<0.05
3 讨 论
IOL在囊袋内位置改变会影响患者术后屈光状态或引入高阶像差,从而影响患者术后视觉功能[8-9]。因此,维持IOL在囊袋内的稳定性十分重要。白内障术后IOL稳定性主要与IOL的材料及设计、悬韧带张力、前囊口的大小与完整性、葡萄膜炎、视网膜色素变性及高度近视等因素相关[3,10]。高度近视,尤其是眼轴>26mm者晶状体囊袋大、悬韧带松弛,白内障术后前囊收缩、IOL倾斜和偏心的频率明显高于正常眼[1,11]。传统白内障手术中连续环形撕囊(continuous curvilinear capsulorhexis, CCC)若不规则、偏心,易引起前囊口不平衡收缩[12]。飞秒激光作为白内障手术中新的辅助技术,能在前节OCT引导下完成关键步骤,包括截囊、预劈核及制作透明角膜切口等。既往研究报道在正视眼患者中,飞秒激光通过精确控制前囊口的形状、大小和中心,有效减少IOL偏心[5-6,13]。而在高度近视中,尚无飞秒激光白内障术后囊袋及IOL稳定性的研究。本研究采用连续前瞻性队列研究,与传统白内障手术进行比较,旨在探究飞秒激光辅助白内障手术对前囊口收缩程度,以及IOL偏心、倾斜及有效位置的影响。
本研究通过测量Scheimpflug图像的前囊口垂直、水平直径及变化量来描述前囊口形态的改变。本研究数据表明,高度近视白内障术后前囊口收缩逐渐进展,对照组前囊口缩窄程度显著高于飞秒组。据报道眼内炎性环境如葡萄膜炎、高度近视等前囊收缩更明显[11,14]。飞秒激光预处理后前房炎症因子水平增高,而由于术中超声能量使用减少,术后前房炎症反应与传统白内障手术相似或减轻[15-16]。本研究尚未观察到术后发生葡萄膜炎的病例。白内障术后前囊收缩与残留的晶状体上皮细胞(lens epithelial cells, LECs)及其纤维化有关[11]。王志亮等[17]发现术中有效清除LECs后,前囊收缩明显减少。目前有多项研究发现,飞秒激光能诱导LECs凋亡且抑制其纤维化[18-19]。猜测激光处理后,LECs残留较少可能是飞秒组前囊口收缩程度小的原因之一。
考虑到高度近视人群囊袋较大,本研究采用总长12.5mm,光学区直径为6.25mm的Rayner920H。它具有两个较为宽大的C型襻,能提供较好的水平支撑;其次,IOL展开缓慢,可防止襻展开过快引起的囊袋损坏[20-21]。术中植入同一IOL,排除IOL材质及设计对结果的影响。本研究通过测量IOL的偏心量、倾斜角及术后前房深度来反映IOL-囊袋的稳定性。本研究发现高度近视白内障术后IOL偏心、倾斜均呈现增加趋势。飞秒组各时间段IOL水平偏心量及变化量低于对照组,术后1个月开始水平倾斜角明显低于对照组,倾斜角的变化较对照组稳定。有研究[22]通过比较囊袋的最大拉伸力,发现飞秒激光制作的前囊口边缘强度一致,其抵抗断裂和过度变形的能力均优于CCC。而CCC的囊口欠规则,由于前囊边缘所受收缩力不均衡,IOL在囊袋内的位置可能受到影响[6]。以上结果表明飞秒激光制作的前囊口可能有益于维持IOL的稳定性。除此之外IOL襻在囊袋内的方向可能也会影响其稳定性[12]。Zhu等[23]发现双襻IOL在大囊袋内受重力作用可能轻微下沉,而垂直放置的IOL由于襻的支撑,下沉变化较水平放置少。本研究中,IOL在垂直方向上的偏心、倾斜变化更稳定,结合术中IOL襻多位于垂直位,推测这可能由于IOL襻在垂直方向提供了更多的支撑作用。术后前房深度的变化反映了IOL有效位置的改变,术后1周到3个月IOL轻度后移,这与高度近视白内障术后常出现远视漂移相一致[24]。在悬韧带功能薄弱的情况下,囊膜收缩对襻的挤压易引起IOL的轴向运动[25]。与CCC相比,飞秒激光截囊不依赖于悬韧带的支撑[26]。因此飞秒组前房深度变化程度低可能与术中悬韧带损伤风险更小有关。至于飞秒激光对悬韧带及屈光状态的影响还需进一步的观察。
结果表明,在高度近视人群中,飞秒激光白内障手术减少前囊膜收缩程度,增强IOL在囊袋内的稳定性,这与既往正视眼中的研究结果一致。随着多功能IOL的发展及应用,飞秒激光白内障手术联合多功能IOL的植入可能会为患者带来更满意的视觉质量。本研究亦存在一定局限性。首先,Scheimpflug图像需要使用图像处理软件,人为因素较多。然而,通过同一人操作并测量3次取平均值可在一定程度上弥补缺陷。其次,本研究为连续前瞻性、非随机队列研究,由于手术费用相差较大,随机分组在临床工作中难以展开,研究结果可能受患者经济水平、心理因素等影响。研究中样本数量较小,未来研究还需进一步扩大样本量。
[1] 王丹丹,郑宇曦,俞晓宇,等.超高度近视眼白内障超声乳化术后囊袋变化及人工晶状体稳定性研究[J].浙江医学,2016,38(17): 1397-1400.
[2] SUBASI S, YUKSEL N, KARABAS V L, et al. Late in-the-bag spontaneous IOL dislocation: risk factors and surgical outcomes[J]. Int J Ophthalmol, 2019,12(6): 954-960.
[3] FERN NDEZ-BUENAGA R, ALIO J L, PÉREZ-ARDOY A L, et al. Late in-the-bag intraocular lens dislocation requiring explantation: risk factors and outcomes[J]. Eye (Lond), 2013,27(7): 795-801.
NDEZ-BUENAGA R, ALIO J L, PÉREZ-ARDOY A L, et al. Late in-the-bag intraocular lens dislocation requiring explantation: risk factors and outcomes[J]. Eye (Lond), 2013,27(7): 795-801.
[4] REY A, JÜRGENS I, DYRDA A, et al. Surgical outcome of late in-the-bag intraocular lens dislocation treated with pars Plana vitrectomy[J]. Retina, 2016,36(3): 576-581.
[5] NAGY Z Z, KR NITZ K, TAKACS A I, et al. Comparison of intraocular lens decentration parameters after femtosecond and manual capsulotomies[J]. J Refract Surg, 2011,27(8): 564-569.
NITZ K, TAKACS A I, et al. Comparison of intraocular lens decentration parameters after femtosecond and manual capsulotomies[J]. J Refract Surg, 2011,27(8): 564-569.
[6] KR NITZ K, MIH
NITZ K, MIH LTZ K, S
LTZ K, S NDOR G L, et al. Intraocular lens tilt and decentration measured by scheimpflug camera following manual or femtosecond laser-created continuous circular capsulotomy[J]. J Refract Surg, 2012,28(4): 259-263.
NDOR G L, et al. Intraocular lens tilt and decentration measured by scheimpflug camera following manual or femtosecond laser-created continuous circular capsulotomy[J]. J Refract Surg, 2012,28(4): 259-263.
[7] DE CASTRO A, ROSALES P, MARCOS S. Tilt and decentration of intraocular lenses in vivo from Purkinje and Scheimpflug imaging. Validation study[J]. J Cataract Refract Surg, 2007,33(3): 418-429.
[8] TAKETANI F, MATUURA T, YUKAWA E, et al. Influence of intraocular lens tilt and decentration on wavefront aberrations[J]. J Cataract Refract Surg, 2004,30(10): 2158-2162.
[9] TAKETANI F, YUKAWA E, UEDA T, et al. Effect of tilt of 2 acrylic intraocular lenses on high-order aberrations[J]. J Cataract Refract Surg, 2005,31(6): 1182-1186.
[10] 王于蓝,王敏,高峰,等.超高度近视白内障不同撕囊口直径下术后人工晶状体稳定性观察[J].国际眼科杂志,2015,15(1): 76-78.
[11] ZHU X J, CHEN M J, ZHANG K K, et al. Elevated TGF-β2 level in aqueous humor of cataract patients with high myopia: potential risk factor for capsule contraction syndrome[J]. J Cataract Refract Surg, 2016,42(2): 232-238.
[12] SHAH G D, PRAVEEN M R, VASAVADA A R, et al. Rotational stability of a toric intraocular lens: influence of axial length and alignment in the capsular bag[J]. J Cataract Refract Surg, 2012,38(1): 54-59.
[13] ABOUZEID H, FERRINI W. Femtosecond-laser assisted cataract surgery: a review[J]. Acta Ophthalmol, 2014,92(7): 597-603.
[14] ELGOHARY M A, MCCLUSKEY P J, TOWLER H M, et al. Outcome of phacoemulsification in patients with uveitis[J]. Br J Ophthalmol, 2007,91(7): 916-921.
[15] FAVUZZA E, BECATTI M, GORI A M, et al. Cytokines, chemokines, and flare in the anterior chamber after femtosecond laser-assisted cataract surgery[J]. J Cataract Refract Surg, 2019,45(7): 910-914.
[16] ABELL R G, ALLEN P L, VOTE B J. Anterior chamber flare after femtosecond laser-assisted cataract surgery[J]. J Cataract Refract Surg, 2013,39(9): 1321-1326.
[17] 王志亮,陈志敏,许衍辉,等.清除LECs对高度近视合并白内障患者囊袋稳定性的影响[J].国际眼科杂志,2020,20(2): 294-296.
[18] SUN W, LIU J, LI J, et al. Human lens epithelial cell apoptosis and epithelial to mesenchymal transition in femtosecond laser-assisted cataract surgery[J]. Int J Ophthalmol, 2018,11(3): 401-407.
[19] PISCIOTTA A, DE MARIA M, VERDINA T, et al. Anterior capsule of the lens: comparison of morphological properties and apoptosis induction following FLACS and standard phacoemulsification surgery[J]. Biomed Res Int, 2018,2018: 7242837.
[20] ZHU X J, HE W W, YANG J, et al. Adhesion of the posterior capsule to different intraocular lenses following cataract surgery[J]. Acta Ophthalmol, 2016,94(1): e16-e25.
[21] 邢晓杰,汤欣,宋慧,等.四种非球面人工晶状体植入术后倾斜和偏心的比较[J].中华眼科杂志,2010,46(4): 332-336.
[22] TAKAGI M, KOJIMA T, ICHIKAWA K, et al. Comparison of maximum stretch forces between femtosecond laser-assisted capsulotomy and continuous curvilinear capsulorhexis[J]. J Ophthalmol, 2017,2017: 3489373.
[23] ZHU X J, HE W W, ZHANG Y L, et al. Inferior decentration of multifocal intraocular lenses in myopic eyes[J]. Am J Ophthalmol, 2018,188: 1-8.
[24] EL-NAFEES R, MOAWAD A, KISHK H, et al. Intra-ocular lens power calculation in patients with high axial myopia before cataract surgery[J]. Saudi J Ophthalmol, 2010,24(3): 77-80.
[25] 竺向佳,常瑞琪,卢奕.不可忽视的高度近视白内障术后屈光误差与屈光漂移[J].中国眼耳鼻喉科杂志,2018,18(2): 130-133.
[26] GREWAL D S, SCHULTZ T, BASTI S, et al. Femtosecond laser-assisted cataract surgery: current status and future directions[J]. Surv Ophthalmol, 2016,61(2): 103-131.