中国农药用量呈逐年上升趋势,近年来其使用量已超过180万吨,居世界首位[1]。继有机氯农药在20世纪80年代初被全面禁止使用以来,有机磷农药(organophosphate pesticides, OPs)就逐渐成为使用最广泛的杀虫剂之一[2]。非职业人群暴露主要通过饮食、呼吸、皮肤接触等多种途径进入人体,且具有一定的生殖毒性、神经毒性等[3-4]。已有研究报道,新生儿羊水、脐带血及胎粪中均检测出OPs,表明OPs可通过胎盘屏障对胎儿产生影响[5-6]。迄今为止,全球已超过500万名婴儿是通过辅助生殖技术(assisted reproductive technology, ART)方式出生,全世界每年大约实施100万例ART手术,年出生婴儿约为20万[7]。因此孕前OPs暴露对ART子代健康的影响亟待重视。本研究对上海ART女性孕前尿液OPs浓度进行检测,分析OPs暴露对出生结局的影响,为孕前保健提供合理依据。
1 资料与方法
1.1 研究对象
本研究依托于一项当前正在进行的辅助生殖技术子代胎源性疾病国家出生队列研究。于2017年7月—2018年12月在上海交通大学医学院附属国际和平妇幼保健院生殖门诊招募采用ART治疗的夫妇作为研究对象。纳入标准: (1) 符合不孕症诊断标准(未避孕未怀孕≥1年),具有行体外受精(in vitro fertilization, IVF);卵胞浆内单精子显微注射(intracytoplasmic sperm injection, ICSI)的指征;(2) 年龄≥18岁;(3) 在当地居住≥5年,且计划在该地长期定居;(4) 准备在本医院进行产前检查并分娩者;(5) 接受供卵或使用复苏卵的患者不纳入研究;(6) 自愿同意参与本课题调查研究,并签署知情同意书。本研究共招募597名女性,其中22名自愿退出,49名未进行尿液农药检测和4名未进行采卵治疗的女性被排除在外。在这522名女性中,有293名女性临床妊娠,目前已有133名女性成功分娩,排除27名双胎儿,最后将106对单胎母婴纳入本次分析。本研究经上海交通大学医学院附属国际和平妇幼保健院伦理委员会审查并批准(GKLW-2016-21)。
1.2 问卷调查
研究对象在调查员的指导下,进行面对面的问卷填写,用时约30min。采用国家出生队列孕前调查问卷,对研究人群的人口学特征、居住环境、既往病史和诊疗史进行调查。出生结局的信息由资料员负责从医疗病案中摘抄记录,包括分娩孕周、新生儿性别、出生体重、出生身长等。
1.3 生物样本采集
采卵前使用无菌聚丙烯杯收集研究对象当日随机尿样约50mL,然后每10mL分装于15mL的聚丙烯存储管,样本分装后做好标签立即置于-80℃冰箱冷冻储存直至进行农药检测。
1.4 样本检测
采用气相色谱-质谱串联法(GC-MS,型号TRACE,美国Thermo公司)检测尿液样本中6种OPs非特异性二烷基磷酸酯(DAP)代谢物浓度。DAP代谢物的检出限(LOD)分别为: 磷酸二甲酯(DMP)0.18μg/L,甲基硫代磷酸酯(DMTP)及二甲基二硫代磷酸酯(DMDTP)0.3μg/L,磷酸二乙酯(DEP)及二乙基硫代磷酸酯(DETP)0.06μg/L,二乙基二硫代磷酸酯(DEDTP)0.09μg/L。低于LOD检测值使用![]() 进行替换[8]。对DMP、DMTP、DEP和DETP浓度进行肌酐校正,然后分别除以各物质的摩尔质量,所得数值相加,即为∑DAP摩尔浓度[9]。由于DMDTP和DEDTP检出率太低,因而未纳入∑DAP的计算。使用肌酐(酶法)测定试剂盒(日本和光纯药工业株式会社)和自动化学分析仪(型号7100,日本Hitachi公司)检测尿肌酐含量。
进行替换[8]。对DMP、DMTP、DEP和DETP浓度进行肌酐校正,然后分别除以各物质的摩尔质量,所得数值相加,即为∑DAP摩尔浓度[9]。由于DMDTP和DEDTP检出率太低,因而未纳入∑DAP的计算。使用肌酐(酶法)测定试剂盒(日本和光纯药工业株式会社)和自动化学分析仪(型号7100,日本Hitachi公司)检测尿肌酐含量。
1.5 统计学方法
应用SPSS 19.0软件进行数据的统计分析。采用![]() 频数、百分比描述研究对象的人口学特征和新生儿出生结局。孕前尿液OPs代谢物水平呈偏态分布,故使用检出率及百分位数进行描述。运用广义线性回归模型分析DAP代谢物水平与出生结局之间的关联。依据既往已发表的文献选择可能是混杂因素的变量,最终将女性年龄、家庭月收入、吸烟情况、男性教育水平、不孕时间、不孕原因、流产史及妊娠期并发症(糖尿病、高血压、贫血)作为协变量纳入回归模型[10-16]。此外,在敏感性分析中,排除早产儿(n=8)后再次分析孕前OPs暴露与子代出生结局的关系,以检测早产儿是否会对结果的可靠性产生影响。P<0.05为差异有统计学意义。
频数、百分比描述研究对象的人口学特征和新生儿出生结局。孕前尿液OPs代谢物水平呈偏态分布,故使用检出率及百分位数进行描述。运用广义线性回归模型分析DAP代谢物水平与出生结局之间的关联。依据既往已发表的文献选择可能是混杂因素的变量,最终将女性年龄、家庭月收入、吸烟情况、男性教育水平、不孕时间、不孕原因、流产史及妊娠期并发症(糖尿病、高血压、贫血)作为协变量纳入回归模型[10-16]。此外,在敏感性分析中,排除早产儿(n=8)后再次分析孕前OPs暴露与子代出生结局的关系,以检测早产儿是否会对结果的可靠性产生影响。P<0.05为差异有统计学意义。
2 结 果
2.1 基本信息
本研究共纳入106对单胎母婴,人口学信息见表1。本部分研究人群(n=106)与总研究人群(N=522)的人口学信息差异无统计学意义(P>0.05)。
新生儿中57.5%为女婴,略多于男婴(42.5%)。婴儿分娩孕周为(39.05±1.72)周,出生体重为(3277.03±469.64) g,出生身长为(49.54±1.99) cm。根据出生体重及出生身长计算得到重量指数(g×100/cm3)为2.68±0.22,见表2。
2.2 孕前尿液DAP代谢物浓度
尿液DAP代谢物检出率和浓度见表3。在DAP的6种尿液代谢产物中,有4种的检出率在85%以上,分别为DMP(91.5%)、DMTP(87.7%)、DEP(91.5%)和DETP(95.3%)。尿肌酐校正后,DAP代谢物DMP、DMTP、DEP、DETP中位数水平分别为16.46、1.76、27.5、2.31μg/g。
表1 研究人群(n=106)与总人群(n=522)的人口学信息
Tab.1 Demographic characteristics of the study group
(n=106) and the eligible participants(n=522)
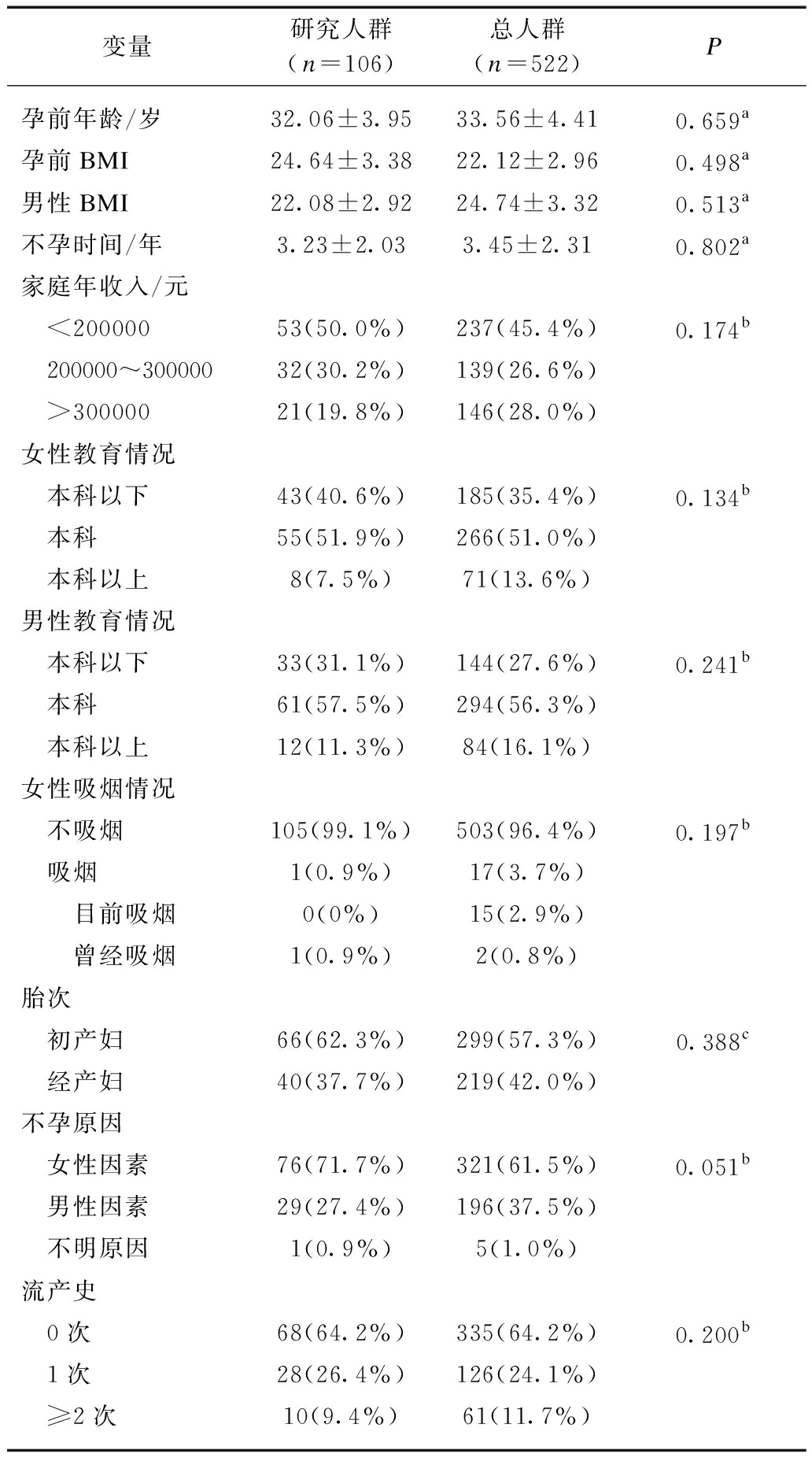
变量研究人群(n=106)总人群(n=522)P孕前年龄/岁32.06±3.9533.56±4.410.659a孕前BMI24.64±3.3822.12±2.960.498a男性BMI22.08±2.9224.74±3.320.513a不孕时间/年3.23±2.033.45±2.310.802a家庭年收入/元 <20000053(50.0%)237(45.4%)0.174b 200000~30000032(30.2%)139(26.6%) >30000021(19.8%)146(28.0%)女性教育情况 本科以下43(40.6%)185(35.4%)0.134b 本科55(51.9%)266(51.0%) 本科以上8(7.5%)71(13.6%)男性教育情况 本科以下33(31.1%)144(27.6%)0.241b 本科61(57.5%)294(56.3%) 本科以上12(11.3%)84(16.1%)女性吸烟情况 不吸烟105(99.1%)503(96.4%)0.197b 吸烟1(0.9%)17(3.7%) 目前吸烟0(0%)15(2.9%) 曾经吸烟1(0.9%)2(0.8%)胎次 初产妇66(62.3%)299(57.3%)0.388c 经产妇40(37.7%)219(42.0%)不孕原因 女性因素76(71.7%)321(61.5%)0.051b 男性因素29(27.4%)196(37.5%) 不明原因1(0.9%)5(1.0%)流产史 0次68(64.2%)335(64.2%)0.200b 1次28(26.4%)126(24.1%) ≥2次10(9.4%)61(11.7%)
a采用独立样本t检验;b采用非参数检验;c采用χ2检验
表2 妊娠期并发症和新生儿的出生结局
Tab.2 Pregnant complications and birth characteristics (n=106)

变量数值妊娠期糖尿病 否89(84.0%) 是16.0(16.0%)妊娠期高血压 否102(96.2%) 是4(3.8%)
续表
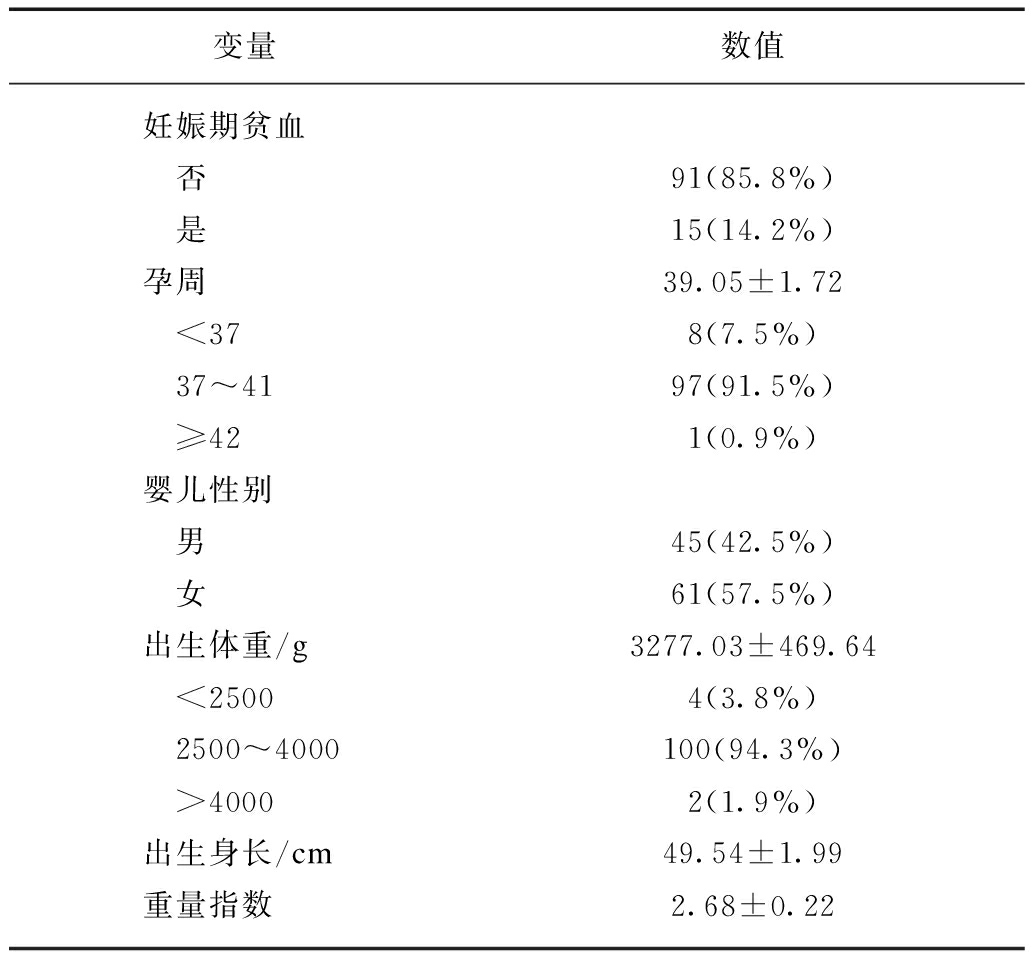
变量数值妊娠期贫血 否91(85.8%) 是15(14.2%)孕周39.05±1.72 <378(7.5%) 37~4197(91.5%) ≥421(0.9%)婴儿性别 男45(42.5%) 女61(57.5%)出生体重/g3277.03±469.64 <25004(3.8%) 2500~4000100(94.3%) >40002(1.9%)出生身长/cm49.54±1.99重量指数2.68±0.22
2.3 孕前DAP浓度与出生结局之间的关联
运用回归模型,调整混杂因素后,孕前尿液DETP浓度与新生儿分娩孕周呈负相关。与最低四分位组(Q1)相比,最高四分位组(Q4)新生儿分娩孕周减少1.34周(95%CI: -2.24~-0.45),见表4。当排除对出生结局有影响的早产儿(n=8)后,结果未发生明显改变,见表5。
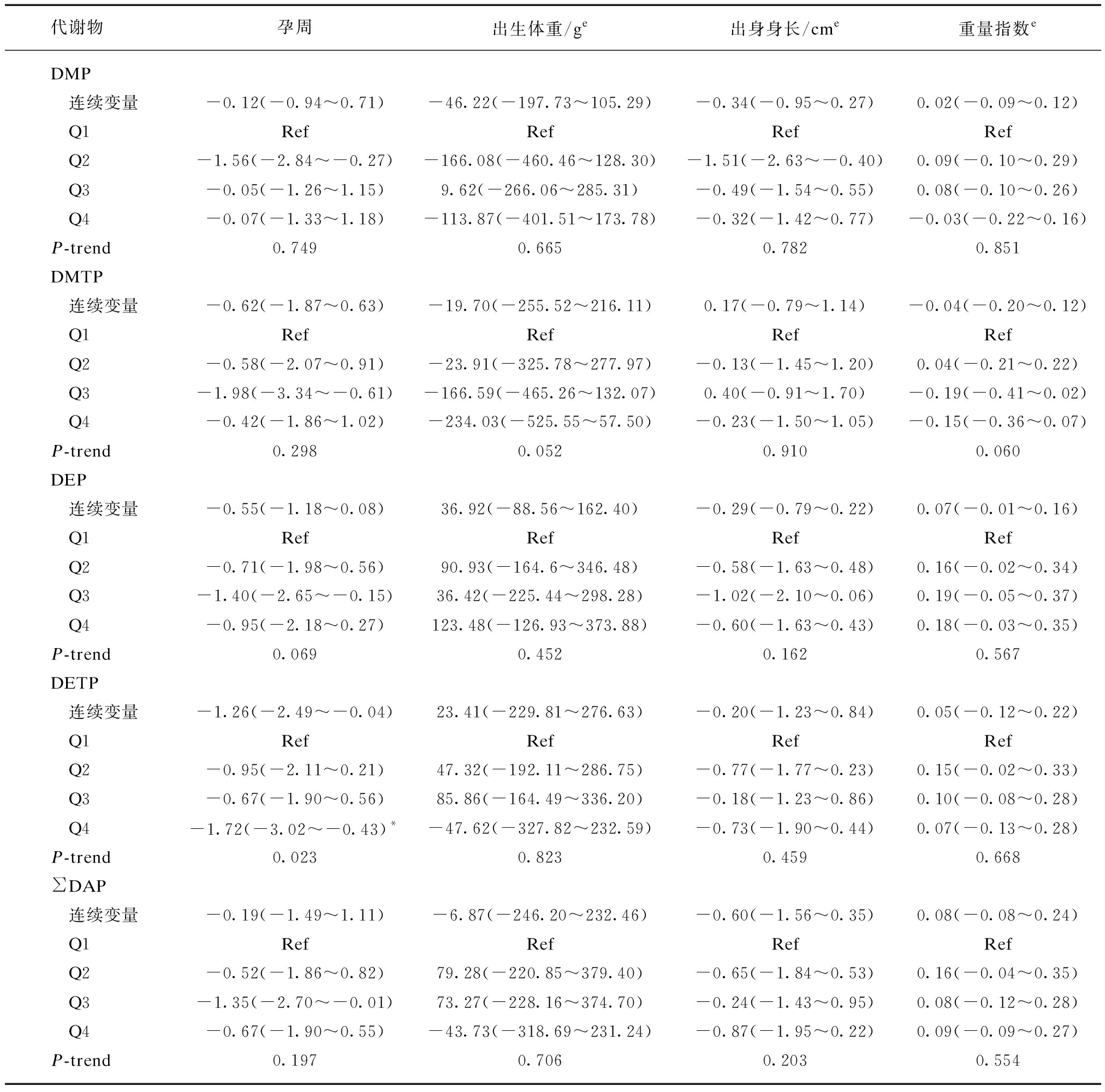
性别分层分析显示: 在男婴中,孕前尿液DETP水平与孕周呈负相关(β=-1.72,95%CI: -3.02~-0.43),见表6。但在女婴中未发现此关联(P>0.05)。
表3 女性孕前尿液中DAP代谢物水平
Tab.3 Urinary concentrations of DAP metabolites
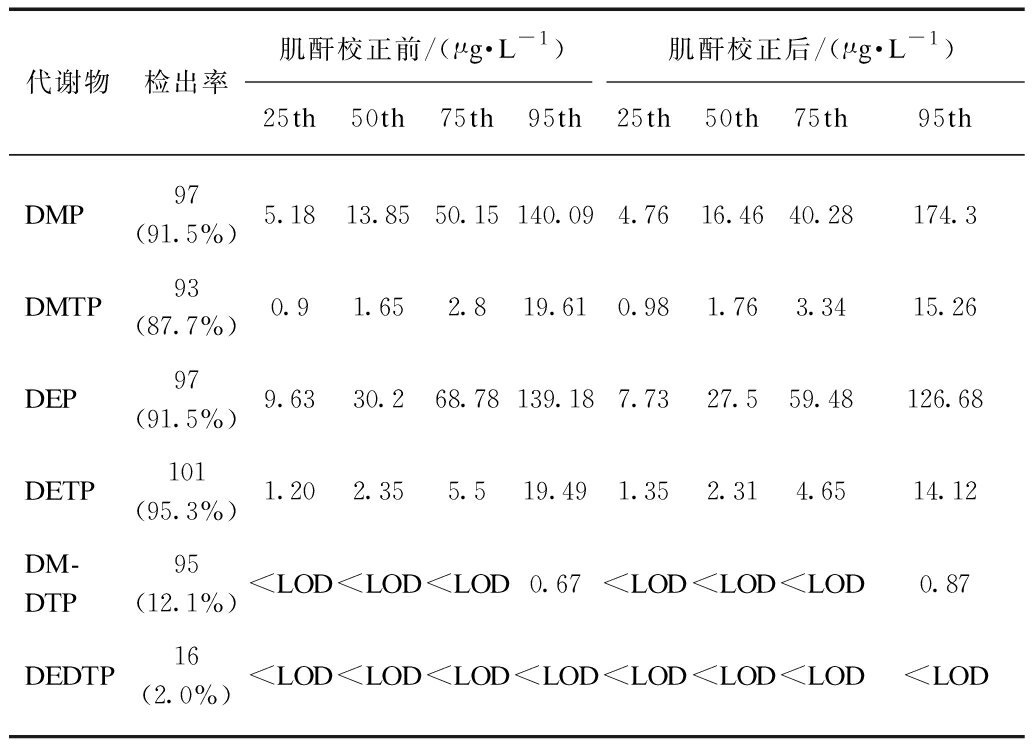
代谢物检出率肌酐校正前/(μg·L-1)肌酐校正后/(μg·L-1)25th50th75th95th25th50th75th95thDMP97(91.5%)5.1813.8550.15140.094.7616.4640.28174.3DMTP93(87.7%)0.91.652.819.610.981.763.3415.26DEP97(91.5%)9.6330.268.78139.187.7327.559.48126.68DETP101(95.3%)1.202.355.519.491.352.314.6514.12DM-DTP95(12.1%)
表4 女性孕前DAP代谢物浓度与新生儿出生结局之间的关联
Tab.4 Association between preconception DAP metabolite levels and birth outcomes [β(95%CI)]
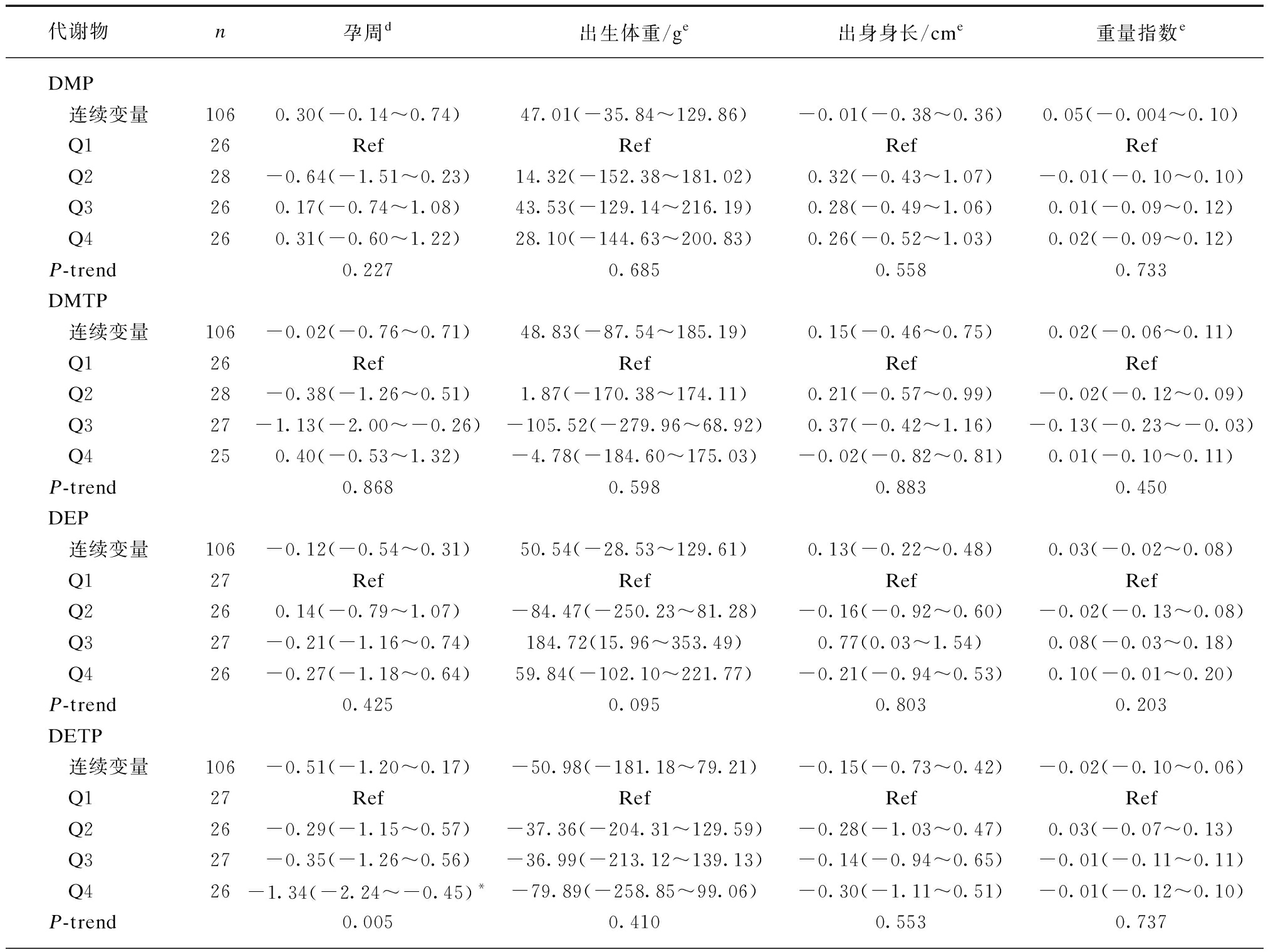
代谢物n孕周d出生体重/ge出身身长/cme重量指数eDMP 连续变量1060.30(-0.14~0.74)47.01(-35.84~129.86)-0.01(-0.38~0.36)0.05(-0.004~0.10) Q126RefRefRefRef Q228-0.64(-1.51~0.23)14.32(-152.38~181.02)0.32(-0.43~1.07)-0.01(-0.10~0.10) Q3260.17(-0.74~1.08)43.53(-129.14~216.19)0.28(-0.49~1.06)0.01(-0.09~0.12) Q4260.31(-0.60~1.22)28.10(-144.63~200.83)0.26(-0.52~1.03)0.02(-0.09~0.12)P-trend0.2270.6850.5580.733DMTP 连续变量106-0.02(-0.76~0.71)48.83(-87.54~185.19)0.15(-0.46~0.75)0.02(-0.06~0.11) Q126RefRefRefRef Q228-0.38(-1.26~0.51)1.87(-170.38~174.11)0.21(-0.57~0.99)-0.02(-0.12~0.09) Q327-1.13(-2.00~-0.26)-105.52(-279.96~68.92)0.37(-0.42~1.16)-0.13(-0.23~-0.03) Q4250.40(-0.53~1.32)-4.78(-184.60~175.03)-0.02(-0.82~0.81)0.01(-0.10~0.11)P-trend0.8680.5980.8830.450DEP 连续变量106-0.12(-0.54~0.31)50.54(-28.53~129.61)0.13(-0.22~0.48)0.03(-0.02~0.08) Q127RefRefRefRef Q2260.14(-0.79~1.07)-84.47(-250.23~81.28)-0.16(-0.92~0.60)-0.02(-0.13~0.08) Q327-0.21(-1.16~0.74)184.72(15.96~353.49)0.77(0.03~1.54)0.08(-0.03~0.18) Q426-0.27(-1.18~0.64)59.84(-102.10~221.77)-0.21(-0.94~0.53)0.10(-0.01~0.20)P-trend0.4250.0950.8030.203DETP 连续变量106-0.51(-1.20~0.17)-50.98(-181.18~79.21)-0.15(-0.73~0.42)-0.02(-0.10~0.06) Q127RefRefRefRef Q226-0.29(-1.15~0.57)-37.36(-204.31~129.59)-0.28(-1.03~0.47)0.03(-0.07~0.13) Q327-0.35(-1.26~0.56)-36.99(-213.12~139.13)-0.14(-0.94~0.65)-0.01(-0.11~0.11) Q426-1.34(-2.24~-0.45)*-79.89(-258.85~99.06)-0.30(-1.11~0.51)-0.01(-0.12~0.10)P-trend0.0050.4100.5530.737
续表

代谢物n孕周d出生体重/ge出身身长/cme重量指数e∑DAP 连续变量1060.40(-0.35~1.15)61.79(-79.26~202.83)-0.05(-0.68~0.57)0.07(-0.02~0.16) Q126RefRefRefRef Q2280.50(-0.41~1.41)-100.29(-266.08~65.51)-0.39(-1.14~0.37)-0.01(-0.11~0.09) Q327-0.34(-1.22~0.54)165.44(4.63~326.24)0.64(-0.09~1.37)0.07(-0.03~0.17) Q4250.79(-0.13~1.71)-42.34(-212.29~127.61)-0.30(-1.08~0.47)0.03(-0.08~0.14)P-trend0.3900.4170.7140.244
d调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、流产史及妊娠期并发症(糖尿病、高血压、贫血);e调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、分娩孕周、流产史及妊娠期并发症(糖尿病、高血压、贫血);*P<0.05
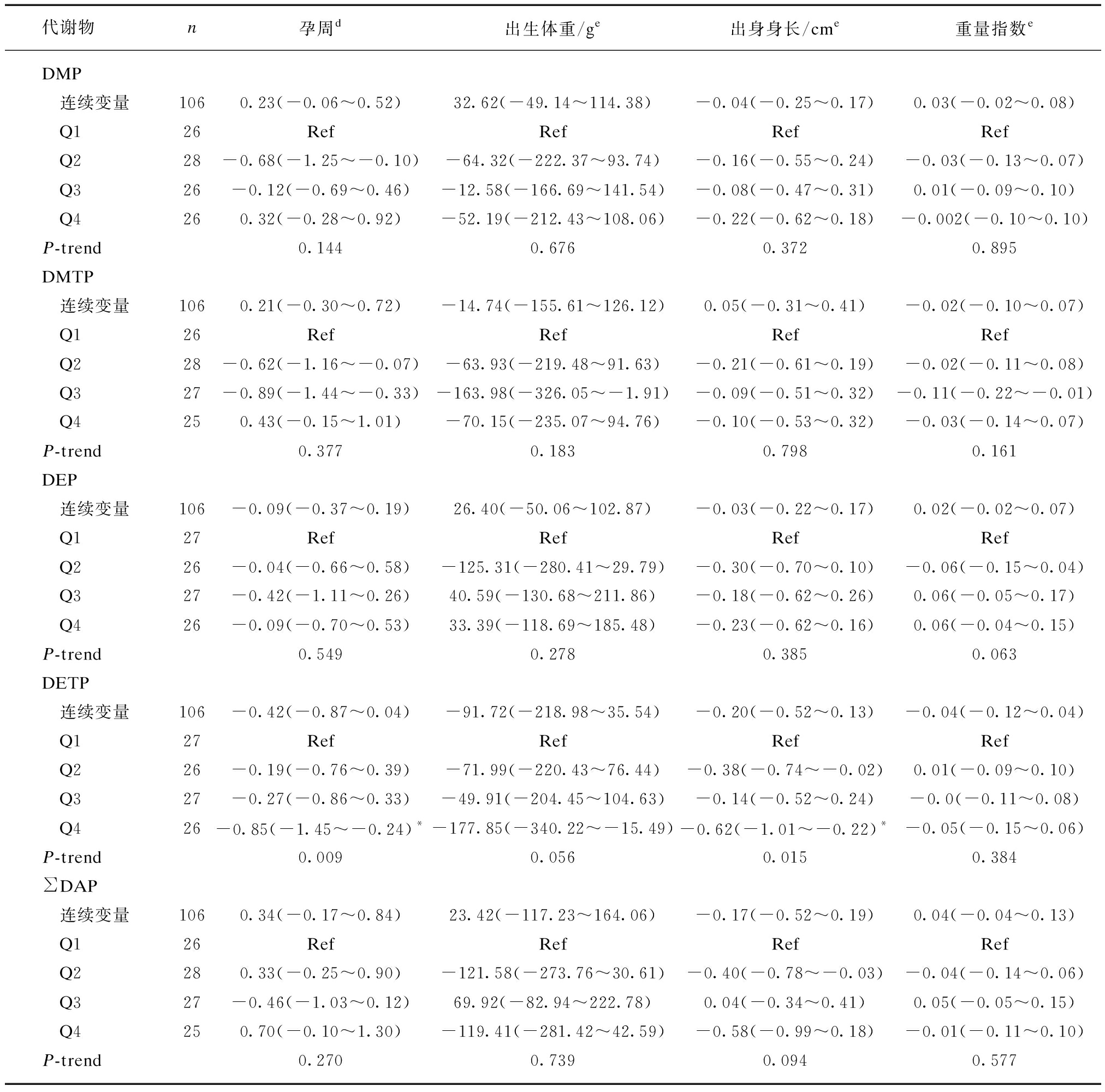
表5 足月儿母亲孕前期DAP代谢物水平与出生结局之间的关联
Tab.5 Association between DAP levels and birth outcomes among term infants [n=98,β(95%CI)]
代谢物n孕周d出生体重/ge出身身长/cme重量指数eDMP 连续变量1060.23(-0.06~0.52)32.62(-49.14~114.38)-0.04(-0.25~0.17)0.03(-0.02~0.08) Q126RefRefRefRef Q228-0.68(-1.25~-0.10)-64.32(-222.37~93.74)-0.16(-0.55~0.24)-0.03(-0.13~0.07) Q326-0.12(-0.69~0.46)-12.58(-166.69~141.54)-0.08(-0.47~0.31)0.01(-0.09~0.10) Q4260.32(-0.28~0.92)-52.19(-212.43~108.06)-0.22(-0.62~0.18)-0.002(-0.10~0.10)P-trend0.1440.6760.3720.895DMTP 连续变量1060.21(-0.30~0.72)-14.74(-155.61~126.12)0.05(-0.31~0.41)-0.02(-0.10~0.07) Q126RefRefRefRef Q228-0.62(-1.16~-0.07)-63.93(-219.48~91.63)-0.21(-0.61~0.19)-0.02(-0.11~0.08) Q327-0.89(-1.44~-0.33)-163.98(-326.05~-1.91)-0.09(-0.51~0.32)-0.11(-0.22~-0.01) Q4250.43(-0.15~1.01)-70.15(-235.07~94.76)-0.10(-0.53~0.32)-0.03(-0.14~0.07)P-trend0.3770.1830.7980.161DEP 连续变量106-0.09(-0.37~0.19)26.40(-50.06~102.87)-0.03(-0.22~0.17)0.02(-0.02~0.07) Q127RefRefRefRef Q226-0.04(-0.66~0.58)-125.31(-280.41~29.79)-0.30(-0.70~0.10)-0.06(-0.15~0.04) Q327-0.42(-1.11~0.26)40.59(-130.68~211.86)-0.18(-0.62~0.26)0.06(-0.05~0.17) Q426-0.09(-0.70~0.53)33.39(-118.69~185.48)-0.23(-0.62~0.16)0.06(-0.04~0.15)P-trend0.5490.2780.3850.063DETP 连续变量106-0.42(-0.87~0.04)-91.72(-218.98~35.54)-0.20(-0.52~0.13)-0.04(-0.12~0.04) Q127RefRefRefRef Q226-0.19(-0.76~0.39)-71.99(-220.43~76.44)-0.38(-0.74~-0.02)0.01(-0.09~0.10) Q327-0.27(-0.86~0.33)-49.91(-204.45~104.63)-0.14(-0.52~0.24)-0.0(-0.11~0.08) Q426-0.85(-1.45~-0.24)*-177.85(-340.22~-15.49)-0.62(-1.01~-0.22)*-0.05(-0.15~0.06)P-trend0.0090.0560.0150.384∑DAP 连续变量1060.34(-0.17~0.84)23.42(-117.23~164.06)-0.17(-0.52~0.19)0.04(-0.04~0.13) Q126RefRefRefRef Q2280.33(-0.25~0.90)-121.58(-273.76~30.61)-0.40(-0.78~-0.03)-0.04(-0.14~0.06) Q327-0.46(-1.03~0.12)69.92(-82.94~222.78)0.04(-0.34~0.41)0.05(-0.05~0.15) Q4250.70(-0.10~1.30)-119.41(-281.42~42.59)-0.58(-0.99~0.18)-0.01(-0.11~0.10)P-trend0.2700.7390.0940.577
d调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、流产史及妊娠期并发症(糖尿病、高血压、贫血);e调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、分娩孕周、流产史及妊娠期并发症(糖尿病、高血压、贫血);*P<0.05
表6 女性孕前DAP代谢物水平与男孩出生结局之间的关联
Tab.6 Association between DAP metabolite levels and birth outcomes among male neonates [β(95%CI)]
代谢物孕周出生体重/ge出身身长/cme重量指数eDMP 连续变量-0.12(-0.94~0.71)-46.22(-197.73~105.29)-0.34(-0.95~0.27)0.02(-0.09~0.12) Q1RefRefRefRef Q2-1.56(-2.84~-0.27)-166.08(-460.46~128.30)-1.51(-2.63~-0.40)0.09(-0.10~0.29) Q3-0.05(-1.26~1.15)9.62(-266.06~285.31)-0.49(-1.54~0.55)0.08(-0.10~0.26) Q4-0.07(-1.33~1.18)-113.87(-401.51~173.78)-0.32(-1.42~0.77)-0.03(-0.22~0.16)P-trend0.7490.6650.7820.851DMTP 连续变量-0.62(-1.87~0.63)-19.70(-255.52~216.11)0.17(-0.79~1.14)-0.04(-0.20~0.12) Q1RefRefRefRef Q2-0.58(-2.07~0.91)-23.91(-325.78~277.97)-0.13(-1.45~1.20)0.04(-0.21~0.22) Q3-1.98(-3.34~-0.61)-166.59(-465.26~132.07)0.40(-0.91~1.70)-0.19(-0.41~0.02) Q4-0.42(-1.86~1.02)-234.03(-525.55~57.50)-0.23(-1.50~1.05)-0.15(-0.36~0.07)P-trend0.2980.0520.9100.060DEP 连续变量-0.55(-1.18~0.08)36.92(-88.56~162.40)-0.29(-0.79~0.22)0.07(-0.01~0.16) Q1RefRefRefRef Q2-0.71(-1.98~0.56)90.93(-164.6~346.48)-0.58(-1.63~0.48)0.16(-0.02~0.34) Q3-1.40(-2.65~-0.15)36.42(-225.44~298.28)-1.02(-2.10~0.06)0.19(-0.05~0.37) Q4-0.95(-2.18~0.27)123.48(-126.93~373.88)-0.60(-1.63~0.43)0.18(-0.03~0.35)P-trend0.0690.4520.1620.567DETP 连续变量-1.26(-2.49~-0.04)23.41(-229.81~276.63)-0.20(-1.23~0.84)0.05(-0.12~0.22) Q1RefRefRefRef Q2-0.95(-2.11~0.21)47.32(-192.11~286.75)-0.77(-1.77~0.23)0.15(-0.02~0.33) Q3-0.67(-1.90~0.56)85.86(-164.49~336.20)-0.18(-1.23~0.86)0.10(-0.08~0.28) Q4-1.72(-3.02~-0.43)*-47.62(-327.82~232.59)-0.73(-1.90~0.44)0.07(-0.13~0.28)P-trend0.0230.8230.4590.668∑DAP 连续变量-0.19(-1.49~1.11)-6.87(-246.20~232.46)-0.60(-1.56~0.35)0.08(-0.08~0.24) Q1RefRefRefRef Q2-0.52(-1.86~0.82)79.28(-220.85~379.40)-0.65(-1.84~0.53)0.16(-0.04~0.35) Q3-1.35(-2.70~-0.01)73.27(-228.16~374.70)-0.24(-1.43~0.95)0.08(-0.12~0.28) Q4-0.67(-1.90~0.55)-43.73(-318.69~231.24)-0.87(-1.95~0.22)0.09(-0.09~0.27)P-trend0.1970.7060.2030.554
d调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、流产史及妊娠期并发症(糖尿病、高血压、贫血);e调整年龄、孕前BMI、家庭收入、吸烟状况、男性教育水平、不孕原因、不孕时间、分娩孕周、流产史及妊娠期并发症(糖尿病、高血压、贫血);*P<0.05
3 讨 论
本研究结果显示,上海地区ART女性孕前尿液OPs代谢物浓度远高于发达国家,并且发现孕前OPs浓度主要影响新生儿分娩孕周,男婴对OPs暴露更敏感。
本研究定量检测了上海市106名ART女性孕前尿液DAP代谢物的水平,其中位数分别为DMP 16.46μg/g,DMTP 1.76μg/g,DEP 27.5μg/g,DETP 2.31μg/g。一项来自美国CHAMACOS队列研究,检测了居住在加利福尼亚州农业区附近498名孕妇尿液DAP代谢物水平,其中位数分别为DMP 1.92μg/g、DMTP 6.46μg/g、DEP 0.29μg/g、DETP 2.55μg/g[17]。另一项在荷兰进行的Gene-ration R出生队列研究,于2002—2006年评估了鹿特丹100名孕期女性OPs暴露水平,则尿液中DMP、DMTP、DEP、DETP的中位数分别为17.64、15.48、2.96、1.05μg/g[18]。总体而言,本研究女性尿液OPs暴露水平高于欧美发达国家。此外,本课题组前期已发表上海市普通人群(自然受孕女性)OPs暴露水平。经过比较,本研究ART女性DMP、DEP中位数分别是自然受孕女性的2.4倍(16.46 vs 6.99μg/g)和2.7倍(27.5 vs 10.25μg/g),而两组人群的DMTP(1.76 vs 2.79μg/g)与DETP(2.31 vs 3.47μg/g)中位数水平相当,提示ART妇女的OPs暴露水平高于自然受孕女性[19]。因此,在中国ART女性中探究OPs暴露对新生儿生长发育的影响值得关注。
既往的人群研究主要以自然受孕分娩的新生儿作为观察对象,且结果报道不完全一致[10-16]。一项来自美国纽约市的出生队列研究显示,孕期OPs暴露可显著降低新生儿出生体重和身长[11]。另一项来自美国加利福尼亚州农业区的队列研究表明,孕期DAP暴露与出生体重、身长、体重指数、头围均无关联,但能显著缩短出生孕周[10]。其中有两项研究均未发现OPs暴露水平对子代出生结局的影响[15-16]。当前,关于ART女性孕前OPs暴露与新生儿出生结局的相关流行病学研究非常有限。仅有一项来自美国的环境与生殖健康(EARTH)队列研究,评估了ART夫妇孕前环境污染物暴露对子代健康影响,该研究表明孕前尿液邻苯二甲酸盐和酚类暴露水平与胎儿出生体重呈显著负相关[20-21]。因此,有关孕前OPs暴露对子代出生结局影响的研究尚需在多中心大样本的研究中进一步的探索和验证。
动物研究表明,OPs可能通过氧化应激的方式导致胎盘线粒体功能障碍,降低腺苷酸环化酶活性,或者干扰正常甲状腺激素功能,进而影响胎儿生长发育,为本研究提供了一定的理论依据[22-23]。值得注意的是,本研究还观察到孕前OPs暴露对出生结局的影响可能存在性别差异,孕前DETP水平仅与男婴出生孕周呈负相关。Wang等[24]招募187对母婴进行研究,发现在女婴中(n=91)孕期尿液DEs水平与出生孕周呈负相关。然而,Dalsager等[16]发现,母亲OPs暴露(n=858)与男婴的出生体重存在显著负相关性。目前OPs对子代出生结局影响具有性别差异的作用机制尚不清楚。已有动物研究显示,OPs具有环境内分泌干扰作用,可通过影响类固醇激素合成途径的芳构化作用而直接影响性激素的合成[25]。这意味着OPs可能导致体内激素失衡而不同程度地影响着男婴和女婴的生长发育。由于OPs暴露对性别易感性的相关研究有限,因此需要进一步探索。
本研究尚存在一些局限性: (1) 使用孕前单次随机尿液OPs检测结果不能完全代表整个孕期OPs暴露状况,今后的研究将评估多时点暴露以弥补不足。(2) 受到课题时间及条件限制,目前只检测单一污染物暴露,可能存在其他环境污染物(包括铅、汞、拟除虫菊酯农药)暴露对子代健康影响的混杂作用。(3) 由于本研究中早产儿(n=8,7.5%),低出生体重(n=4,3.8%)和小于胎龄儿(n=1,0.9%)所占比例很小,所以没有再针对这些指标做进一步的分层分析。鉴于以上存在的不足,需要对大量孕妇和婴儿进行长期随访,以评估农药暴露对胎儿生长发育的潜在不利健康影响。
综上所述,本研究发现孕前OPs暴露对出生结局的不良影响可能存在性别差异。考虑到上海地区易感人群农药暴露的普遍性,因此未来的研究需要关注多种污染物暴露对孕妇及其子代健康的影响。
[1] 杨益军.我国农药需求状况和趋势分析[J].营销界(农资与市场),2015(17): 38-41.
[2] 束放,王强,韩梅.2013年我国农药生产与使用概况[J].中国植保导刊,2014,34(12): 49-52.
[3] PEIRIS-JOHN R J, WICKREMASINGHE R. Impact of low-level exposure to organophosphates on human reproduction and survival[J]. Trans R Soc Trop Med Hyg, 2008,102(3): 239-245.
[4] MIGNERON-FOISY V, BOUCHARD M F, FREEMAN E E, et al. Myopia and exposure to organophosphate and pyrethroid pesticides in the general United States population[J]. Invest Ophthalmol Vis Sci, 2017,58(11): 4915-4924.
[5] WHYATT R M, BARR D B. Measurement of organophosphate metabolites in postpartum meconium as a potential biomarker of prenatal exposure: a validation study[J]. Environ Health Perspect, 2001,109(4): 417-420.
[6] BRADMAN A, BARR D B, CLAUS HENN B G, et al. Measurement of pesticides and other toxicants in amniotic fluid as a potential biomarker of prenatal exposure: a validation study[J]. Environ Health Perspect, 2003,111(14): 1779-1782.
[7] 金帆.ART安全性临床流行病学研究[J].科技纵览,2017(2): 68-69.
[8] HORNUNG R W, REED L D. Estimation of average concentration in the presence of nondetectable values[J]. Appl Occup Environ Hyg, 1990,5(1): 46-51.
[9] ARCURY T A, GRZYWACZ J G, DAVIS S W, et al. Organophosphorus pesticide urinary metabolite levels of children in farmworker households in eastern North Carolina[J]. Am J Ind Med, 2006,49(9): 751-760.
[10] ESKENAZI B, HARLEY K, BRADMAN A, et al. Association of in utero organophosphate pesticide exposure and fetal growth and length of gestation in an agricultural population[J]. Environ Health Perspect, 2004,112(10): 1116-1124.
[11] WOLFF M S, ENGEL S, BERKOWITZ G, et al. Prenatal pesticide and PCB exposures and birth outcomes[J]. Pediatr Res, 2007,61(2): 243-250.
[12] RAUCH S A, BRAUN J M, BARR D B, et al. Associations of prenatal exposure to organophosphate pesticide metabolites with gestational age and birth weight[J]. Environ Health Perspect, 2012,120(7): 1055-1060.
[13] NAKSEN W, PRAPAMONTOL T, MANGKLABRUKS A, et al. Associations of maternal organophosphate pesticide exposure and PON1 activity with birth outcomes in SAWASDEE birth cohort, Thailand[J]. Environ Res, 2015,142: 288-296.
[14] HAUSER R, GASKINS A J, SOUTER I, et al. Urinary phthalate metabolite concentrations and reproductive outcomes among women undergoing in vitro fertilization: results from the EARTH study[J]. Environ Health Perspect, 2016,124(6): 831-839.
[15] HARLEY K G, ENGEL S M, VEDAR M G, et al. Prenatal exposure to organophosphorous pesticides and fetal growth: pooled results from four longitudinal birth cohort studies[J]. Environ Health Perspect, 2016,124(7): 1084-1092.
[16] DALSAGER L, CHRISTENSEN L E, KONGSHOLM M G, et al. Associations of maternal exposure to organophosphate and pyrethroid insecticides and the herbicide 2, 4-D with birth outcomes and anogenital distance at 3 months in the Odense Child Cohort[J]. Reprod Toxicol, 2018,76: 53-62.
[17] BRADMAN A, ESKENAZI B, BARR D B, et al. Organophosphate urinary metabolite levels during pregnancy and after delivery in women living in an agricultural community[J]. Environ Health Perspect, 2005,113(12): 1802-1807.
[18] YE X B, PIERIK F H, HAUSER R, et al. Urinary metabolite concentrations of organophosphorous pesticides, bisphenol A, and phthalates among pregnant women in Rotterdam, the Netherlands: the Generation R study[J]. Environ Res, 2008,108(2): 260-267.
[19] HU Y, JI L, ZHANG Y, et al. Organophosphate and pyrethroid pesticide exposures measured before conception and associations with time to pregnancy in Chinese couples enrolled in the Shanghai birth cohort[J]. Environ Health Perspect, 2018,126(7): 077001.
[20] MESSERLIAN C, MUSTIELES V, MINGUEZ-ALARCON L, et al. Preconception and prenatal urinary concentrations of phenols and birth size of singleton infants born to mothers and fathers from the Environment and Reproductive Health(EARTH) study[J]. Environ Int, 2018,114: 60-68.
[21] MESSERLIAN C, BRAUN J M, M NGUEZ-ALARC
NGUEZ-ALARC N L, et al. Paternal and maternal urinary phthalate metabolite concentrations and birth weight of singletons conceived by subfertile couples[J]. Environ Int, 2017,107: 55-64.
N L, et al. Paternal and maternal urinary phthalate metabolite concentrations and birth weight of singletons conceived by subfertile couples[J]. Environ Int, 2017,107: 55-64.
[22] PEARSON J N, PATEL M. The role of oxidative stress in organophosphate and nerve agent toxicity[J]. Ann N Y Acad Sci, 2016,1378(1): 17-24.
[23] SONG X, SEIDLER F J, SALEH J L, et al. Cellular mechanisms for developmental toxicity of chlorpyrifos: targeting the adenylyl cyclase signaling cascade[J]. Toxicol Appl Pharmacol, 1997,145(1): 158-174.
[24] WANG P, TIAN Y, WANG X J, et al. Organophosphate pesticide exposure and perinatal outcomes in Shanghai, China[J]. Environ Int, 2012,42: 100-104.
[25] TIAN H, SUN Y, WANG H, et al. Monocrotophos pesticide affects synthesis and conversion of sex steroids through multiple targets in male goldfish(Carassius auratus)[J]. Sci Rep, 2017,7(1): 2306.