生物传感器是一种多学科渗透的技术,它是以生物活性单元作为生物敏感元件,通过转换元件和信号放大装置对被测物质进行高度选择性检测的检测装置[1]。根据传感器中生物活性单元上敏感物质的不同可将其分为酶传感器、微生物传感器、免疫传感器、组织传感器、核酸传感器、细胞及细胞器传感器。而根据信号转化类型又可分为电化学生物传感器、半导体生物传感器、测热型生物传感器、测光型生物传感器[2]、测声型生物传感器等[3]。
在传感器的设计中不仅有物理化学因素的引入,在近几年的研究中,很多材料学方面的创新也不断出现。各种类型纳米粒子和其他纳米材料的使用可以很大程度上改进生物传感器的检测性能[4-6],主要是利用此类材料导电性、磁性[7]、生物兼容性、大比表面积等方面的优点[8]。而具体这些纳米材料在各种传感器设计中所起到的具体作用却是模糊的,或者说是分类不够明确。本文拟以免疫生物传感器为例,总结近年来纳米材料在生物传感器设计中的应用,对免疫传感器研究中纳米材料所充当的具体作用进行分类。这样的综合分析不仅对分析领域的化学家而且对医学和生物学研究领域的研究者或是初入传感器领域的一些学者来说都大有裨益,毕竟这种简洁纵向的分析论述也是少见的。
本论述中所涉及的传感技术主要以电化学和一些光学传感器为主,也有部分化学发光传感器,比较特殊的有免疫磁力检测型传感器[9],但传感器的设计大都是以抗原抗体免疫分析为主。电化学主要表现为最简单的电流测量,然后是伏安法和阻抗检测。光学检测类传感主要涉及电化学发光和拉曼散射以及荧光信号检测。所提到的纳米粒子大致为金属和金属氧化物,特别是金纳米粒子、碳类纳米材料,磁性纳米粒子等。单个传感器通常还含有其他组分,包括产生氧化还原活性供体/受体的酶(过氧化物酶,葡萄糖氧化酶,碱性磷酸酶),电活性分子(例如阿霉素)。这些纳米材料与传感器的有机结合使传感器的性能大大提高,同时也在很大程度上拓宽了免疫传感器的设计思路。
纳米材料作为一类非生物类物质,要参与到生物反应中必需考虑如何与生物类分子进行结合,这个结合过程被称为纳米材料的生物功能化。目前已知的常见的几种结合方法分别是非共价键结合(π-π键等)、共价键结合以及一些特殊的结合方式(链霉素-亲和素结合系统等)。与生物分子结合之后的纳米材料在整个传感器的设计中发挥着不同的功能,可大致分为纳米材料作为生物分子载体、纳米材料对检测信号进行放大以及纳米材料本身作为一种信号分子材料被检测系统检测等3类,然究其根本都是为了最终提高生物传感器的敏感性。
1 载体功能
由于纳米材料独特的性质,特别是碳和金属类材料,不仅具有良好的导电性和生物相容性,还可以作为生物分子载体,增强探针的比表面积,同时纳米粒子作为基底支持物,可以捕获大量靶分子或信号分子[9-10]。
1.1 碳类纳米材料
目前,碳纳米管由于其所带多种基团可以促进抗体与纳米管之间的结合且具有较大的比表面积,已广泛用于固定抗体以制备电化学免疫生物传感器的载体。同时,一些碳纳米管相关的材料也可以在一定程度上改善非特异性吸附,比如研究表明多壁碳纳米管(multi-walled carbon nanotubes, MWCNTs)相比于石墨烯类碳材料就能在一定程度上防止抗体的非特异吸附[11]。Han等[12]通过气相化学沉积法制备了一种垂直排列的MWCNTs,并在碱性溶液中对其进行功能化使其生成含氧基团,这些基团可将微囊藻毒素(microcystin-LR, MC-LR)结合到MWCNTs表面的侧壁上,通过测量抗体与对MC-LR结合之前和之后电阻抗值的变化,实现了MC-LR的定量检测,其检测范围可以达到0.05~20μg/mL。Zhang和他的团队[13]也研发了一种同样可检测MC-LR的生物传感器,他们所使用的是一种氮杂多壁碳纳米管(CNx-MWNT)类纳米材料,这种碳纳米管不仅生物毒性低而且生物兼容性更好,同时合成方法既方便又环保,不需要一些复杂的化学试剂参与。他们将金纳米粒子(gold nanoparticles, AuNP)直接连接到这种CNx-MWNT上,制备了一种高灵敏免疫传感器以检测MC-LR。该传感器使用AuNP/CNx-MWNTs纳米复合物作为抗体固定支架,在优化后的最佳条件下,对MC-LR的检测范围可以达到0.005~1μg/mL,检测限为0.002μg/mL,信噪比3。检出限值远低于世界卫生组织指南中的规定。
另一种碳纳米材料石墨烯片,同样拥有较大的比表面积,被大量用作生物传感器的基底来负载生物分子,特别是氧化石墨烯和还原氧化石墨烯[14-16]。Eissa等[17]报道了一种基于氧化石墨烯的竞争性免疫传感器,用于测定贝类组织中冈田酸(Okadaic acid, OA)含量。冈田酸抗体首先吸附在碳二亚胺修饰的羧基化氧化石墨烯电极上,然后OA通过和已知浓度的OA-卵清蛋白结合物竞争性结合提前固定在基板上的抗体,最后通过检测电化学信号值变化得到OA的检测量。在另一个检测血管内皮细胞因子受体2(vascular endothelial growth factor 2, VEGFR2)的电化学免疫传感器中,Wei等[18]采用也使用了石墨烯来增强基底比表面积,加速界面电子传递,该传感器可以检测细胞裂解液中VEGFR2蛋白的浓度,可以区分不同抑制剂诱导的VEGFR2的表达变化。
1.2 金属类纳米材料
金属类纳米材料中经常被用做生物分子和信号分子载体的是金纳米粒子。金纳米粒子俗称胶体金,由于其体积小、比表面积大、生物相容性好等优点,使得金纳米粒子在电化学传感器的设计中大放异彩。Hao等[19]就使用24nm的金纳米粒子同时作为抗体和单链DNA链的载体,构建了一种利用等温扩增放大技术来增强传感器检测灵敏度的方法,同时得益于金纳米粒子的强导电性,使得最后被测物PSA的线性范围达到15pg/mL~8ng/mL,最低检测限值达到1.7pg/mL。
另外,复合型金属纳米粒子作为生物分子载体的传感器设计也展现了其特有的性质,比如壳核型双金属材料。金纳米粒子就经常被用于一些壳核类纳米粒子的制备,这种复合粒子在传感器的设计中可以同时发挥两种金属的优良性能[20-21]。Gan团队[22]就使用一种金/四氧化三铁壳核纳米材料(Fe3O4@PDA-Au)作为抗体和酶的载体来检测MC-LR。随着纳米材料制作工艺的一步步提升,更多种类更多形态的纳米材料也被应用于传感器的设计中。Sun团队[10]就同时以分支状的纳米氧化锌和多孔状的纳米氧化锌为载体构建了一种纸基电化学免疫传感器用于肿瘤标志物AFP的检测。
在众多研究中也不乏一些特色设计,比如Yang等[23]设计的传感器就将电化学信号分子阿霉素(doxorubicin, DOX)巧妙地封装在了多孔纳米金颗粒里面,多孔金纳米粒子不仅是DOX的载体,同时也是第二抗体的载体。另外,该设计中也将多孔类碳材料和金纳米粒子的复合物用于电极的修饰,多方面改善传感器的性能。最终,在最优条件下,该设计好的传感器对青霉素结合蛋白2a(penicillin-binding protein 2a, PbP2a)的最低检测限达到0.65pg/mL,信噪比为3。
2 信号放大功能
2.1 光信号放大功能
光学检测由于其灵敏度高,检测范围宽和多通路检测等特点而在生物传感器设计中被广泛使用。而一些金属或非金属性物质在纳米级时,它们的一些电学、热学和光学性质都发生了显著改变,特别是光学效应[24]。在光学传感器的设计中,功能化的纳米粒子合理利用之后可以显著增强光学检测性能,很大程度上起到放大光学信号的作用。
Liu等[25]设计了一种免疫生物传感器,该传感器由核壳表面增强拉曼散射(surface enhanced Raman scattering, SERS)纳米材料作为标签,用光子晶体珠(photonic crystal beads, PCB)作为载体,用于C反应蛋白(C-reactive protein, CRP)的超灵敏检测。当拉曼染料嵌入金银壳核界面上形成SERS纳米标签时,由于核壳结构的耦合,拉曼信号被显著放大,灵敏度得到显着提高,加之PCB的高体表面积,线性范围也得到扩展,而且这种类型的传感器具有稳定性良好和背景信号低等优点。
当在纳米粒子表面同时组装酶和抗体时,功能化的纳米粒子也可以方便地化学发光的免疫测定设计。Zhou等[26]将掺有Ru(bpy)32+的二氧化硅(Ru-SiO2)纳米颗粒和修饰了金纳米颗粒的石墨烯(P-RGO@Au)组合成P-RGO@Au@Ru-SiO2复合材料。使用该复合材料用于设计一种新型夹心式电化学发光免疫传感器,用于HIV-1 p24抗原的检测。由于SiO2纳米粒子的作用,每个Ru-SiO2复合物具有大量的Ru(bpy)32+分子,使得电化学发光(electrochemi-luminescence, ECL)信号被放大。使用用Ru-SiO2纳米颗粒和P-RGO@Au复合材料之后,该免疫传感器的线性范围为1.0×10-9~1.0×10-5 mg/mL,检出限值达到1ng/mL。
在光学传感器中,基于荧光检测的免疫分析传感器在新型纳米材料的帮助下,其敏感性也得到了很大提高。荧光免疫分析型传感器的灵敏度主要取决于3个因素: 荧光标记的强度,荧光基团的堆积密度,以及检测光学系统的参数[27]。而前两个因素均可以通过使用新型荧光纳米材料的方法来解决。Xie团队[28]基于点击化学设计了一种荧光免疫分析传感器用于AFP的检测,其使用氧化铜纳米粒子(CuO NPs)来放大荧光信号。当标记了抗体的CuO复合物探针溶解在HCL溶液中时,CuO会变成铜离子(Cu+),这一反应可以催化原先荧光染料的环加成作用,使之前的弱荧光物质变为强荧光物质,起到信号放大的作用。最终对AFP的检测范围为0.025~5.0ng/mL。检测限值为12pg/mL。而Hu团队[29]设计的另外一种用于检测致病性大肠杆菌的荧光免疫传感器,使用多孔硅纳米粒子负载荧光物质的方式来提高传感器的检测灵敏度,也得到了较理想的检测效果。
2.2 电信号放大功能
尽管许多免疫传感器的检测限已经达到了皮克级别,但是它们的电信号响应值通常在几微安级别,这就限制了传感器灵敏度的提升,这也表明灵敏度放大策略的研发是迫切且必要的。电化学免疫传感器的灵敏度定义为空白和有靶物质时电信号的差值[30]。因此,大电流差值通常意味着一个比较高的灵敏度。理论上来说,电流差值主要受传感材料和免疫探针的物理和化学性质的影响,比如说传感界面的导电性以及氧化还原材料的电化学活性。因此灵敏度的放大就聚焦在提高导电性、增强电流信号或者增加免疫反应面积这些层面。
在对电化学信号进行放大以提高检测灵敏度的方法上,纳米材料的使用作为一个新方向得到了大量关注,这其中金、硅、铂、和碳等纳米材料在传感器设计中的应用已经被大量报道。使用纳米粒子标记抗体相比于那些用传统的氧化还原分子(辣根过氧化物酶、二茂铁等)标记的抗体表现出更强的电流信号值。这种检测性能的增强要归功于导电纳米材料的应用,免疫反应界面的电子传递与电信号放大之间存在着很大关联,这种放大效果不仅体现在电极基板上电子的传递效率上,也体现在探针部分电化学信号物质之间与电极基板之间的电信号响应[31]。其中碳类纳米材料[32]和金属纳米材料都具有较高的电导率,可以促进生物分子和电极表面之间的直接电子转移[33]。Tang团队[34]就报道了这样一篇文章,采用聚合多巴胺/铅离子/壳聚糖/金纳米粒子复合物(Chit-AuNPs/PDA-Pb2+/GCE)修饰玻碳电极,由于PDA对铅离子的强吸附,使PDA-Pb2+产生了一个较强的电流信号,加之壳聚糖-AuNPs进一步对电信号起到放大作用,同时还提供了大量CEA抗体活性结合位点,使传感器从整体上拥有较高的电化学活性和导电性,最终综合提高了传感器的检测性能。这也说明金属离子氧化还原纳米材料的超灵敏性免疫测定效应。
在大量传感器的设计中,往往不是单独使用一种纳米材料,多种纳米材料或多重功能化纳米材料同时使用策略在提高传感器灵敏度方面发挥着重要作用。通常,这些策略表现为多重放大电流信号或者导电性。另外,一些纳米材料在传感器的设计中既可以起到放大电信号的作用,同时又充当了生物分子或是信号分子载体的双重作用。比如,Yang等[23]设计的夹心免疫传感器,多孔金充当了信号分子DOX载体的作用,多孔碳材料沉积到金电极上,可以提高大量的抗体结合位点;而另一方面,多孔金和多孔碳材料又因其具有较好的导电性,可以促进电子传递,几种材料共同作用,又发挥着多重作用,最终对电化学信号起到了多重放大作用,综合提高了传感器的检测灵敏度。
3 催化剂功能
部分纳米粒子可以充当催化剂,参与催化反应,而其催化效应远高于普通的生物类催化剂。钠米粒子或功能化纳米粒子的电催化是实现超灵敏检测的一种新方法,这种纳米材料催化剂是通过同时触发反应界面上氧化还原物质的电化学氧化和催化反应来实现的。对于为什么纳米粒子的电化学反应能够产生催化效果的一种可能解释是,催化反应和电化学氧化的一种耦联[35]。
通常来说,催化反应对于电信号的增强作用受传感界面导电性的影响,同时也和催化剂本身的催化性能和浓度有关,特别是催化性能。在纳米粒子充当催化剂的研究中,最常见且使用最广泛的是纳米粒子充当类过氧化物酶作用参与反应。比如在这篇3倍信号放大的文章中,作者使用导电性催化材料和生物酶复合物,铂纳米粒子-还原氧化石墨烯/辣根过氧化物酶-葡萄糖氧化酶/抗体(PtNPs-rGO/HRP-GOD/Ab)复合物,作为检测探针,使得该传感器拥有三级催化效果。生物酶GOD-HRP和纳米粒子PtNPs在电场作用下都可以加速葡萄糖的氧化和过氧化氢的还原。PtNPs-rGO不仅可以充当酶的作用促进电子的转移,而且其大比表面积能够富集大量的酶、抗体-氧化还原物质,最终使电流信号大大增强。与单用其中一种催化剂相比,多联催化展现出了较强的催化性能,放大效果也更强[36]。
另外,也有一些研究发现合金纳米粒子比单独一种纳米粒子拥有更强的催化效果。Zhang等[37]就发现钯铂合金纳米粒子比单独使用铂或钯纳米粒子催化过氧化氢效果更强。于是他们团队基于钯铂合金/辣根过氧化物酶(PbtNPs@PtNPs/HRP)联合应用催化过氧化氢这构建了一种电化学免疫传感器用于EB病毒衍生的潜伏膜蛋白1(LMP-1)的检测,最终的检测范围为0.01~40ng/mL,最低检测限为0.62pg/mL。
磁性纳米粒子(MNP)也是另外一种特殊的具有与天然过氧化物酶有类似酶活性的纳米材料[38]。Fe3O4 MNP作为催化剂非常有效,其对基质3,3,5,5-四甲基联苯胺的结合亲和力高于辣根过氧化物酶(HRP)[39]。在相同的摩尔浓度下,Fe3O4 MNP显示出比HRP高40倍的活性水平。基于这一发现,有研究者设计了一种新的免疫分析方法[40],将单克隆CEA抗体固定在金纳米粒子(AuNPs)沉积的电极上,磁珠(MB)和CEA共轭的多个3,3,5,5-四甲基联苯胺(TMB)被用作电化学标记,基于MB/TMB-共轭CEA和游离CEA之间竞争结合后,多个TMB标签对抗坏血酸(AA)的电催化氧化效果检测来达到检测样本CEA的目的。最终该传感器对CEA的最低检测限达到1pg/mL[41]。磁性纳米粒子不同于其他类拟酶纳米粒子(钯铂类),由于Fe3O4 MNP还具有磁性的特点,基于这一原理设计的传感器在操作过程中还会更易于分离产物[42-43],所以更受研究者青睐。
4 信号分子功能
随着生物传感技术的发展,纳米材料的其它一些特殊性质也被挖掘出来,用于生物传感器的构建。比如纳米粒子直接充当信号分子,结合特殊检测仪器用于生物分子的检测。Orlov和他的团队[9]就利用磁性纳米粒子的磁性效应结合侧流免疫层吸技术构建了一种生物传感器用于PSA的检测。在这项研究中,200nm的磁性粒子不仅发挥信号分子的作用,还作为第一抗体的载体捕获PSA抗原,然后基于免疫层吸原理,在260μm厚的硝化纤维膜上侧向运动到达检测区域,与第二抗体结合形成免疫夹心复合物。然后通过特殊的磁力计(magnetic particle quantification reader, MPQ reader)进行磁力信号检测。该传感器对PSA的最低检测限可以达到25pg/mL,而且由于采用了免疫层析技术,整个检测过程只需要30min。
5 展 望
科学研究从来都不是单向独立发展的,特别是最近几年来,多学科交叉渗透发展更是显现出了巨大优势。随着材料学的快速发展,其在生物传感器研究领域的应用也越来越受到重视。纳米材料的使用在提高生物传感器的敏感性方面具有巨大潜力,通过描述现阶段在免疫传感器设计构建中经常被用到的一些纳米材料,并大致从其发挥作用的4个方面对其进行了论述。此类纳米材料之所以能够被广泛应用,与其简易的制造过程也是分不开的。众多传感器设计中所使用的纳米材料基本都是一些在普通试验室可以简单合成的,并且生物传感器设计所需要的一些物理性质,例如稳定性,生物兼容性、导电性,电化学活性和催化性能都可以保证,且易于保存。而对于超灵敏测定,纳米材料的这些性质都发挥着重要作用,综合这些因素,纳米材料在免疫传感器以及其它类型传感器的设计中被广泛使用。对于传感器的性能来说,稳定性和重复性也是必不可少的一项考核指标,在后续的研究中,有必要进一步探索发现新型纳米材料,用于超灵敏检测,或是发现现有纳米材料的一些未知性能,并有效的应用于传感器的设计中,改善传感器性能,促进传感器与纳米材料学的多学科交流发展。
[1] MADURAIVEERAN G, SASIDHARAN M, GANESAN V.Electrochemical sensor and biosensor platforms based on advanced nanomaterials for biological and biomedical applications[J].Biosens Bioelectron, 2018,103: 113-129.
[2] 聂玮,李娟,曹晓炼,等.基于荧光共振能量转移技术的快速检测CA16型手足口病病原体新方法的建立及其评价[J].吉林大学学报(医学版),2020,46(1): 169-175.
[3] 陈玲.生物传感器的研究进展综述[J].传感器与微系统,2006,25(9): 4-7.
[4] LU Y X, ZHAO H, LI C P.Advances in detection of nucleic acid tumor biomarkers via electrochemical biosensors[J].Sci Sin-Vitae, 2019,49(7): 814-827.
[5] JIANG Y, WU J.Recent development in chitosan nanocomposites for surface-based biosensor applications[J].Electrophoresis, 2019,40(16-17): 2084-2097.
[6] NEETHIRAJAN S, WENG X, TAH A, et al.Nano-biosensor platforms for detecting food allergens-New trends[J].Sens Bio-Sens Res, 2018,18: 13-30.
[7] 赵慧君,王德平,黄文旵,等.磁性纳米微球的特性及其在生物医学中的应用[J].同济大学学报(医学版),2003,24(4): 288-291.
[8] POSCHENRIEDER A, THALER M, JUNKER R, et al.Recent advances in immunodiagnostics based on biosensor technologies-from central laboratory to the point of care[J].Anal Bioanal Chem, 2019,411(29): 7607-7621.
[9] ORLOV A V, BRAGINA V A, NIKITIN M P, et al.Rapid dry-reagent immunomagnetic biosensing platform based on volumetric detection of nanoparticles on 3D structures[J].Biosens Bioelectron, 2016,79: 423-429.
[10] SUN G Q, YANG H M, ZHANG Y, et al.Branched zinc oxide nanorods arrays modified paper electrode for electrochemical immunosensing by combining biocatalytic precipitation reaction and competitive immunoassay mode[J].Biosens Bioelectron, 2015,74: 823-829.
[11] S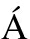 NCHEZ S, PUMERA M, F
NCHEZ S, PUMERA M, F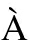 BREGAS E.Carbon nanotube/polysulfone screen-printed electrochemical immunosensor[J].Biosens Bioelectron, 2007,23(3): 332-340.
BREGAS E.Carbon nanotube/polysulfone screen-printed electrochemical immunosensor[J].Biosens Bioelectron, 2007,23(3): 332-340.
[12] HAN C, DOEPKE A, CHO W, et al.A multiwalled-carbon-nanotube-based biosensor for monitoring microcystin-LR in sources of drinking water supplies[J].Adv Funct Mater, 2013,23(14): 1807-1816.
[13] ZHANG J, LEI J P, PAN R, et al.In situ assembly of gold nanoparticles on nitrogen-doped carbon nanotubes for sensitive immunosensing of microcystin-LR[J].Chem Commun(Camb), 2011,47(2): 668-670.
[14] PARK S, SINGH A, KIM S, et al.Electroreduction-based electrochemical-enzymatic redox cycling for the detection of cancer antigen 15-3 using graphene oxide-modified indium-tin oxide electrodes[J].Anal Chem, 2014,86(3): 1560-1566.
[15] SRIVASTAVA S, KUMAR V, ALI M A, et al.Electrophoretically deposited reduced graphene oxide platform for food toxin detection[J].Nanoscale, 2013,5(7): 3043-3051.
[16] HAQUE A M, PARK H, SUNG D, et al.An electrochemically reduced graphene oxide-based electrochemical immunosensing platform for ultrasensitive antigen detection[J].Anal Chem, 2012,84(4): 1871-1878.
[17] EISSA S, ZOUROB M.A graphene-based electrochemical competitive immunosensor for the sensitive detection of okadaic acid in shellfish[J].Nanoscale, 2012,4(23): 7593-7599.
[18] WEI T X, TU W W, ZHAO B, et al.Electrochemical monitoring of an important biomarker and target protein: VEGFR2 in cell lysates[J].Sci Rep, 2014,4: 3982.
[19] HAO Y X, YAN P D, ZHANG X, et al.Ultrasensitive amperometric determination of PSA based on a signal amplification strategy using nanoflowers composed of single-strand DNA modified fullerene and Methylene Blue, and an improved surface-initiated enzymatic polymerization[J].Microchim Acta, 2017,184(11): 4341-4349.
[20] YANG T, TIAN L L, ZHOU E M, et al.Design of Ni(OH)2 nanocages@MnO2 nanosheets core-shell architecture to jointly facilitate electrocatalytic dynamic for highly sensitive detection of dopamine[J].Biosens Bioelectron, 2019,143: 111634.
[21] KHAN M S, AMEER H, ALI A, et al.Electrochemiluminescence behaviour of silver/silver orthophosphate/graphene oxide quenched by Pd@Au core-shell nanoflowers for ultrasensitive detection of insulin[J].Biosens Bioelectron, 2020,147: 111767.
[22] GAN C F, LING L, HE Z Y, et al.In-situ assembly of biocompatible core-shell hierarchical nanostructures sensitized immunosensor for microcystin-LR detection[J].Biosens Bioelectron, 2016,78: 381-389.
[23] YANG J, SHEN H W, ZHANG X, et al.A novel platform for high sensitivity determination of PbP2a based on gold nanoparticles composited graphitized mesoporous carbon and doxorubicin loaded hollow gold nanospheres[J].Biosens Bioelectron, 2016,77: 1119-1125.
[24] CHEN J, LIU J W, CHEN X G, et al.Recent progress in nanomaterial-enhanced fluorescence polarization/anisotropy sensors[J].Chin Chem Lett, 2019,30(9): 1575-1580.
[25] LIU B, NI H B, ZHANG D, et al.Ultrasensitive detection of protein with wide linear dynamic range based on core-shell SERS nanotags and photonic crystal beads[J].ACS Sens, 2017,2(7): 1035-1043.
[26] ZHOU L M, HUANG J S, YU B, et al.A novel electrochemiluminescence immunosensor for the analysis of HIV-1 p24 antigen based on P-RGO@Au@Ru-SiO2 composite[J].ACS Appl Mater Interfaces, 2015,7(44): 24438-24445.
[27] FARKA Z, ![]() D, et al.Nanoparticle-based immunochemical biosensors and assays: recent advances and challenges[J].Chem Rev, 2017,117(15): 9973-10042.
D, et al.Nanoparticle-based immunochemical biosensors and assays: recent advances and challenges[J].Chem Rev, 2017,117(15): 9973-10042.
[28] XIE Q F, WENG X H, LU L J, et al.A sensitive fluorescent sensor for quantification of alpha-fetoprotein based on immunosorbent assay and click chemistry[J].Biosens Bioelectron, 2016,77: 46-50.
[29] HU R R, YIN Z Z, ZENG Y B, et al.A novel biosensor for Escherichia coli O157: H7 based on fluorescein-releasable biolabels[J].Biosens Bioelectron, 2016,78: 31-36.
[30] LIU Z M, MA Z F.Fabrication of an ultrasensitive electrochemical immunosensor for Cea based on conducting long-chain polythiols[J].Biosens Bioelectron, 2013,46: 1-7.
[31] ZHU C Z, YANG G H, LI H, et al.Electrochemical sensors and biosensors based on nanomaterials and nanostructures[J].Anal Chem, 2015,87(1): 230-249.
[32] YANG Y B, YANG X D, YANG Y J, et al.Aptamer-functionalized carbon nanomaterials electrochemical sensors for detecting cancer relevant biomolecules[J].Carbon, 2018,129: 380-395.
[33] LI Y F, ZHANG H H, CAI X, et al.Electrochemical detection of superoxide anions in HeLa cells by using two enzyme-free sensors prepared from ZIF-8-derived carbon nanomaterials[J].Mikrochim Acta, 2019,186(6): 370.
[34] TANG Z X, MA Z F.Ultrasensitive amperometric immunoassay for carcinoembryonic antigens by using a glassy carbon electrode coated with a polydopamine-Pb(Ⅱ)redox system and a chitosan-gold nanocomposite[J].MicrochimActa, 2017,184(4): 1135-1142.
[35] MIAO L Y, JIAO L, ZHANG J, et al.Amperometric sandwich immunoassay for the carcinoembryonic antigen using a glassy carbon electrode modified with iridium nanoparticles, polydopamine and reduced graphene oxide[J].Microchim Acta, 2017,184(1): 169-175.
[36] JIA X L, CHEN X, HAN J M, et al.Triple signal amplification using gold nanoparticles, bienzyme and platinum nanoparticles functionalized graphene as enhancers for simultaneous multiple electrochemical immunoassay[J].Biosens Bioelectron, 2014,53: 65-70.
[37] ZHANG X, ZHOU D D, SHENG S C, et al.Electrochemical immunoassay for the cancer marker LMP-1(Epstein-Barr virus-derived latent membrane protein 1)using a glassy carbon electrode modified with Pd@Pt nanoparticles and a nanocomposite consisting of graphene sheets and MWCNTs[J].Microchim Acta, 2016,183(6): 2055-2062.
[38] CHEN Y, ZHANG Y Y, KOU Q W, et al.Enhanced catalytic reduction of 4-nitrophenol driven by Fe3O4-Au magnetic nanocomposite interface engineering: from facile preparation to recyclable application[J].Nanomaterials(Basel), 2018,8(5): E353.
[39] LI W S, FAN G C, GAO F X, et al.High-activity Fe3O4 nanozyme as signal amplifier: a simple, low-cost but efficient strategy for ultrasensitive photoelectrochemical immunoassay[J].Biosens Bioelectron, 2019,127: 64-71.
[40] AKTER R, KYUN RHEE C, RAHMAN M A.Sensitivity enhancement of an electrochemical immunosensor through the electrocatalysis of magnetic bead-supported non-enzymatic labels[J].Biosens Bioelectron, 2014,54: 351-357.
[41] WU D, MA H M, ZHANG Y, et al.Corallite-like magnetic Fe3O4@MnO2@Pt nanocomposites as multiple signal amplifiers for the detection of carcinoembryonic antigen[J].ACS Appl Mater Interfaces, 2015,7(33): 18786-18793.
[42] ZHANG X, BAO N, LUO X L, et al.Patchy gold coated Fe3O4 nanospheres with enhanced catalytic activity applied for paper-based bipolar electrode-electrochemiluminescence aptasensors[J].Biosens Bioelectron, 2018,114: 44-51.
[43] MA N, ZHANG T, YAN T, et al.Novel electrochemical immunosensor for sensitive monitoring of cardiac troponin I using antigen-response cargo released from mesoporous Fe3O4[J].Biosens Bioelectron, 2019,143: 111608.