自20世纪70年代Brånemark提出“骨结合”的理论后,纯钛及钛合金因其良好的生物相容性和力学性能,成为应用最为广泛的牙科种植体材料,以工业纯钛TA3及Ti-6Al-4V合金为代表,工业纯钛TA3的抗腐蚀性能较低,强度较高,Ti-6Al-4V合金的强度较高,但抗腐蚀性能较低。虽然钛是一种活泼的金属,其表面暴露在空气中就能形成以TiO2为主要成分的氧化膜,以保护其内部金属进一步被腐蚀,但是在种植手术及种植体使用过程中,种植体均会受到外力,且长期处于口腔这个不稳定的环境中,磨损和腐蚀均会引起的口腔内牙种植体材料的降解,磨损是种植体表面机械或物理形式的降解,主要产生金属颗粒;而腐蚀是化学或电化学形式的降解,主要产生可溶性金属离子[1]。
随着种植技术的普及,越来越多的年轻缺牙患者接受了种植修复治疗,种植体将在患者体内与组织长期甚至终生接触并行使功能,这对钛或钛合金种植体的抗腐蚀性能及耐磨性能提出了很高的要求。骨结合的种植体可能释放金属离子或颗粒,并在人体远端分布,对生物体具有潜在影响。因此,本文对牙种植体释放金属离子和颗粒现象的研究进展做一综述,希望对于种植体加工技术及种植临床操作的改进提供理论依据。
1 发现及分布
近些年来,多项临床检测实验均表明钛及钛合金种植体会在人体中释放金属离子和颗粒。Olmedo等[2]对150例牙种植体覆盖螺丝旁口腔黏膜进行活检,发现其中40%的样本中存在金属颗粒与吞噬金属颗粒的免疫细胞。He等[3]比较了下颌植入种植体的患者与未接受种植治疗人群,发现在相同解剖位置,种植患者骨内Ti离子含量显著高于对照组。
钛及钛合金种植体释放的金属离子或颗粒多分布在种植体周围组织中,但也有学者在实验动物体内发现其也可分布至远端组织器官中,这一现象引起了广泛关注。在种植体周围,健康或种植体周炎的组织中,检出的Ti颗粒尺寸为100nm~54μm,且在邻近种植体的组织内,其密度更高[4]。Sarmiento-Gonz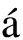 lez等[5]检测了种植手术后大鼠各脏器中钛含量,发现均有所增高,且Ti离子没有靶向器官,TiO2颗粒更易在肺部聚集。Meningaud等[6]应用X射线能量色散荧光分析技术检测到种植患者指甲中存在钛元素,而对照人群的指甲中未发现钛元素。除了牙种植体,对于接受人工膝关节或髋关节置换患者,Ti离子和颗粒也存在于新形成的骨小梁和周围血管中,甚至分布于肝、脾和腹部淋巴结中[7]。
lez等[5]检测了种植手术后大鼠各脏器中钛含量,发现均有所增高,且Ti离子没有靶向器官,TiO2颗粒更易在肺部聚集。Meningaud等[6]应用X射线能量色散荧光分析技术检测到种植患者指甲中存在钛元素,而对照人群的指甲中未发现钛元素。除了牙种植体,对于接受人工膝关节或髋关节置换患者,Ti离子和颗粒也存在于新形成的骨小梁和周围血管中,甚至分布于肝、脾和腹部淋巴结中[7]。
2 影响牙种植体金属颗粒和离子释放的因素
在复杂的口腔环境中,许多因素影响着牙种植体金属颗粒和离子的释放。其中规范种植手术操作、减小基台种植体之间动度、优化基台-种植体连接方式、减少种植体周围菌斑附着、避免种植体周围形成高糖、低pH值的微环境等因素对均减少牙种植体金属颗粒及离子的释放具有显著意义,下文将分别详细介绍。
2.1 影响牙种植体耐磨性的因素
磨损是种植体表面机械或物理形式的降解,主要产生金属颗粒。牙种植体可能因植入过程中扭矩过大、骨密度较高、金属氧化膜被破坏、冲洗不充分等原因,产生较多金属颗粒并残留在周围组织中[8]。Deppe等[9]发现种植体在植入过程中会发生表面损伤,脱落的金属颗粒多集中在螺纹顶端。
种植义齿行使功能时基台-种植体界面会产生微动,引起种植体磨损,释放金属颗粒[10]。Klotz等[11]比较了氧化锆及钛合金的上部结构,发现前者基台-种植体界面因磨损导致种植体产生的金属颗粒更多。这可能与氧化锆较高的机械强度有关。另外,Blum等[12]证明当基台与种植体之间存在微间隙时,种植体与基台间的微动摩擦加剧,导致种植体金属颗粒释放增加。Alrabeah等[13]比较了多种基台-种植体连接方式,发现内连接设计及平台转移设计可以显著减少基台-种植体界面金属颗粒的脱落。
2.2 影响牙种植体抗腐蚀性的因素
腐蚀是种植体表面化学或电化学形式的降解,主要产生可溶性金属离子。种植体表面改性技术、上部结构的材料、生物膜菌斑的定植、氟化物的使用及全身状况等因素均会影响种植体的耐腐蚀性能,造成金属离子释放增加。
增加种植体表面粗糙度可以增加细胞的定植,促进骨结合,但可能会降低种植体抗腐蚀性能,目前有多种表面改性技术被用于提升种植体的骨结合能力,这些方法对抗腐蚀性能的影响程度不一。Díaz等[14]比较了5种种植体表面处理技术对抗腐蚀性能的影响,包括2种酸蚀技术、酸蚀+阳极氧化、喷砂酸蚀、机械加工,发现经过酸蚀+阳极氧化处理的纯钛种植体抗腐蚀性最强。Messer等[15]发现,在炎症环境及高血糖条件下,TiUnite®种植体抗腐蚀性能更强。
不同金属在电解质溶液中相互接触时,会发生原电池反应,比较活泼的金属失去电子被氧化,这种腐蚀叫做电化学腐蚀,不同材质的上部结构会引起种植体不同程度的电化学腐蚀。Anwar等[16]和Sikora等[17]发现,无论是采用纯钛还是Ti-6Al-4V种植体,采用氧化锆作为上部结构比采用其他材质的上部结构,对种植体产生的电化学腐蚀更小。
与牙周炎相关的菌群相比,在种植体周炎相关菌群中,变异链球菌的成分显著增高[18]。Sridhar等[19]在体外实验中发现变异链球菌的定植会让种植体周围持续处于酸性环境,加速其表面的腐蚀。Siddiqui等[20]亦发现变异链球菌可使喷砂酸蚀处理的Ti及TiZr种植体表面出现局部腐蚀的现象。另外,Yu等[21]还发现革兰氏阴性菌的脂多糖可以促进钛种植体表面的腐蚀。近年来,研究证明在患有种植体周炎的种植体龈沟液及龈下生物膜中,钛离子浓度比健康种植体的高[4,22],这进一步表明种植体金属离子的析出程度可能与龈下菌斑生物膜有关。
牙膏及漱口水中普遍含有氟化物(0.1%~0.15%)。Roselino等[23]和Sartori等[24]均用含有氟离子(0.15%)的溶液模拟漱口水的使用频率浸没钛种植体,5年后发现其表面有点蚀现象。
Messer等[25]将种植体置于含有红细胞、脂多糖、高糖的单核细胞培养液中,证明了炎症应激和高血糖可增加钛种植体的腐蚀程度。此外,Tamam等[26]还将种植体置于不同pH值及糖浓度的Ringer’s溶液中,发现在低pH值和高糖的条件下,钛种植体的腐蚀风险较大。
3 对生物体的影响
3.1 细胞水平
2018年第五届EAO会议共识提出,Ti离子/颗粒或TiO2颗粒对成骨细胞、破骨细胞、巨噬细胞等细胞功能都有一定负面影响[27]。
3.1.1 成骨细胞和破骨细胞 Ribeiro等[28]发现Ti离子蛋白质聚合物和TiO2颗粒会被成骨细胞内化,诱导其释放IL-6、COX-2等细胞因子,导致成骨细胞黏附能力和迁移分化能力下降,凋亡增加,且这些变化均有浓度依赖性,Ti离子蛋白质聚合物比TiO2颗粒表现出更高的生物活性。另外,Vallés等[29]发现共培养的巨噬细胞与成骨细胞在Ti颗粒或TiO2颗粒存在的环境下,释放更多的IL-6,较少的骨保护素,由此激活破骨细胞的增殖与分化。
3.1.2 免疫细胞 Kumazawa等[30]发现,Ti颗粒和V颗粒会使中性粒细胞释放过多的过氧化氢离子,且颗粒越小这种影响越显著。Vallés等[31]发现巨噬细胞细胞能有效地内化Ti颗粒或TiO2颗粒,分泌较多的TNF-α、IL-6和IL-1β,可能加剧局部炎症反应,且Ti颗粒产生的影响更大。
3.1.3 成纤维细胞和内皮细胞 Tsaryk等[32]发现内皮细胞在直接接触Ti-6Al-4V后,会产生较强的氧化应激反应,细胞活力受损。Okazaki等[33]发现高浓度的Al和V颗粒会降低成纤维细胞和成骨细胞的增殖率,而Ti颗粒无明显影响。
3.1.4 遗传毒性 过量V化合物可导致细胞有丝分裂异常,细胞形态改变;过量Al离子可促使细胞产生超氧自由基,可能导致基因突变[34-35]。但目前尚无研究直接证实种植体析出的V和Al离子具有遗传毒性。Ribeiro等[36]在雌性小鼠生殖细胞的培养液中加入多种种植体洗脱液,均未发现基因损伤和遗传毒性。
3.2 组织水平
已有多项临床证据表明种植体释放的金属离子或颗粒与组织过敏反应及种植体周围炎可能存在相关关系,但缺乏临床统计学分析证明这种相关性。
3.2.1 过敏反应 释放的Ti离子/颗粒可能与生物分子(如天然蛋白质)结合,形成蛋白质-金属复合物,从而具有免疫原性,引发Ⅳ型过敏反应,表现为无法解释的疼痛、皮疹、湿疹、伤口不愈或无菌性骨髓炎[37]。Sicilia等[38]对1500位种植患者行皮肤过敏试验,发现9人对钛元素过敏,其中5例出现种植体失败,4例出现过敏症状。
3.2.2 种植体周炎 Ti离子/颗粒可能会刺激免疫反应,引起种植体周炎[39]。Rodrigues等[40]检测了因种植体周炎取出的种植体,发现其表面均有腐蚀现象。Fretwurst等[41]在种植体周炎的失败种植体周围,刮取软硬组织,发现巨噬细胞及淋巴细胞的数量与Ti离子浓度呈正相关。但此两者间的因果关系尚无定论。
4 材料及表面处理技术的改进
4.1 新型材料
为了提升种植体表面抗腐蚀及耐磨性能,学者们不断探索着新型钛合金材料。Wang等[42]研究发现,具有α-Ti+Ti2Cu显微结构的Ti-5Cu合金与纯钛种植体相比,不仅具有良好的抗腐蚀、抗菌性性能,还具有合适强度和延展性。Xu等[43]发现由金属粉末注射成型技术制成的Ti-12Mo合金因其可以形成较厚的TiO2-MoO3氧化膜,故其抗腐蚀性能优于纯钛种植体。Zhang等[44]认为经过热氧化处理的Zr-20Nb-3Ti合金具有更优的抗腐蚀及耐磨性能。以上3种合金均具有较好的抗腐蚀及耐磨性能,目前正在深入研究其生物相容性及骨结合能力。另外,新型质轻高分子聚合材料聚醚醚酮因也其具有耐腐蚀、抗磨损、无细胞毒性的特点引起了广泛关注[45]。
4.2 表面处理技术
因TiO2氧化膜具有良好的骨结合性能,近年来,研究方向大多为修饰或增强种植体表面氧化膜,以提升种植体表面抗腐蚀性能。Visentin等[46]用低压有机化学气相沉积法在种植体表面形成TiO2膜。Marques等[47]发现在微弧氧化层中加入了一定比例的Ca/P。也有学者通过增加表面涂层来阻止种植体释放金属离子或颗粒。Zhang等[48]采用磁控溅射法在Ti种植体表面沉积TaN层,以提升种植体表面的抗腐蚀性和耐磨性能。Romanov等[49]用电爆技术在种植体表面形成Ti-Zr涂层,提高了种植体的耐磨性。但经以上两种方法处理后,涂层在牙种植体植入过程中的稳定性及其骨结合性能还有待研究。
5 展 望
综上所述,牙种植体在植入及长期行使功能的过程中,受多种口腔及全身因素影响,存在释放金属离子和颗粒的现象。这些离子和颗粒对体内多种细胞功能存在负面影响,影响的大小与离子浓度及颗粒尺寸有相关性。此外,释放的金属离子和颗粒可能导致局部过敏反应,且与种植体周炎存在相关关系。目前,种植牙已成为临床缺牙患者修复治疗的常规方案,从事口腔种植工作的医师应进一步规范临床操作技术,在术前仔细评估患者条件并积极规避不利影响因素,以降低种植体金属离子和颗粒释放的风险。此外,积极探索种植体新型材料及表面处理技术,不断提高其耐磨性及抗腐蚀性,以进一步减少种植治疗相关并发症,是口腔种植体材料发展的研究热点及趋势。
[1] SHEMTOV-YONA K, RITTEL D, LEVIN L, et al.The effect of oral-like environment on dental implants’ fatigue performance[J].Clin Oral Implants Res, 2014,25(2): e166-e170.
[2] OLMEDO D G, PAPARELLA M L, SPIELBERG M, et al.Oral mucosa tissue response to titanium cover screws[J].J Periodontol, 2012,83(8): 973-980.
[3] HE X L, REICHL F X, WANG Y, et al.Analysis of titanium and other metals in human jawbones with dental implants—A case series study[J].Dent Mater, 2016,32(8): 1042-1051.
[4] SU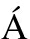 REZ-L
REZ-L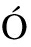 PEZ DEL AMO F, GARAICOA-PAZMI
PEZ DEL AMO F, GARAICOA-PAZMI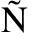 O C, FRETWURST T, et al.Dental implants-associated release of titanium particles: a systematic review[J].Clin Oral Implants Res, 2018,29(11): 1085-1100.
O C, FRETWURST T, et al.Dental implants-associated release of titanium particles: a systematic review[J].Clin Oral Implants Res, 2018,29(11): 1085-1100.
[5] SARMIENTO-GONZ LEZ A, ENCINAR J R, MARCHANTE-GAY
LEZ A, ENCINAR J R, MARCHANTE-GAY N J M, et al.Titanium levels in the organs and blood of rats with a titanium implant, in the absence of wear, as determined by double-focusing ICP-MS[J].Anal Bioanal Chem, 2009,393(1):335-343.
N J M, et al.Titanium levels in the organs and blood of rats with a titanium implant, in the absence of wear, as determined by double-focusing ICP-MS[J].Anal Bioanal Chem, 2009,393(1):335-343.
[6] MENINGAUD J P, POUPON J, BERTRAND J C, et al.Dynamic study about metal release from titanium miniplates in maxillofacial surgery[J].Int J Oral Maxillofac Surg, 2001,30(3): 185-188.
[7] URBAN R M, JACOBS J J, TOMLINSON M J, et al.Dissemination of wear particles to the liver, spleen, and abdominal lymph nodes of patients with hip or knee replacement[J].J Bone Joint Surg Am, 2000,82(4): 457-477.
[8] DELGADO-RUIZ R, ROMANOS G.Potential causes of titanium particle and Ion release in implant dentistry: a systematic review[J].Int J Mol Sci, 2018,19(11): E3585.
[9] DEPPE H, GRÜNBERG C, THOMAS M, et al.Surface morphology analysis of dental implants following insertion into bone using scanning Electron microscopy: a pilot study[J].Clin Oral Implants Res, 2015,26(11): 1261-1266.
[10] REVATHI A, BORR S A D, MU
S A D, MU OZ A I, et al.Degradation mechanisms and future challenges of titanium and its alloys for dental implant applications in oral environment[J].Mater Sci Eng C Mater Biol Appl, 2017,76: 1354-1368.
OZ A I, et al.Degradation mechanisms and future challenges of titanium and its alloys for dental implant applications in oral environment[J].Mater Sci Eng C Mater Biol Appl, 2017,76: 1354-1368.
[11] KLOTZ M W, TAYLOR T D, GOLDBERG A J.Wear at the titanium-zirconia implant-abutment interface: a pilot study[J].Int J Oral Maxillofac Implants, 2011,26(5): 970-975.
[12] BLUM K, WIEST W, FELLA C, et al.Fatigue induced changes in conical implant-abutment connections[J].Dent Mater, 2015,31(11): 1415-1426.
[13] ALRABEAH G O, KNOWLES J C, PETRIDIS H.The effect of platform switching on the levels of metal Ion release from different implant-abutment couples[J].Int J Oral Sci, 2016,8(2): 117-125.
[14] D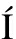 AZ I, PACHA-OLIVENZA M
AZ I, PACHA-OLIVENZA M 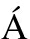 , TEJERO R, et al.Corrosion behavior of surface modifications on titanium dental implant.In situ bacteria monitoring by electrochemical techniques[J].J Biomed Mater Res Part B Appl Biomater, 2018,106(3): 997-1009.
, TEJERO R, et al.Corrosion behavior of surface modifications on titanium dental implant.In situ bacteria monitoring by electrochemical techniques[J].J Biomed Mater Res Part B Appl Biomater, 2018,106(3): 997-1009.
[15] MESSER R L, SETA F, MICKALONIS J, et al.Corrosion of phosphate-enriched titanium oxide surface dental implants(TiUnite)under in vitro inflammatory and hyperglycemic conditions[J].J Biomed Mater Res Part B Appl Biomater, 2010,92(2): 525-534.
[16] ANWAR E M, KHEIRALLA L S, TAMMAM R H.Effect of fluoride on the corrosion behavior of Ti and Ti6Al4V dental implants coupled with different superstructures[J].J Oral Implantol, 2011,37(3): 309-317.
[17] SIKORA C L, ALFARO M F, YUAN J C, et al.Wear and corrosion interactions at the titanium/zirconia interface: dental implant application[J].J Prosthodont, 2018,27(9): 842-852.
[18] KUMAR P S, MASON M R, BROOKER M R, et al.Pyrosequencing reveals unique microbial signatures associated with healthy and failing dental implants[J].J Clin Periodontol, 2012,39(5): 425-433.
[19] SRIDHAR S, ABIDI Z, WILSON T G Jr, et al.In vitro evaluation of the effects of multiple oral factors on dental implants surfaces[J].J Oral Implantol, 2016,42(3): 248-257.
[20] SIDDIQUI D A, GUIDA L, SRIDHAR S, et al.Evaluation of oral microbial corrosion on the surface degradation of dental implant materials[J].J Periodontol, 2019,90(1): 72-81.
[21] YU F, ADDISON O, BAKER S J, et al.Lipopolysaccharide inhibits or accelerates biomedical titanium corrosion depending on environmental acidity[J].Int J Oral Sci, 2015,7(3): 179-186.
[22] SAFIOTI L M, KOTSAKIS G A, POZHITKOV A E, et al.Increased levels of dissolved titanium are associated with peri-implantitis—A cross-sectional study[J].J Periodontol, 2017,88(5): 436-442.
[23] ROSELINO RIBEIRO A L, NORIEGA J R, DAMETTO F R, et al.Compressive fatigue in titanium dental implants submitted to fluoride ions action[J].J Appl Oral Sci, 2007,15(4): 299-304.
[24] SARTORI R, CORREA C B, MARCANTONIO E Jr, et al.Influence of a fluoridated medium with different pHs on commercially pure titanium-based implants[J].J Prosthodont, 2009,18(2): 130-134.
[25] MESSER R L, TACKAS G, MICKALONIS J, et al.Corrosion of machined titanium dental implants under inflammatory conditions[J].J Biomed Mater Res Part B Appl Biomater, 2009,88(2): 474-481.
[26] TAMAM E, TURKYILMAZ I.Effects of pH and elevated glucose levels on the electrochemical behavior of dental implants[J].J Oral Implantol, 2014,40(2): 153-159.
[27] SCHLIEPHAKE H, SICILIA A, NAWAS B A, et al.Drugs and diseases: Summary and consensus statements of group 1.The 5th EAO Consensus Conference 2018[J].Clin Oral Implants Res, 2018,29(Suppl 18): 93-99.
[28] RIBEIRO A R, GEMINI-PIPERNI S, TRAVASSOS R, et al.Trojan-like internalization of anatase titanium dioxide nanoparticles by human osteoblast cells[J].Sci Rep, 2016,6: 23615.
[29] VALLÉS G, GONZ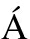 LEZ-MELENDI P, SALDA
LEZ-MELENDI P, SALDA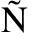 A L, et al.Rutile and titanium particles differentially affect the production of osteoblastic local factors[J].J Biomed Mater Res A, 2008,84(2): 324-336.
A L, et al.Rutile and titanium particles differentially affect the production of osteoblastic local factors[J].J Biomed Mater Res A, 2008,84(2): 324-336.
[30] KUMAZAWA R, WATARI F, TAKASHI N, et al.Effects of Ti ions and particles on neutrophil function and morphology[J].Biomaterials, 2002,23(17): 3757-3764.
[31] VALLÉS G, GONZ LEZ-MELENDI P, GONZ
LEZ-MELENDI P, GONZ LEZ-CARRASCO J L, et al.Differential inflammatory macrophage response to rutile and titanium particles[J].Biomaterials, 2006,27(30): 5199-5211.
LEZ-CARRASCO J L, et al.Differential inflammatory macrophage response to rutile and titanium particles[J].Biomaterials, 2006,27(30): 5199-5211.
[32] TSARYK R, KALBACOVA M, HEMPEL U, et al.Response of human endothelial cells to oxidative stress on Ti6Al4V alloy[J].Biomaterials, 2007,28(5): 806-813.
[33] OKAZAKI Y, RAO S, ASAO S, et al.Effects of Ti, Al and V concentrations on cell viability[J].Mater Trans, JIM, 1998,39(10): 1053-1062.
[34] ABOU-SEIF M A M.Oxidative stress of vanadium-mediated oxygen free radical generation stimulated by aluminium on human erythrocytes[J].Ann Clin Biochem, 1998,35(2): 254-260.
[35] CORTIZO A M, S LICE V C, VESCINA C M, et al.Proliferative and morphological changes induced by vanadium compounds on Swiss 3T3 fibroblasts[J].Biometals, 1997,10(2): 127-133.
LICE V C, VESCINA C M, et al.Proliferative and morphological changes induced by vanadium compounds on Swiss 3T3 fibroblasts[J].Biometals, 1997,10(2): 127-133.
[36] RIBEIRO D A, MATSUMOTO M A, PADOVAN L E, et al.Genotoxicity of corrosion eluates obtained from endosseous implants[J].Implant Dent, 2007,16(1): 101-109.
[37] HALLAB N, MERRITT K, JACOBS J J.Metal sensitivity in patients with orthopaedic implants[J].J Bone Joint Surg Am, 2001,83(3): 428-436.
[38] SICILIA A, CUESTA S, COMA G, et al.Titanium allergy in dental implant patients: a clinical study on 1500 consecutive patients[J].Clin Oral Implants Res, 2008,19(8): 823-835.
[39] APAZA-BEDOYA K, TARCE M, BENFATTI C A M, et al.Synergistic interactions between corrosion and wear at titanium-based dental implant connections: a scoping review[J].J Periodont Res, 2017,52(6): 946-954.
[40] RODRIGUES D C, VALDERRAMA P, WILSON T G, et al.Titanium corrosion mechanisms in the oral environment: a retrieval study[J].Materials(Basel), 2013,6(11): 5258-5274.
[41] FRETWURST T, BUZANICH G, NAHLES S, et al.Metal elements in tissue with dental peri-implantitis: a pilot study[J].Clin Oral Implants Res, 2016,27(9): 1178-1186.
[42] WANG J W, ZHANG S Y, SUN Z Q, et al.Optimization of mechanical property, antibacterial property and corrosion resistance of Ti-Cu alloy for dental implant[J].J Mater Sci Technol, 2019,35(10): 2336-2344.
[43] XU W, LU X, WANG L N, et al.Mechanical properties, in vitro corrosion resistance and biocompatibility of metal injection molded Ti-12 Mo alloy for dental applications[J].J Mech Behav Biomed Mater, 2018,88: 534-547.
[44] ZHANG J F, GAN X X, TANG H Q, et al.Enhancement of wear and corrosion resistance of low Modulus β-type Zr-20Nb-xTi(x=0, 3)dental alloys through thermal oxidation treatment[J].Mater Sci Eng C Mater Biol Appl, 2017,76: 260-268.
[45] 李启期,魏杰,周聪颖,等.纳米氟磷灰石/聚醚醚酮种植体成骨效能研究[J].同济大学学报(医学版),2013,34(1): 40-44.
[46] VISENTIN F, GALENDA A, FABRIZIO M, et al.Assessment of synergistic effects of LP-MOCVD TiO2 and Ti surface finish for dental implant purposes[J].Appl Surf Sci, 2019,490: 568-579.
[47] MARQUES I D S V, ALFARO M F, CRUZ N C D, et al.Tribocorrosion behavior of biofunctional titanium oxide films produced by micro-arc oxidation: synergism and mechanisms[J].J Mech Behav Biomed Mater, 2016,60: 8-21.
[48] ZHANG Y F, ZHENG Y F, LI Y L, et al.Tantalum nitride-decorated titanium with enhanced resistance to microbiologically induced corrosion and mechanical property for dental application[J].PLoS One, 2015,10(6): e0130774.
[49] ROMANOV D A, SOSNIN K V, GROMOV V E, et al.Titanium-zirconium coatings formed on the titanium implant surface by the electroexplosive method[J].Mater Lett, 2019,242: 79-82.