肺炎支原体肺炎(mycoplasma pneumoniae pne-umonia, MPP)是儿童时期最常见的社区获得性肺炎之一,约占社区获得性肺炎(community-acquired pneumonia, CAP)的10%~40%[1]。感染后可呈不同临床表现,轻者可仅表现为咳嗽,肺部体征轻微,重者可出现持续高热,剧烈咳嗽,肺部啰音迁延不愈,并可出现胸腔积液、肺不张、坏死性肺炎等重症肺炎表现,并可累及其他肺外系统。随着支原体耐药株的不断增加,肺炎支原体感染呈严重化趋势,难治性支原体肺炎(refractory mycoplasma pneumoniae pneumonia, RMPP)逐渐增多,给患者带来了身心和经济上的双重打击。本研究拟采用回顾性分析,对293例肺炎支原体感染儿童的临床资料及常用炎症指标进行分析,探讨炎症指标与肺炎支原体感染性肺炎中难治性肺炎的相关性,从而指导临床进行早期干预。
1 资料与方法
1.1 一般资料
以2018年12月至2019年11月在同济大学附属东方医院南院儿科住院的293例MPP患儿为研究对象。诊断标准依照《儿童社区获得性肺炎管理指南(2013修订)》(下文简称2013指南)[2]。MPP诊断标准: (1) 临床表现有发热、咳嗽等;(2) 胸部影像学肺炎改变;(3) 病原学: 单份血清MP—IgM明显升高≥1∶160,鼻咽拭子检测支原体DNA阳性。难治性支原体肺炎(refractory mycoplasma pneumoniae pneumonia, RMPP)诊断标准: 经过大环内酯类抗菌药物正规治疗7d以上,临床症状加重,持续发热,肺部影像加重者。根据临床表现将支原体肺炎分为普通支原体肺炎(general mycoplasma pneumoniae pneumonia, GMPP)组和RMPP组。依据影像学描述分为4级。1级: 双肺纹理增多增粗模糊;2级: 在1级的基础上可见斑点状渗出;3级: 双肺可见斑片状渗出;4级: 一侧或双侧肺野可见大片状渗出,或伴肺不张、肺实变、胸膜反应者。其中1~3级归为非大叶性肺炎组,4级为大叶性肺炎组。
1.2 方法
收集患儿临床资料,包括性别、年龄、发病季节、发热时间、咳嗽时间等。所有患儿均于入院前给予完善影像学检查,入院第2天进行血常规、C反应蛋白(C-reactive protein, CRP)、肺炎支原体抗体、乳酸脱氢酶(lactate dehydrogenase, LDH)、降钙素原(procalcitonin, PCT)、D-二聚体(D-dimer, DD)、白细胞介素-6(interleukin-6, IL-6)、前白蛋白(prealbumin, PA)、鼻咽拭子支原体DNA及呼吸道九联病原菌等检测。
肺炎支原体抗体检测: 于清晨空腹采集静脉血2mL,离心力1000×g,离心15min后,取上清液,-20℃ 冰箱保存。采用颗粒凝集法检测支原体抗体水平,试剂盒来自于赛乐迪亚公司,严格按照说明书步骤进行。支原体DNA的检测: 取患儿咽拭子标本,采用PCR的方法,检测支原体DNA,试剂盒来自于Liferive公司的试剂盒,试验方法严格按照试剂盒操作说明。
1.3 统计学处理
数据采用SPSS 22.0软件进行统计分析,计量资料服从正态分布时采用![]() 表示,不服从正态分布的采用中位数和四分位数表示,计数资料采用频数或者率表示。两组计量资料比较服从正态分布的采用两个独立样本T检验,不服从正态分布的采用秩和检验;计数资料比较采用χ2检验;多因素分析采用二元Logistic回归分析;诊断预测效果分析采用ROC曲线分析。P<0.05为差异有统计学意义。
表示,不服从正态分布的采用中位数和四分位数表示,计数资料采用频数或者率表示。两组计量资料比较服从正态分布的采用两个独立样本T检验,不服从正态分布的采用秩和检验;计数资料比较采用χ2检验;多因素分析采用二元Logistic回归分析;诊断预测效果分析采用ROC曲线分析。P<0.05为差异有统计学意义。
2 结 果
2.1 一般资料
2018年12月至2019年11月在本院儿科住院治疗的患儿中肺炎共707例,经病原学诊断为支原体感染的共计293例。根据就诊时间进行季节划分,春季(3~5月)有56例、夏季(6~8月)87例、秋季(9~11月)102例、冬季(12~2月)48例。不同季节就诊患者中支原体感染所占比例情况如图1所示。293例患者的一般情况见表1。其中男性有141例,占比为48.12%;女性有152例,占比为51.88%。年龄最大者为15岁,最小者为6个月,平均年龄为(5.17±2.63)岁。293例支原体感染患者中有41例合并其他细菌病毒感染,占比为13.99%,其中合并细菌感染7例、合并病毒感染34例。影像学的严重程度分类显示1级有33例,占比为11.26%;2级有130例,占比为44.37%;3级有81例,占比为27.65%;4级有49例,占比为17.72%,见表1。
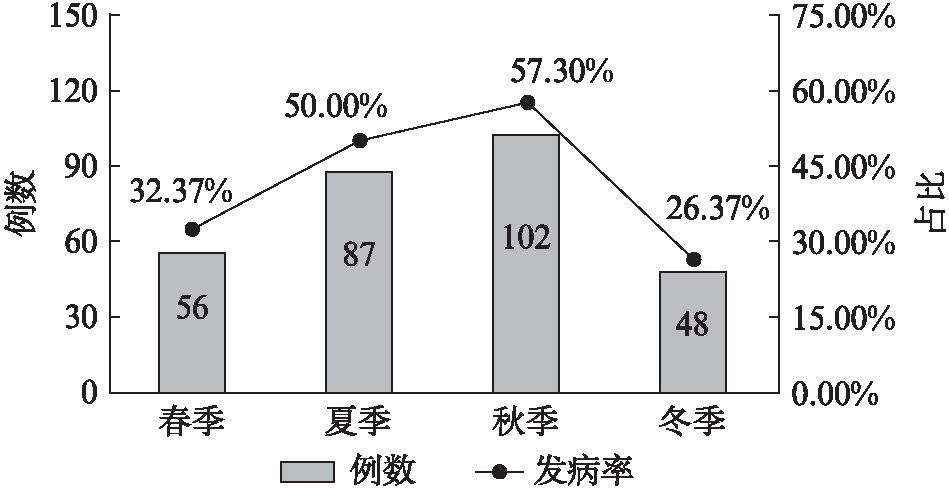
图1 不同季节肺炎患者中支原体感染比例情况
Fig.1 The proportion of MP infection in patients with pneumonia in different seasons
2.2 影像学的严重程度影响因素分析
根据患者的影像学的严重程度,分析患者一般情况及生化检查对影像学严重程度的影响。4级患者的年龄、入院前发热时间、CRP、LDH、D-二聚体、降钙素原、IL-6均高于1~3级患者,差异均有统计学意义(P均<0.05)。4级患者的PA水平、入院前咳嗽时间低于1~3级患者,差异有统计学意义(t=2.919,P=0.004)。不同严重程度患者的性别构成、合并感染情况和白细胞水平差异经比较无统计学意义(P>0.05),见表2。
表1 293例支原体肺炎患者一般情况
Tab.1 General clinic data of 293 cases of MPP

项目n构成比年龄/岁 <110.34% 1~33511.95% 3~510335.15% 5~77425.26% ≥78027.30%性别 男性14148.12% 女性15251.88%发病季节 春季5619.11% 夏季8729.69% 秋季10234.81% 冬季4816.38%合并感染 否25286.01% 病毒3411.60% 细菌72.39%胸片严重程度 1级3311.26% 2级13044.37% 3级8127.65% 4级4916.72%
2.3 难治性支原体肺炎影响因素单因素分析
293例MPP患者中,对门诊及住院期间正规使用大环内酯类抗菌药物正规治疗7d,仍有持续发热、临床症状加重者,考虑为RMPP,共有59例,GMPP 234例,分析比较两组患者间一般情况和炎症指标。RMPP组入院前发热时间、CRP、LDH、DD、降钙素原、IL-6均高于GMPP组,差异有统计学意义(P<0.05)。RMPP组的入院前咳嗽时间和PA水平低于GMPP组,差异均有统计学意义(P<0.05)。但两组患者间的年龄、性别构成、合并感染情况和白细胞水平差异均无统计学意义(P>0.05),见表3。
表2 影像学的严重程度影响因素单因素分析
Tab.2 Univariate analysis of influencing factors of radiographic severity
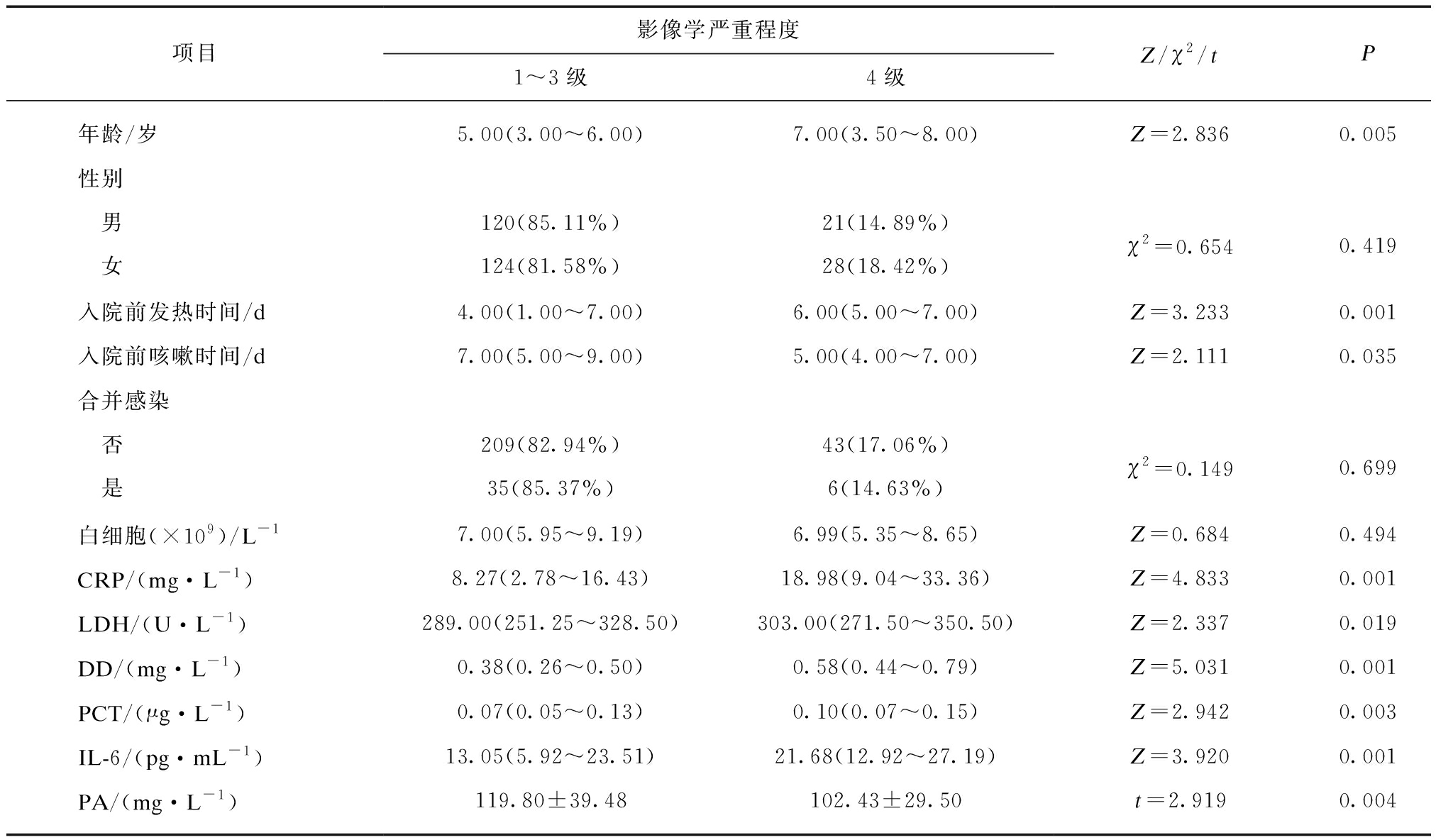
项目影像学严重程度1~3级4级Z/χ2/tP年龄/岁5.00(3.00~6.00)7.00(3.50~8.00)Z=2.8360.005性别 男120(85.11%)21(14.89%) 女124(81.58%)28(18.42%)χ2=0.6540.419入院前发热时间/d4.00(1.00~7.00)6.00(5.00~7.00)Z=3.2330.001入院前咳嗽时间/d7.00(5.00~9.00)5.00(4.00~7.00)Z=2.1110.035合并感染 否209(82.94%)43(17.06%) 是35(85.37%)6(14.63%)χ2=0.1490.699白细胞(×109)/L-17.00(5.95~9.19)6.99(5.35~8.65)Z=0.6840.494CRP/(mg·L-1)8.27(2.78~16.43)18.98(9.04~33.36)Z=4.8330.001LDH/(U·L-1)289.00(251.25~328.50)303.00(271.50~350.50)Z=2.3370.019DD/(mg·L-1)0.38(0.26~0.50)0.58(0.44~0.79)Z=5.0310.001PCT/(μg·L-1)0.07(0.05~0.13)0.10(0.07~0.15)Z=2.9420.003IL-6/(pg·mL-1)13.05(5.92~23.51)21.68(12.92~27.19)Z=3.9200.001PA/(mg·L-1)119.80±39.48102.43±29.50t=2.9190.004
表3 难治性支原体肺炎的影响因素单因素分析
Tab.3 Univariate analysis of influencing factors of RMPP

项目GMPP组RMPP组Z/χ2/tP年龄/岁5.00(3.00~7.00)5.00(3.00~7.00)Z=1.4190.156性别 男115(81.56%)26(18.44%) 女119(78.29%)33(21.71%)χ2=0.4870.485入院前发热时间/d4.00(1.00~7.00)6.00(5.00~7.00)Z=3.7110.001入院前咳嗽时间/d7.00(5.00~10.00)5.00(4.00~7.00)Z=3.0500.002合并感染 否198(78.57%)54(21.43%) 是36(87.80%)5(12.20%)χ2=1.8690.172白细胞(×109)/L-17.07(5.93~9.38)6.72(5.37~8.10)Z=0.6840.494CRP/(mg·L-1)8.11(2.63~16.46)14.00(7.67~32.79)Z=4.8330.001LDH/(U·L-1)288.00(251.00~327.50)311.00(258.00~365.00)Z=2.3370.019DD/(mg·L-1)0.38(0.25~0.51)0.46(0.38~0.78)Z=5.0310.001PCT/(μg·L-1)0.07(0.05~0.11)0.11(0.07~0.19)Z=2.9420.003IL-6/(pg·mL-1)12.07(5.88~22.69)23.16(16.46~31.49)Z=3.9200.001PA/(mg·L-1)122.02±40.0996.58±21.95t=6.5620.001
2.4 难治性支原体肺炎影响因素多因素分析
进一步进行RMPP影响因素的多因素分析,以单因素分析中有意义的因素为自变量,是否为RMPP为因变量(0=“GMPP”,1=“RMPP”),进行逐步Logistic回归。结果显示,IL-6和PA为诊断RMPP的独立影响因素。IL-6越高,考虑RMPP的可能性越大(OR=1.037,95%CI为1.017~1.058);PA越低,考虑RMPP可能性越大(OR=0.984,95%CI为0.972~0.996),见表4。
表4 难治性支原体肺炎影响因素多因素分析
Tab.4 Multivariate analysis of risk factors of RMPP
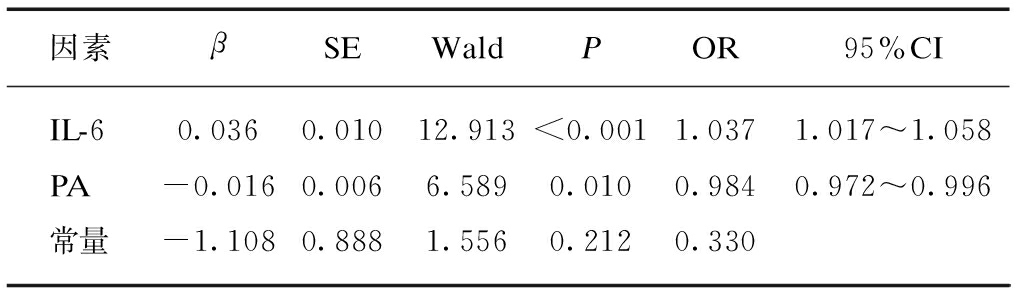
因素βSEWaldPOR95%CIIL-60.0360.01012.913<0.0011.0371.017~1.058PA-0.0160.0066.5890.0100.9840.972~0.996常量-1.1080.8881.5560.2120.330
2.5 相关指标对难治性支原体肺炎的预测效果
采用ROC曲线分析,以RMPP为目标变量,绘制的ROC曲线,如图2所示,各个指标对RMPP的预测效果汇总如表5所示。分析结果显示,对于IL-6,曲线下面积(AUC)为0.745,95%CI为0.683~0.807,差异有统计学意义(P<0.001);当IL-6≥14.455pg/mL预测为RMPP时,此时预测的灵敏度为83.05%,特异度为61.21%。对于PA,AUC为0.703,95%CI为0.634~0.772,差异有统计学意义(P<0.001),当PA≤101.500mg/L预测为RMPP时,此时预测的灵敏度为67.95%,特异度为69.49%。
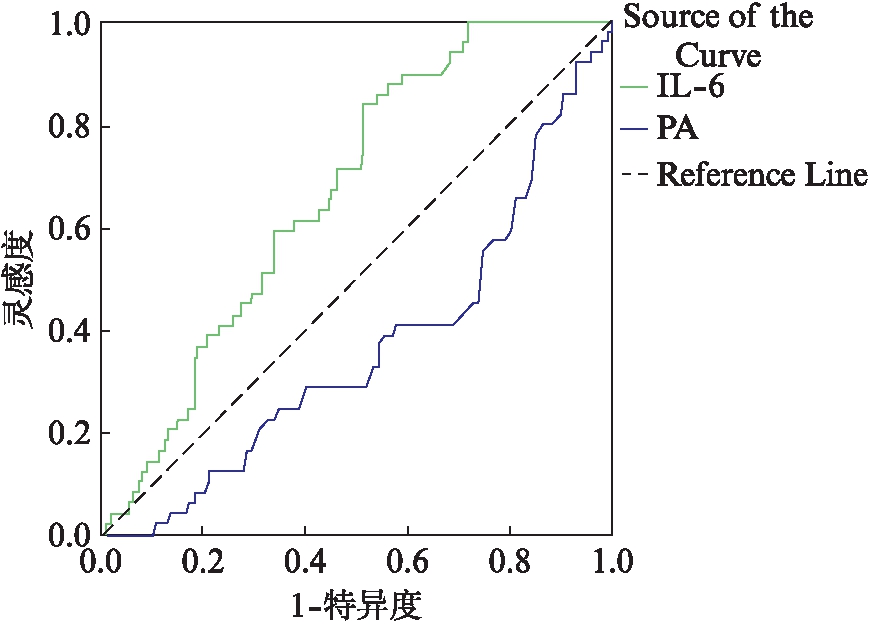
图2 相关指标对难治性支原体肺炎的预测ROC曲线
Fig.2 ROC curve of prediction effect on relevant items of RMPP
表5 相关指标对难治性支原体肺炎预测效果
Tab.5 Prediction effect of relevant indicators on RMPP

指标AUC95%CIP临界值灵敏度特异度IL-60.7450.683~0.807<0.001≥14.455pg·mL-183.05%61.21%PA0.7030.634~0.772<0.001≤101.500mg·L-167.95%69.49%
2.6 影像学的严重程度与难治性支原体肺炎的相关性
GMPP的234例患者中,影像学的表现为4级的有16例,占比为6.84%,RMPP的59例患者中,影像学的表现为4级的有33例,占比为55.93%。RMPP影像学的严重程度高于GMPP组,差异有统计学意义(χ2=81.549,P<0.001),见表6。
表6 胸片严重程度与不同支原体肺炎相关性
Tab.6 Correlation between severity in chest radiograph and different types of MPP
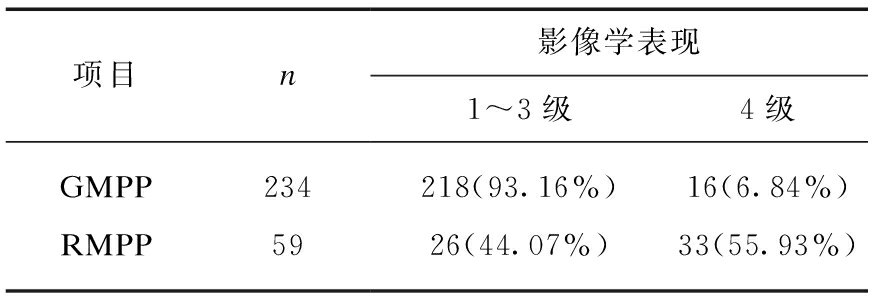
项目n影像学表现1~3级4级GMPP234218(93.16%)16(6.84%)RMPP5926(44.07%)33(55.93%)
3 讨 论
肺炎支原体感染常见于学龄前期和学龄期儿童[3],全年均可散发,北方以秋冬季为发病高峰[4],南方以夏秋季为发病高峰[5],每隔3~7年会有1次周期性社区流行。在北京儿童呼吸道感染流行病调查[4]发现,每年肺炎支原体感染率存在很大的差异,2007年(27.31%)和2012年(28.09%)明显高于其他的年份。2015年上海某医院采用血清呼吸道病原体9联检方法发现住院急性呼吸道感染患儿中支原体感染比例达35.1%[6]。在肺炎支原体流行年,高达40%的CAP可由肺炎支原体感染所致[7]。本研究发现,肺炎支原体感染主要见于学龄期和学龄前期儿童,<3岁儿童患病构成比只有12.29%,这可能与婴幼儿产生抗体的免疫应答低有关。在上海地区发病高峰季节为夏秋季,2019年夏秋季在我院住院的CAP患儿中肺炎支原体感染率分别高达到50%、57.7%,2019年是肺炎支原体感染的流行年。
支原体肺炎影像学的表现各异,可表现为支气管肺炎、间质性肺炎、节段性或大叶性肺炎等,重者可伴有肺不张、胸腔积液、坏死性肺炎、肺脓肿等[8]。各年龄段儿童表现也不同,婴幼儿以间质性肺炎表现为主,年长儿以大叶性肺炎表现为主[9]。本研究根据MPP影像学的表现分成4级,1~3级归于非大叶性肺炎组,两组比较发现,大叶性肺炎组平均年龄7岁,明显大于非大叶性肺炎组,发热时间及各炎症指标明显高于非大叶性肺炎组。但非大叶性肺炎组入院前咳嗽时间反而较大叶性肺炎更长,咳嗽是由来自鼻、咽喉、支气管、胸膜等感受器的刺激传入延髓咳嗽反射中枢引起,考虑大叶性肺炎早期为充血期,主要是肺泡壁炎症,未累及支气管黏膜,故导致咳嗽症状反而不明显。Zhou等[10]发现临床上耐药株感染的患儿胸部影像学的改变更严重,住院时间延长且更易伴有肺外并发症。本研究亦提示胸片的严重程度和病情严重程度密切相关,大叶性肺炎更容易发生RMPP。
支原体感染致病机制尚未明确,目前认为,支原体可以通过黏附在呼吸道上皮产生细胞毒效应而造成直接损伤,也可以通过免疫机制导致肺部炎性损伤及肺外表现[11]。随着支原体感染发病率升高及大环内酯类的广泛使用,支原体耐药株也不断出现,免疫机制导致的肺部炎性损伤更为明显,本研究统计数据显示,RMPP在MPP中发生率达到20%。RMPP病情进展快,常在短时间内出现多种并发症,包括累及多个肺叶、合并肺不张、胸腔积液,部分病例可发展成坏死性肺炎、闭塞性细支气管炎等[12]。而根据指南[2],大环内酯类抗菌药物正规治疗7d及以上,临床症状加重者,才考虑RMPP。当诊断RMPP时,机体已经发生了不可逆转的病理改变,已错失了最佳治疗时期。Choi等[13]认为,MPP经正规抗感染治疗72h仍有发热者即考虑RMPP,给予激素治疗后,临床取得较好效果。多项研究将糖皮质激素用于治疗RMPP,取得加速退热、缓解症状、缩短住院时间等效果[14-15]。因此,在临床治疗中,早期识别RMPP,及早采取相应的干预措施,具有重要的临床意义。
2013指南认为血清LDH>410IU/L,CRP>40mg/L 是RMPP的高危因素[2]。国内外多项研究旨在发现引起RMPP的高危因素。RMPP与机体免疫功能紊乱密切相关,包括细胞免疫和体液免疫功能紊乱,Th1、Th2细胞比例失衡、T细胞亚群功能紊乱、多种细胞因子失衡等。蓝引乐等[16]发现RMPP患儿肺泡灌洗液(broncho alveolar lavage fluid, BALF)中IL-4、IL-6、IL-8、IL-10、IFN-7均高于对照组,说明MP感染可引起肺部广泛的细胞因子升高。本研究选取的PA、LDH、PCT、DD、IL-6等都是临床上常用的非特异性炎症反应指标。研究发现,RMPP组CRP、LDH、DD、IL-6的水平均高于GMPP组,而PA水平低于GMPP组,差异均有统计学意义。因为不同分组合并感染情况各组间无统计学差异,故可排除合并感染对各炎症指标的影响。LDH是一种糖酵解酶,当组织被破坏时释放入血液中,是判断病情严重程度和预后的可靠指标。PCT在正常人体内水平很低,当机体发生细菌感染时,PCT急剧升高,且保持时间较长,是判断细菌感染及治疗效果的观察指标。DD是纤维蛋白降解产物,与脓毒症密切相关,是脓毒症的重要预后因素。其中IL-6和PA是发生RMPP的独立危险因素。IL-6是由T淋巴细胞、巨噬细胞和内皮细胞等分泌的细胞因子,当外源性病原体被机体免疫细胞识别后,通过产生IL-6等促炎因子来清除病原微生物,以促进组织修复,同时产生大量IL-10,下调炎症反应[17]。当组织免疫损伤严重,发生较强炎症反应时,可产生大量IL-6[18]。已有研究提出,RMPP患儿血中IL-6水平较GMPP患儿显著增高,IL-6显著增高可作为RMPP的预测因子[19],但具体的指标未确定。本研究发现,当IL-6≥14.455pg/mL预测为难治性肺炎时,此时预测的灵敏度为83.05%,特异度为61.21%,IL-6具有抗炎和促炎双向调节作用,其不同作用取决于IL-6的水平。提示当IL-6≥14.455pg/mL时,体内可能存在过度的炎症反应,IL-6与MPP的严重程度和转归密切相关。PA既往在细菌感染中研究比较广泛,它是一种非特异性宿主防御物质在肝细胞内合成,可清除细菌感染过程中释放于血循环中的毒性代谢产物,并被逐渐消耗,在急性感染时可迅速降低,如果感染未得到控制,PA可持续降低,是一种负急性时相蛋白,而在支原体感染中PA的变化研究较少。本研究数据显示RMPP时,PA明显降低,当PA≤101.500mg/L预测为RMPP时,此时预测的灵敏度为67.95%,特异度为69.49%。因此初步认为,IL-6≥14.455pg/mL、前白蛋白≤101.500mg/L是RMPP的高危因素,临床可考虑给予激素抗炎治疗,为临床上早期识别和治疗RMPP提供依据,但因为临床病例数较少,尚需要在后续的工作中进一步证实。
[1] YOUN Y S, LEE K Y, HWANG J Y, et al. Difference of clinical features in childhood Mycoplasma pneumoniae pneumonia[J]. BMC Pediatr, 2010,10: 48.
[2] 中华医学会儿科学分会呼吸学组,中华儿科杂志编辑委员会.儿童社区获得行肺炎管理指南(2013修订)(上)[J].中华儿科杂志,2013,51(10): 745-752.
[3] JAIN S, WILLIAMS D J, ARNOLD S R, et al. Community-acquired pneumonia requiring hospitalization among US children[J]. N Engl J Med, 2015,372(9): 835-845.
[4] ZHAO H Q, LI S L, CAO L, et al. Surveillance of Mycoplasma pneumoniae infection among children in Beijing from 2007 to 2012[J]. Chin Med J, 2014,127(7): 1244-1248.
[5] CHEN K P, JIA R Q, LI L, et al. The aetiology of community associated pneumonia in children in Nanjing, China and aetiological patterns associated with age and season[J]. BMC Public Health, 2015,15: 113.
[6] 伏昱璇,谷丽,杨蓉.呼吸道病原体9联检与咽拭子培养在儿科呼吸道感染中的临床应用[J].同济大学学报(医学版),2016,37(3): 87-90.
[7] DUMKE R, SCHNEE C, PLETZ M W, et al. Mycoplasma pneumoniae and Chlamydia spp. infection in community-acquired pneumonia, Germany, 2011-2012[J]. Emerging Infect Dis, 2015,21(3): 426-434.
[8] 宋蕾,彭芸,刘志敏,等.儿童坏死性肺炎支原体肺炎的影像学表现[J].中国医学影像技术,2012,28(3): 397-400.
[9] 孙慧明,季伟,蔡利红,等.不同年龄肺炎支原体肺炎患儿胸片与实验室检查特点比较[J].临床儿科杂志,2012,30(4): 342-346.
[10] ZHOU Y L, ZHANG Y Y, SHENG Y J, et al. More complications occur in macrolide-resistant than in macrolide-sensitive Mycoplasma pneumoniae pneumonia[J]. Antimicrob Agents Chemother, 2014,58(2): 1034-1038.
[11] MEYER SAUTEUR P M, VAN ROSSUM A M, VINK C. Mycoplasma pneumoniae in children: carriage, pathogenesis, and antibiotic resistance[J]. Curr Opin Infect Dis, 2014,27(3): 220-227.
[12] YOU S Y, JWA H J, YANG E A, et al. Effects of methylprednisolone pulse therapy on refractory Mycoplasma pneumoniae pneumonia in children[J]. Allergy Asthma Immunol Res, 2014,6(1): 22-26.
[13] CHOI Y J, JEON J H, OH J W. Critical combination of initial markers for predicting refractory Mycoplasma pneumoniae pneumonia in children: a case control study[J]. Respir Res, 2019,20(1): 193.
[14] LU A Z, WANG L B, ZHANG X B, et al. Combined treatment for child refractory Mycoplasma pneumoniae pneumonia with ciprofloxacin and glucocorticoid[J]. Pediatr Pulmonol, 2011,46(11): 1093-1097.
[15] MEIJVIS S C, HARDEMAN H, REMMELTS H H, et al. Dexamethasone and length of hospital stay in patients with community-acquired pneumonia: a randomised, double-blind, placebo-controlled trial[J]. Lancet, 2011,377(9782): 2023-2030.
[16] 蓝引乐,杨德华,陈志敏,等.甲泼尼龙治疗儿童难治性肺炎支原体肺炎的效果及患儿肺泡灌洗液细胞因子改变[J].中华儿科杂志,2015,10(53): 779-783.
[17] BACCI M R, LEME R C, ZING N P, et al. IL-6 and TNF-α serum levels are associated with early death in community-acquired pneumonia patients[J]. Revista Brasileira De Pesquisas Med E Biol, 2015,48(5): 427-432.
[18] 梁坤,张慧玉,田玲,等.细胞因子IL-6、IL-10在难治性肺炎患儿肺泡灌洗液中的变化及意义[J].临床儿科杂志,2014,32(4): 336-338.
[19] ZHANG Y Y, ZHOU Y L, LI S X, et al. The clinical characteristics and predictors of refractory Mycoplasma pneumoniae pneumonia in children[J]. PLoS One, 2016,11(5): e0156465.