随着腹腔镜技术的迭代更新,微创技术获得了前所未有的发展机遇。经自然腔道取出标本手术(nature orifice specimen extraction surgery, NOSES)是结直肠外科的一种微创技术探索。NOSES是指使用腹腔镜设备完成腹腔内操作,通过自然腔道取出手术标本的手术方式。该技术由经自然腔道内镜手术(natural transluminal endoscopic surgery, NOTES)的概念发展而来,NOSES结合了NOTES的无辅助切口和腹腔镜微创技术,近年来在结直肠癌治疗中越来越普遍[1-3]。
NOSES最早于1993年由Frankin报道[4]。随着3D腹腔镜技术和NOSES术式创新,NOSES逐步应用到腹腔镜结直肠癌的手术中[5-6]。NOSES关键在于标本取出和消化道重建。巨大肿瘤和肥胖人群往往会导致NOSES术中标本取出困难。同时,NOSES面临着标本取出困难和操作过程中无法无菌或无瘤,因此NOSES被国外报道后在国际上尚未广泛应用[7]。近年来,随着腹腔镜设备发展,标本袋应用和手术技术创新,NOSES可以很好地实现术中无菌和无瘤[8-10]。
目前研究表明,NOSES对改善患者术后疼痛和手术并发症具有明显优势[11],但尚未有研究探讨直肠癌患者接受NOSES术后生存质量分析。NOSES按取出方式不同可分为经阴道取出和经直肠取出两大类。经直肠取出标本不需要额外切口,是目前NOSES首选方案[11]。本研究中NOSES均采用经直肠取出标本技术,对患者术后短期临床疗效和生存质量进行研究。
1 资料与方法
1.1 研究对象
2014年2月至2016年2月期间,同济大学附属东方医院胃肠外科接诊341例直肠癌患者采用随机数字表方法将患者分为3组,无切口组(NOSES,n=114)、小切口组(小切口,n=121)、传统开腹组(OS,n=106)。术前检查肿瘤直径>5cm、肿瘤距离肛缘<5cm、BMI>32kg/m2的患者排除于本次研究之外。经充分告知后,患者和家属同意手术方案并签署知情同意书。无切口手术方案的实施经过医院伦理委员会讨论通过。
1.2 手术方法
腹腔镜小切口手术和开腹手术按照常规手术方式实施。腹部无切口经直肠取出标本手术步骤: 距离肿瘤下缘2~4cm处裸化肠管,纱线条结扎肠管,肿瘤远端结扎线远侧约1cm处用超声刀横断远侧肠壁。充分扩肛至4指,经肛门插入带齿Kock钳至直肠残端上方4~5cm;经右下腹主操作Trocar内置入长约25cm标本保护套,自肛门拖出保护建立无菌通道(图1A),经肛门置入吻合器钉砧后(图1B),将标本置入保护套一并拖出(图1C)。剪除近端肠管残端闭合缘,局部消毒,置入抵钉座,圈套器将肠壁环形固定于抵钉座中心杆上(图1D)。
1.3 术前、术后指标评估
记录3组患者术前、术后临床指标。术前指标包括性别、年龄、BMI、肿瘤距肛缘距离、既往腹部手术史、CEA、CA199。术后指标包括手术时间、术中出血量、肿瘤最大直径、术后排气时间、住院时间、初次肛门排气时间、围手术期并发症、术后疼痛评分。手术标本: 肿瘤大小、肿瘤切缘阳性与否、淋巴结分期和肿瘤T分期。
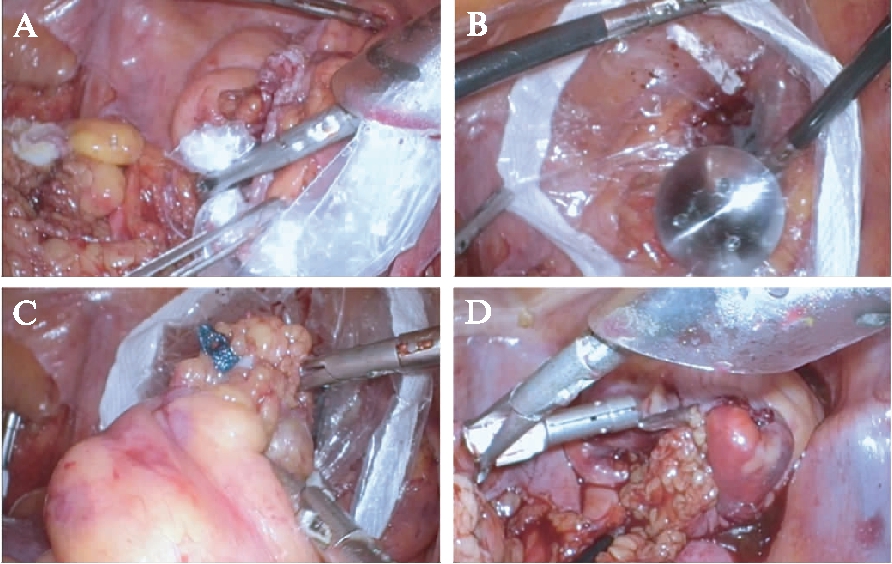
图1 NOSES术中标本经直肠取出手术步骤
Fig.1 Surgical procedure for transanal specimen extraction
A: 置入保护套并自肛门拖出;B: 置入吻合器钉砧;C: 标本从保护套内拖出;D: 自肛门端端吻合器吻合肠管
1.4 生活质量和疼痛程度评估
采用10分制视觉模拟量表(visual analog scale,VAS)作为疼痛程度评价。分别收集和评价3组患者术后第1天、术后第3天VAS评分情况。0分表示无痛,10分表示有严重疼痛,疼痛越厉害,分数越高[12]。
SF-36量表是目前应用最广的健康调查表,其包括躯体功能评分与心理功能评分两大方向,共有8个项目,包括生理机能、生理职能、躯体疼痛、一般健康状况、精力、社会功能、情感职能以及精神健康。每个健康项目的分数范围从0到100,分值越高代表患者生存质量越好。本次入组患者在术前、术后1个月进行SF-36量表填写和分析[13]。
1.5 统计学处理
所有数据采用SPSS 20.0统计软件进行数据分析。计量资料采用![]() 表示,采用t检验比较,计数资料采用[n(%)]表示,采用χ2检验比较。3组患者SF-36量表各项评分采用Levene法进行方差齐性检验。三者间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
表示,采用t检验比较,计数资料采用[n(%)]表示,采用χ2检验比较。3组患者SF-36量表各项评分采用Levene法进行方差齐性检验。三者间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 腹部切口长度及疼痛评分
3组患者术后腹部切口长度不同,NOSES组为(1.2±0.3) cm,小切口组为(5.6±1.4) cm,开腹组为(12.2±3.8) cm,3组间差异有统计学意义(P=0.001),见图1。术后第1天VAS评分,NOSES组是3.4±1.6,小切口组是4.8±2.1,OS组是5.6±2.7,差异有统计学意义(P<0.05)。术后第3天,NOSES组的VAS评分为1.5±0.9,明显低于其他2组,差异有统计学意义(P<0.05),见图2、表1。
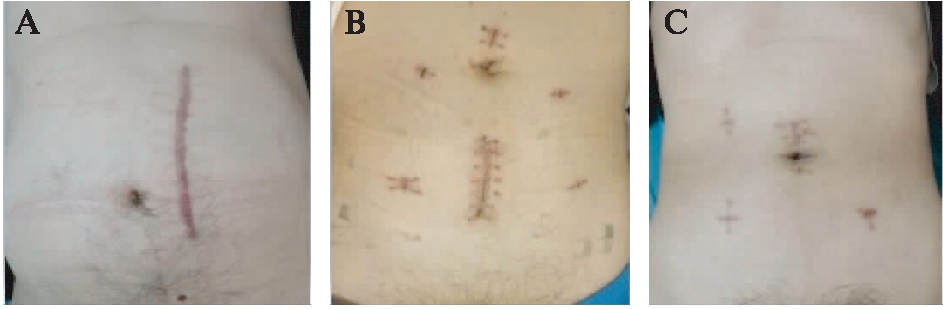
图2 3组患者术后腹部切口长度比较
Fig.2 Comparison of abdominal incision length in three groups
A: 开腹组;B: 小切口组;C: MOSES组
表1 3组患者术后VAS评分
Tab.1 Postoperative VAS score in the three groups
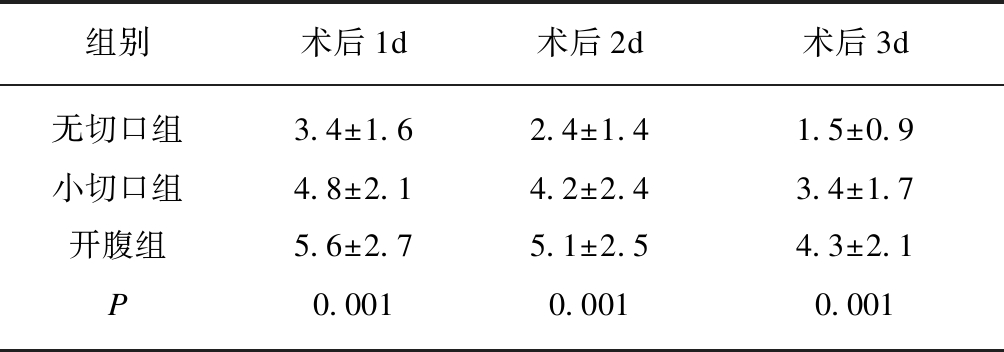
组别术后1d术后2d术后3d无切口组3.4±1.62.4±1.41.5±0.9小切口组4.8±2.14.2±2.43.4±1.7开腹组5.6±2.75.1±2.54.3±2.1P0.0010.0010.001
VAS: 视觉模拟量表.3组之间方差分析,P<0.001
2.2 患者术前、术后临床指标比较
3组患者术前在年龄、性别、BMI、肿瘤距肛缘距离、血清CEA和CA199等指标差异无统计学意义(P>0.05),见表2。
3组患者在术后肿瘤直径、淋巴结阳性率和肿瘤分期上差异无统计学意义(P>0.05)。
3组中NOSES组手术时间最长(P<0.05);OS组术中出血量最多,差异有统计学意义;NOSES组术后肛门初次排气时间最短(P<0.05),在平均住院天数方面最少,差异具有统计学意义(P<0.05)。NOSES组术后并发症发生率为10.5%,低于小切口组的16.5%,两者差异有统计学意义(P<0.05),见表3。
表2 3组患者术前基本临床指标
Tab.2 Preoperative patient characteristics for the three groups
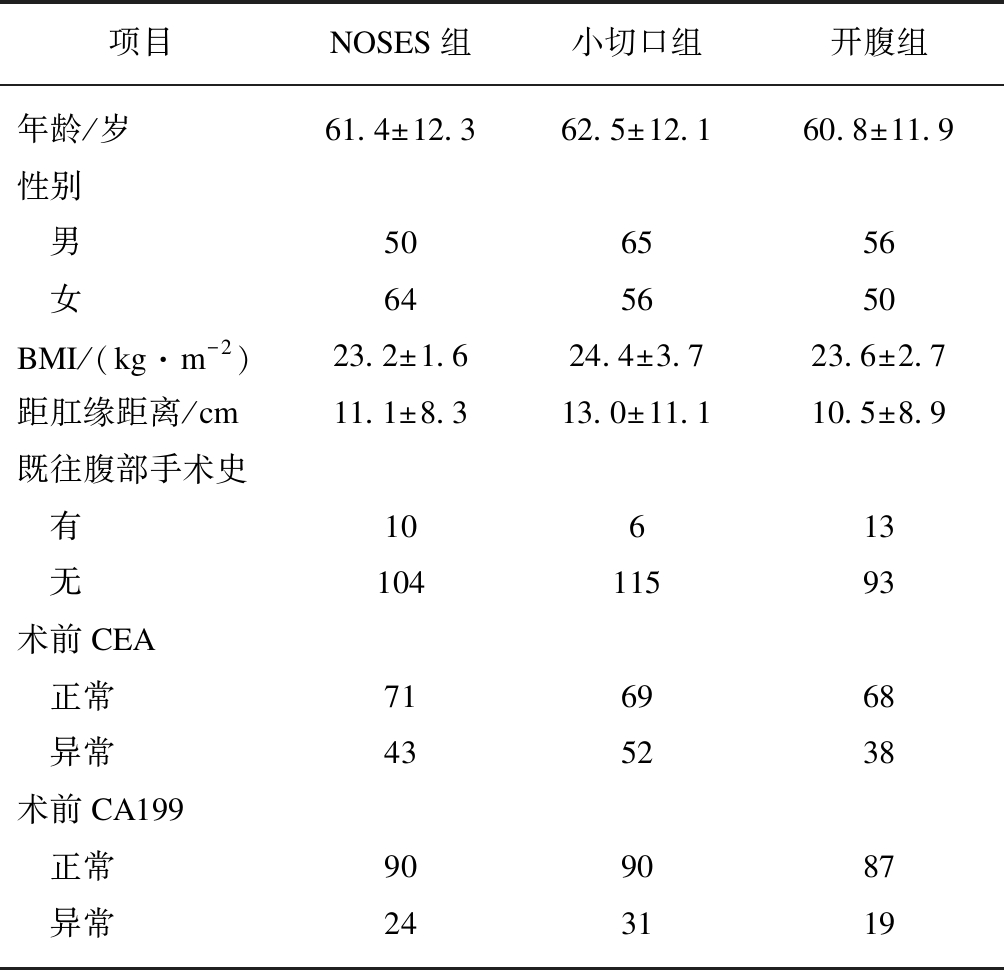
项目NOSES组小切口组开腹组年龄/岁61.4±12.362.5±12.160.8±11.9性别 男506556 女645650BMI/(kg·m-2)23.2±1.624.4±3.723.6±2.7距肛缘距离/cm11.1±8.313.0±11.110.5±8.9既往腹部手术史 有10613 无10411593术前CEA 正常716968 异常435238术前CA199 正常909087 异常243119
表3 3组患者手术相关指标和术后病理
Tab.3 Postoperative clinical indexes in the three groups
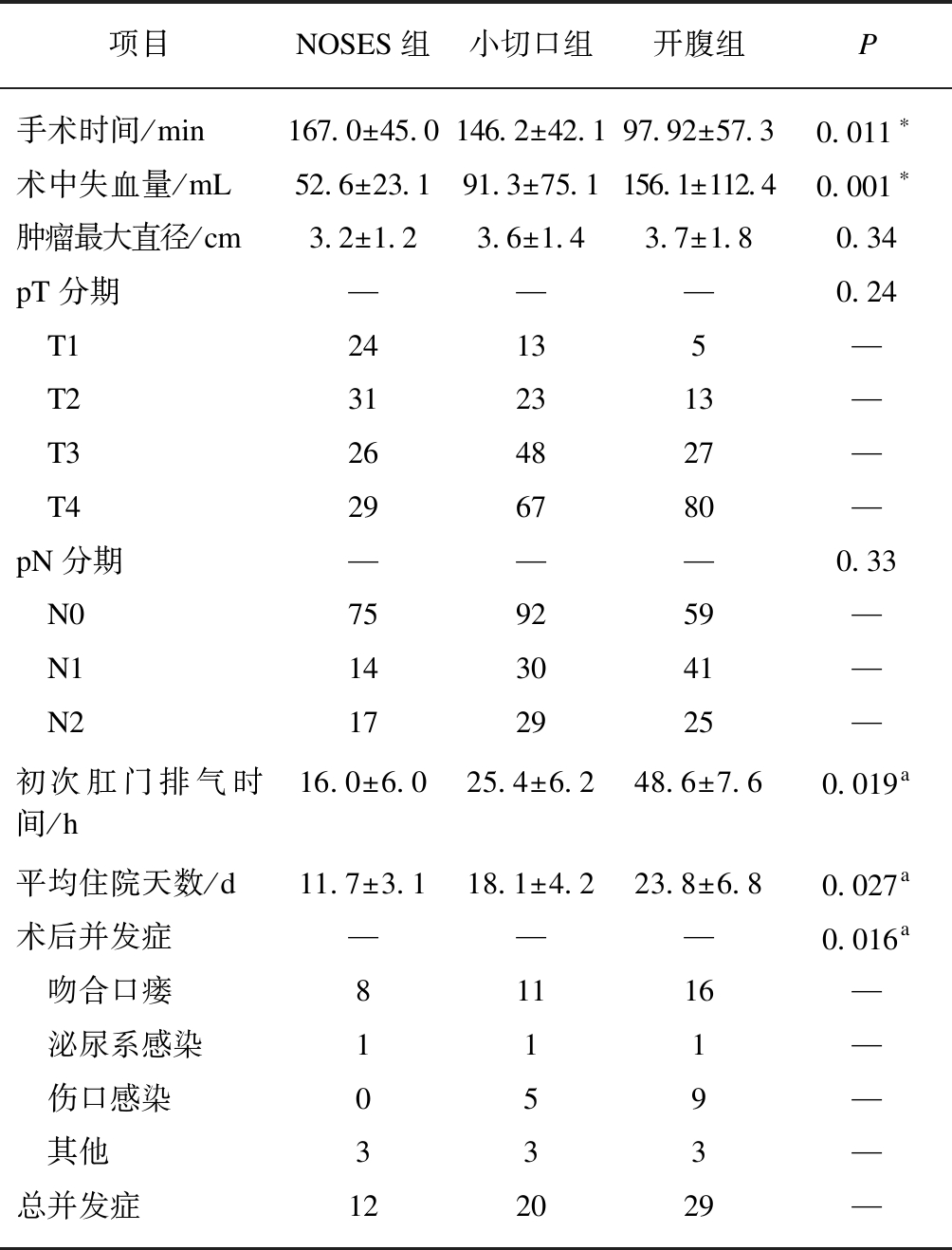
项目NOSES组小切口组开腹组P手术时间/min167.0±45.0146.2±42.197.92±57.30.011∗术中失血量/mL52.6±23.191.3±75.1156.1±112.40.001∗肿瘤最大直径/cm3.2±1.23.6±1.43.7±1.80.34pT分期———0.24 T124135— T2312313— T3264827— T4296780—pN分期———0.33 N0759259— N1143041— N2172925—初次肛门排气时间/h16.0±6.025.4±6.248.6±7.60.019a平均住院天数/d11.7±3.118.1±4.223.8±6.80.027a术后并发症———0.016a 吻合口瘘81116— 泌尿系感染111— 伤口感染059— 其他333—总并发症122029—
a为3组之间单因素方差分析
2.3 患者生活质量评估
3组患者术前SF-36生存质量平均得分为94.6±2.7、95.5±2.4、93.7±1.9,差异无统计学意义(P>0.05)。术后1个月,NOSES组、小切口组在各项评分上均优于OS组,差异有统计学意义(P<0.05)。NOSES组在生理机能、生理职能、社会功能、情感职能四个评分中优于小切口组,差异有统计学(P<0.05)。不管是身体健康领域还是精神健康领域,NOSES组评分最高,优于其他2组,具有统计学差异(P<0.05),见表4。
表4 3组患者术后1个月SF-36量表项目比较
Tab.4 Postoperative quality of life in the three groups(SF-36 points) ![]()
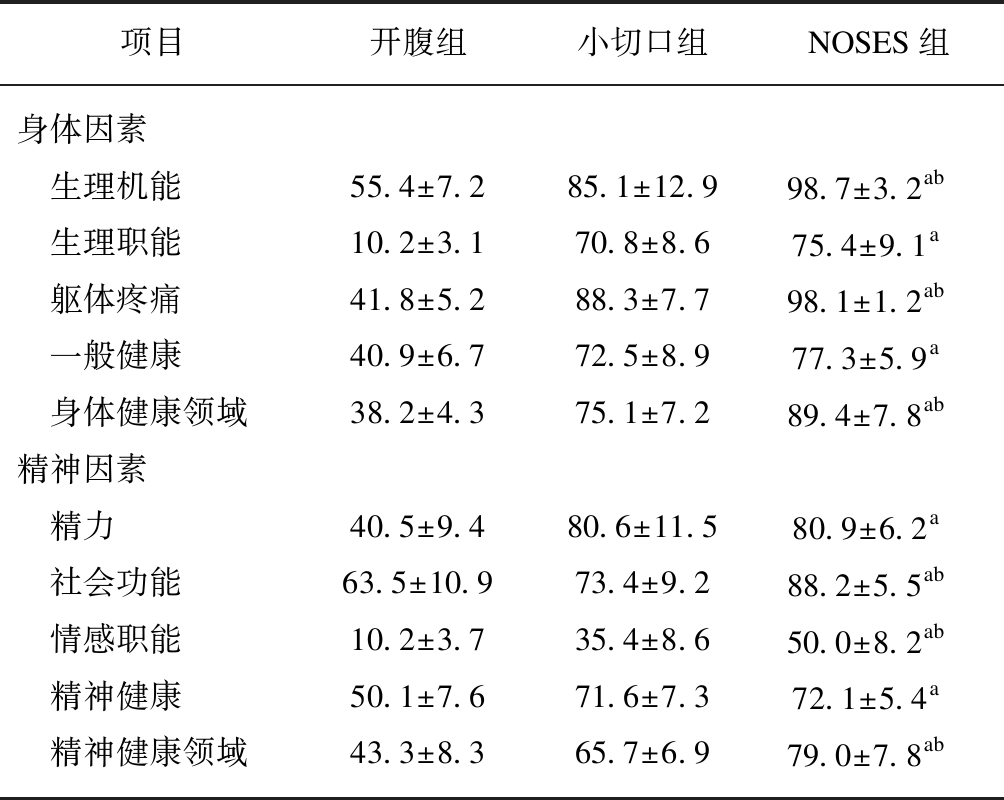
项目开腹组小切口组NOSES组身体因素 生理机能55.4±7.285.1±12.998.7±3.2ab 生理职能10.2±3.170.8±8.675.4±9.1a 躯体疼痛41.8±5.288.3±7.798.1±1.2ab 一般健康40.9±6.772.5±8.977.3±5.9a 身体健康领域38.2±4.375.1±7.289.4±7.8ab精神因素 精力40.5±9.480.6±11.580.9±6.2a 社会功能63.5±10.973.4±9.288.2±5.5ab 情感职能10.2±3.735.4±8.650.0±8.2ab 精神健康50.1±7.671.6±7.372.1±5.4a 精神健康领域43.3±8.365.7±6.979.0±7.8ab
与开腹组相比,aP<0.05;与小切口组相比,bP<0.05
3 讨 论
随着外科技术和器械设备的发展,结直肠癌手术治疗逐渐微创化,这也是当前外科领域总体趋势。腹腔镜技术在全世界已经普及,在有些领域已经取代了开腹手术,成为一种常规治疗手段[14-16]。NOSES在腹腔镜的基础上,经自然腔道取出手术标本,通过创新方式重建肠道,是结直肠外科领域的又一微创技术创新。目前NOSES术式很多[17-18],主要分为经直肠和经阴道两大类。本次研究中NOSES采用经直肠取出标本,评估了NOSES术后患者生活质量和临床疗效,为后续NOSES术式规范和推广提供可靠的临床研究依据。
NOSES避免了腹部切口,有效地减轻患者术后疼痛。术后疼痛减轻对快速康复有极大地帮助[19]。本研究中NOSES组术后腹部切口长度远低于其他2组,术后VAS评分也最低,说明术后疼痛和腹壁切口长度密切相关[20]。此外,缩小腹部切口有利于避免切口感染、脂肪液化等手术并发症[21]。本研究显示NOSES术后短期临床疗效优势显著。NOSES组患者术后排气时间、住院天数等指标明显优于小切口组和开腹组,此外,在术后并发症控制良好,NOSES组显著低于小切口组。NOSES手术通过避免腹部切口,在保证临床疗效的同时,使得患者术后生存质量明显上升。本研究显示,3组患者术后1个月生存质量差异明显,其中NOSES组总体生存质量最高,开腹组生存质量最低,差异明显。生存质量的改善使得结直肠癌患者更好康复,提高治疗质量,符合微创外科趋势[22-24]。
在微创外科时代,外科手术原则是在确保安全、完整切除病变组织的前提下,尽量保留正常组织器官,减少创伤,降低对患者生活质量影响。NOSES符合微创治疗理念,具有重要临床推广价值。然而,NOSES仍处于不断发展过程中,外科医生要严格把握适应证,让患者真正获益。
[1] 杜涛,傅传刚,周主青,等.3D腹腔镜单吻合器法经肛门取出标本在超低位直肠癌保肛手术中的运用[J].同济大学学报(医学版),2019,40(3): 376-379.
[2] 朱哲,傅传刚,周主青,等.经直肠取出标本的全腹腔镜前切除术治疗T4a期高位直肠癌及乙状结肠癌的安全性分析[J].中华胃肠外科杂志,2019,22(5): 484-487.
[3] 王锡山.经自然腔道取标本手术和经自然腔道内镜手术及经肛全直肠系膜切除术的应用前景与挑战[J].中华胃肠外科杂志,2018,21(8): 856-861.
[4] FRANKLIN M E Jr, RAMOS R, ROSENTHAL D, et al. Laparoscopic colonic procedures[J]. World J Surg, 1993,17(1): 51-56.
[5] CHEUNG H Y, LEUNG A L, CHUNG C C, et al. Endo-laparoscopic colectomy without mini-laparotomy for left-sided colonic tumors[J]. World J Surg, 2009,33(6): 1287-1291.
[6] AKAMATSU H, OMORI T, OYAMA T, et al. Totally laparoscopic sigmoid colectomy: a simple and safe technique for intracorporeal anastomosis[J]. Surg Endosc, 2009,23(11): 2605-2609.
[7] SENFT J D, DRÖSCHER T, GATH P, et al. Inflammatory response and peritoneal contamination after transrectal natural orifice specimen extraction(NOSE) versus mini-laparotomy: a porcine in vivo study[J]. Surg Endosc, 2018,32(3): 1336-1343.
[8] WOLTHUIS A M, DEBUCKVANOVERSTRAETEN A, D’HOORE A. Laparoscopic NOSE colectomy with a camera sleeve: a technique in evolution[J]. Colorectal Dis, 2015,17(5): O123-O125.
[9] WOLTHUIS A M, PENNINCKX F, D’HOORE A. Laparoscopic sigmoid resection with transrectal specimen extraction has a good short-term outcome[J]. Surg Endosc, 2011,25(6): 2034-2038.
[10] WOLTHUIS A M, VANGELUWEB, FIEUWSS, et al. Laparoscopic sigmoid resection with transrectal specimen extraction: a systematic review[J]. Colorectal Dis, 2012,14(10): 1183-1188.
[11] 邢俊杰,张辰新,杨晓虹,等.腹部无切口经直肠取出标本的腹腔镜乙状结肠癌根治术与传统腹腔镜手术近期效果比较[J].中华胃肠外科杂志,2017,20(06): 665-670.
[12] BOUSQUET P J, COMBESCURE C, KLOSSEK J M, et al. Change in visual analog scale score in a pragmatic randomized cluster trial of allergic rhinitis[J]. J Allergy Clin Immunol, 2009,123(6): 1349-1354.
[13] APOLONE G, FILIBERTI A, CIFANI S, et al. Evaluation of the EORTC QLQ-C30 questionnaire: a comparison with SF-36 Health Survey in a cohort of Italian long-survival cancer patients[J]. Ann Oncol, 1998,9(5): 549-557.
[14] LORENZON L, LATORRE M, ZIPARO V, et al. Evidence based medicine and surgical approaches for colon cancer: evidences, benefits and limitations of the laparoscopic vs open resection[J]. World J Gastroenterol, 2014,20(13): 3680-3692.
[15] LEE S H, LIM S, KIM J H, et al. Robotic versus conventional laparoscopic surgery for rectal cancer: systematic review and meta-analysis[J]. Ann Surg Treat Res, 2015,89(4): 190-201.
[16] DAI S D, OCHIAI H, TSUKAMOTO S, et al. Long-term outcomes of laparoscopic versus open D3 dissection for stage II/III colon cancer: results of propensity score analyses[J]. Eur J Surg Oncol, 2018,44(7): 1025-1030.
[17] BENHIDJEB T, STARK M. An innovative technique for colorectal specimen retrieval: a new era of “Natural Orifice Specimen Extraction”(N.O.S.E.)[J]. Dis Colon Rectum, 2010,53(4): 502-503.
[18] FU C G, GAO X H, WANG H, et al. Treatment for early ultralow rectal cancer: pull-through intersphi-ncteric stapled transection and anastomosis(Pista) versus low anterior resection[J]. Tech Coloproctol, 2013,17(3): 283-291.
[19] PEDRAZZANI C, MENESTRINA N, MORO M, et al. Local wound infiltration plus transversus abdominis plane(TAP) block versus local wound infiltration in laparoscopic colorectal surgery and ERAS program[J]. Surg Endosc, 2016,30(11): 5117-5125.
[20] YAMAMOTO M, ASAKUMA M, TANAKA K, et al. Clinical impact of single-incision laparoscopic right hemicolectomy with intracorporeal resection for advanced colon cancer: propensity score matching analysis[J]. Surg Endosc, 2019,33(11): 3616-3622.
[21] HISADA M, KATSUMATA K, ISHIZAKI T, et al. Complete laparoscopic resection of the rectum using natural orifice specimen extraction[J]. World J Gastroenterol, 2014,20(44): 16707-16713.
[22] VELTCAMP HELBACH M, KOEDAM T W A, KNOL J J, et al. Quality of life after rectal cancer surgery: differences between laparoscopic and transanal total mesorectal excision[J]. Surg Endosc, 2019,33(1): 79-87.
[23] DOWNING A, FINAN P, SEBAG-MONTEFIORE D, et al. Health-related quality of life and functional outcomes following curative treatments for rectal cancer: a population-level study in England[J]. Int J Radiat Oncol, 2016,96(2): S124-S125.
[24] DECOSSEJ J, CENNERAZZOW J. Quality-of-life management of patients with colorectal cancer[J]. CA Cancer J Clin, 1997,47(4): 198-206.