弥漫大B细胞淋巴瘤(diffuse large B-cell lymphoma, DLBCL)是一种异质性很大的侵袭性淋巴瘤,为了提高国际预后指数(international prognostic index, IPI)分期系统评估的准确性,越来越多的研究正在寻找新的生物学变量。研究[1-5]发现DLBCL患者中多种炎性因子水平增高,并与患者临床表现及不良预后相关。本研究采用前瞻性研究方法,收集2015—2017年40例初发DLBCL患者临床资料,检测初发DLBCL患者血清中炎症指标C反应蛋白(C-reactive protein, CRP)和4种细胞因子TNF-α、sIL-2r、IL6、IL-8的水平,并与肿瘤负荷指标LDH、血β2微球蛋白(β2-MG)、铁蛋白进行对比,探索炎性指标在初发不同分层DLBCL患者中的临床意义。
1 资料与方法
1.1 一般资料
收集2015年9月—2017年9月于同济大学附属同济医院初诊的40例DLBCL患者的临床资料。诊断及分类采用2001年WHO淋巴造血组织肿瘤的分类标准,所有患者均接受利妥昔单抗联合化疗方案。将患者按照初治后是否获得完全缓解(complete remission, CR),是否存在发热、盗汗、体质量减轻等症状(有症状B组,无症状为A组)和IPI积分进行分组比较。其中,CR组(n=24)和非CR组(n=16);A组(n=27)和B组(n=13);IPI 1~2分(n=20)和IPI 3~5分(n=20)。
1.2 主要试剂及检测方法
TNF-α、sIL-2r、IL-6、IL-8检测采用化学发光法,检测试剂盒购自Siemens公司,标本采用患者清晨空腹静脉血3mL,血液凝固后分离血清,采用Siemens Immulete 1000分析仪(购自德国西门子公司)自动检测。血β2-MG及铁蛋白测定采用放射免疫分析法测定。CRP采用免疫透射比浊法检测,LDH采用肌酸激酶检测试剂盒检测。
1.3 疗效评估
患者每完成2个疗程化疗后进行疗效评定,6个周期治疗后进行全面评估。疗效判定按照WHO疗效评价标准,包括CR、部分缓解(partial response, PR)、稳定(stable disease, SD)和进展(progressive disease, PD)。随访方式包括电话随访和门诊复查等,中位随访时间12(1~36)个月。
1.4 统计学处理
数据处理应用SPSS 22.0软件。两组间符合参数条件的变量比较采用两个独立样本均数的t检验,不符合参数条件的变量比较采用非参数的秩和检验(Mann-Whitney检验),两组间率的比较采用χ2检验,相关性采用非参数检验的Spearman相关性分析。所有的P值均为双向,P<0.05为差异有统计学意义。
2 结 果
2.1 CR组与非CR组患者临床特征及炎性指标对比分析
CR组和非CR组患者相比,非CR组患者IPI积分3~5分患者比例显著高于CR组患者的比例,差异有统计学意义(P<0.05),非CR患者年龄、结外累及部位≥2处数目、ECOG积分≥2分比例明显高于CR组患者,见表1。
在炎性指标上,非CR组患者CRP、IL-8显著高于CR组患者,差异有统计学意义(P=0.0113,P=0.0486);其他炎性因子sIL-2r、TNF-α、IL-6和铁蛋白有增高趋势,但差异无统计学意义。非CR组患者血β2-MG水平明显高于CR组患者。见表1。
2.2 A组与B组患者临床特征及炎性指标对比分析
对比A组和B组患者的临床特征,两组在总体IPI积分上无显著差异,但B组患者LDH水平、Ann-Arbor分期Ⅲ-Ⅳ期比例、ECOG积分≥2分比例显著高于A组患者,见表2。
在炎性指标上,B组患者炎性因子sIL-2r水平显著高于A组患者,差异有统计学意义(P<0.05),TNF-α水平和IL-6水平也显著高于A组患者,B组患者CRP水平显著高于A组患者;血β2-mG显著高于A组患者;铁蛋白指标明显高于A组患者;差异有统计学意义(P<0.05);两组之间IL-8水平差异无统计学意义。见表2。
2.3 IPI高中危患者炎性指标CRP、sIL-2r、IL-6对比分析
根据IPI分组对比发现,在炎性指标上,高中危组患者CRP均数显著高于低中危组患者;高中危组患者炎性因子sIL-2r均数显著高于低中危组患者;IL-6水平显著高于低中危组患者;而其他炎性因子TNF-α、IL-8无显著差异。高中危组患者血β2-MG均数显著高于低中危组患者,铁蛋白及LDH水平显著高于低中危组患者,见表3。
表1 根据患者治疗后疗效分组的对比分析
Tab.1 Comparative analysis of inflammatory indexes according to treatment response

项目CR组(n=24)非CR组(n=16)P年龄/岁54.42(49.38~59.46)70(63.07~76.93)0.0019男性14(58.33%)9(56.25%)1IPI积分0.0031 0~2分17(70.83%)3(18.75%) 3~5分7(29.17%)13(81.25%)Ann-Arbor分期Ⅲ~Ⅳ期13(54.17%)13(81.25%)0.1010结外累及部位≥2处8(33.33%)12(75%)0.0225ECOG积分≥2分3(12.5%)8(50%)0.0138LDH/(U·L-1)325.8(214.3~437.2)692.2(221.9~1163)0.1063CRP/(mg·L-1)22.31(6.69~37.94)60.68(28.52~92.84)0.0113铁蛋白/(ng·mL-1)502.2(304.2~700.2)767.9(446.4~1089)0.0750血β2-MG/(mg·mL-1)2.75(2.24~3.26)4.71(3.39~6.03)0.0014细胞因子 sIL-2r/(U·mL-1)2146(954.8~3325)3482(1899~5065)0.1149 TNF-α/(pg·mL-1)13.23(9.02~17.43)21.7(10.59~32.81)0.0978 IL-6/(pg·mL-1)12.35(4.81~19.9)23.40(6.98~39.81)0.1280 IL-8/(pg·mL-1)26.66(9.51~45.81)64.48(19.68~109.3)0.0486B组症状6(25%)7(43.75%)0.7158
表2 根据患者是否存在B组症状分组的对比分析
Tab.2 Comparative analysis based on whether patients have group B symptoms
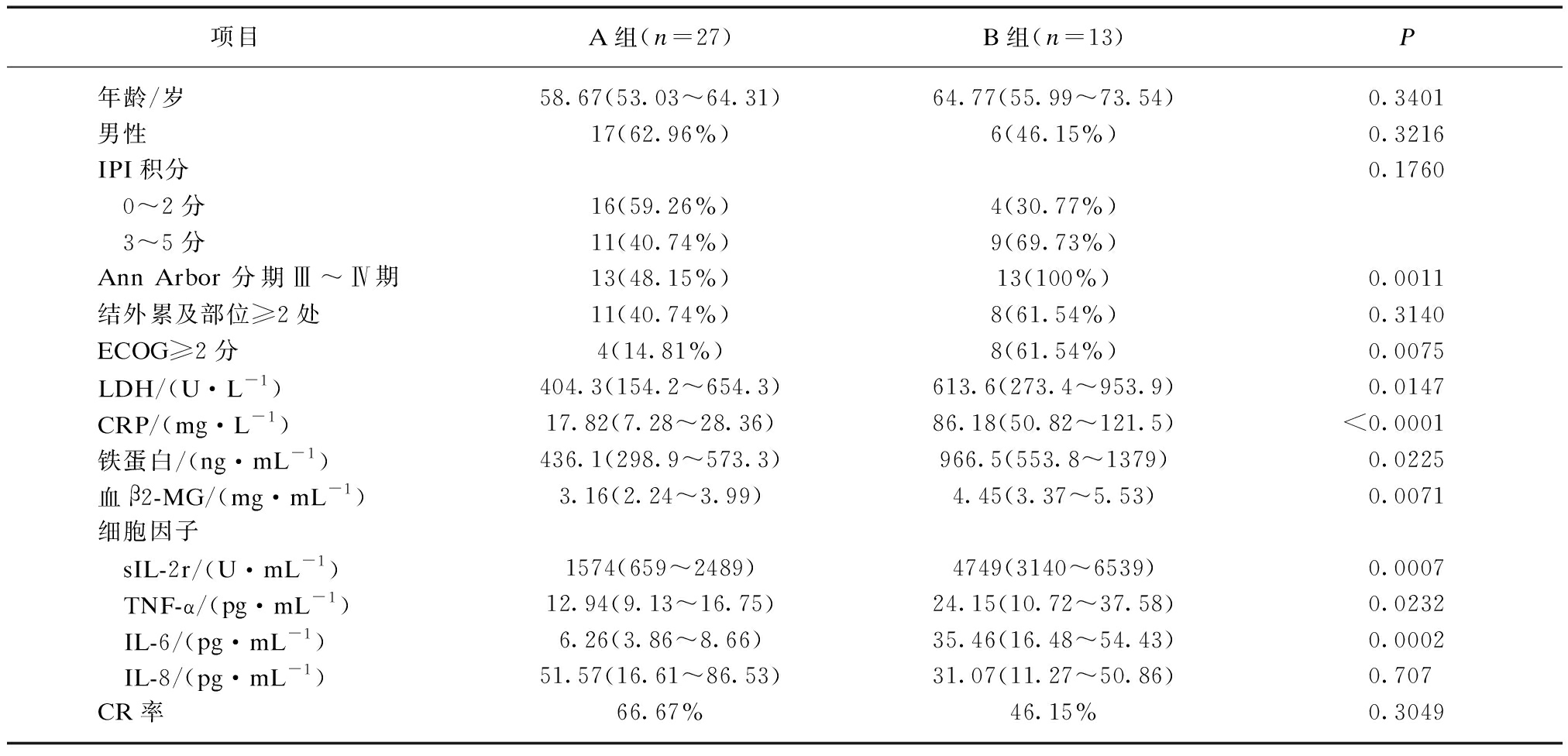
项目A组(n=27)B组(n=13)P年龄/岁58.67(53.03~64.31)64.77(55.99~73.54)0.3401男性17(62.96%)6(46.15%)0.3216IPI积分0.1760 0~2分16(59.26%)4(30.77%) 3~5分11(40.74%)9(69.73%)Ann Arbor分期Ⅲ~Ⅳ期13(48.15%)13(100%)0.0011结外累及部位≥2处11(40.74%)8(61.54%)0.3140ECOG≥2分4(14.81%)8(61.54%)0.0075LDH/(U·L-1)404.3(154.2~654.3)613.6(273.4~953.9)0.0147CRP/(mg·L-1)17.82(7.28~28.36)86.18(50.82~121.5)<0.0001铁蛋白/(ng·mL-1)436.1(298.9~573.3)966.5(553.8~1379)0.0225血β2-MG/(mg·mL-1)3.16(2.24~3.99)4.45(3.37~5.53)0.0071细胞因子 sIL-2r/(U·mL-1)1574(659~2489)4749(3140~6539)0.0007 TNF-α/(pg·mL-1)12.94(9.13~16.75)24.15(10.72~37.58)0.0232 IL-6/(pg·mL-1)6.26(3.86~8.66)35.46(16.48~54.43)0.0002 IL-8/(pg·mL-1)51.57(16.61~86.53)31.07(11.27~50.86)0.707CR率66.67%46.15%0.3049
表3 根据患者IPI积分分组的对比分析
Tab.3 Comparative analysis according to patients’ IPI scores

临床特征IPI 1~2分(n=20)IPI 3~5分(n=20)P年龄/岁54.55(49.57~59.33)66.75(59.55~73.95)0.0068男性14(70%)9(45%)0.2003Ann Arbor分期Ⅲ~Ⅳ期8(40%)17(85%)0.0079结外累及部位≥2处2(10%)18(90%)<0.0001ECOG≥2分1(5%)10(50%)0.0012LDH/(U·L-1)249(160.9~337)695.7(325.2~1066)0.0016CRP/(mg·L-1)13.95(1.95~25.96)61.52(34.33~88.81)0.0207铁蛋白/(ng·mL-1)418.9(242.2~595.6)798(512.9~1083)0.0361血β2-MG/(mg·mL-1)2.58(2.13~3.03)4.58(3.44~5.73)0.0007细胞因子 sIL-2r/(U·mL-1)1575(582.4~2568)3746(2291~5200)0.0291 TNF-α/(pg·mL-1)14.06(9.27~18.86)19.66(10.14~29.18)0.3538 IL-6/(pg·mL-1)8.96(2.16~15.76)23.96(10.04~37.88)0.0159 IL-8/(pg·mL-1)36.4(7.49~65.31)50.31(14.2~86.43)0.3981CR率85%30%0.0107B组症状4(20%)9(45%)0.1760
2.4 炎性指标与肿瘤负荷指标血β2-MG、LDH显著相关
进一步将所测得的炎性指标(4种炎性因子与CRP)分别与肿瘤负荷指标(铁蛋白、血β2-MG、LDH)进行相关性分析,除IL-8外,4种炎性指标与血β2-MG和LDH均呈显著正相关,3种炎性指标sIL-2r、IL-6、CRP与铁蛋白呈正相关,CRP与3种炎性因子sIL-2r、TNF-α、IL-6也显著相关,见表4。
表4 炎性指标与肿瘤负荷指标相关性分析
Tab.4 Correlation Analysis between inflammatory Indexes and tumor burden Indexes
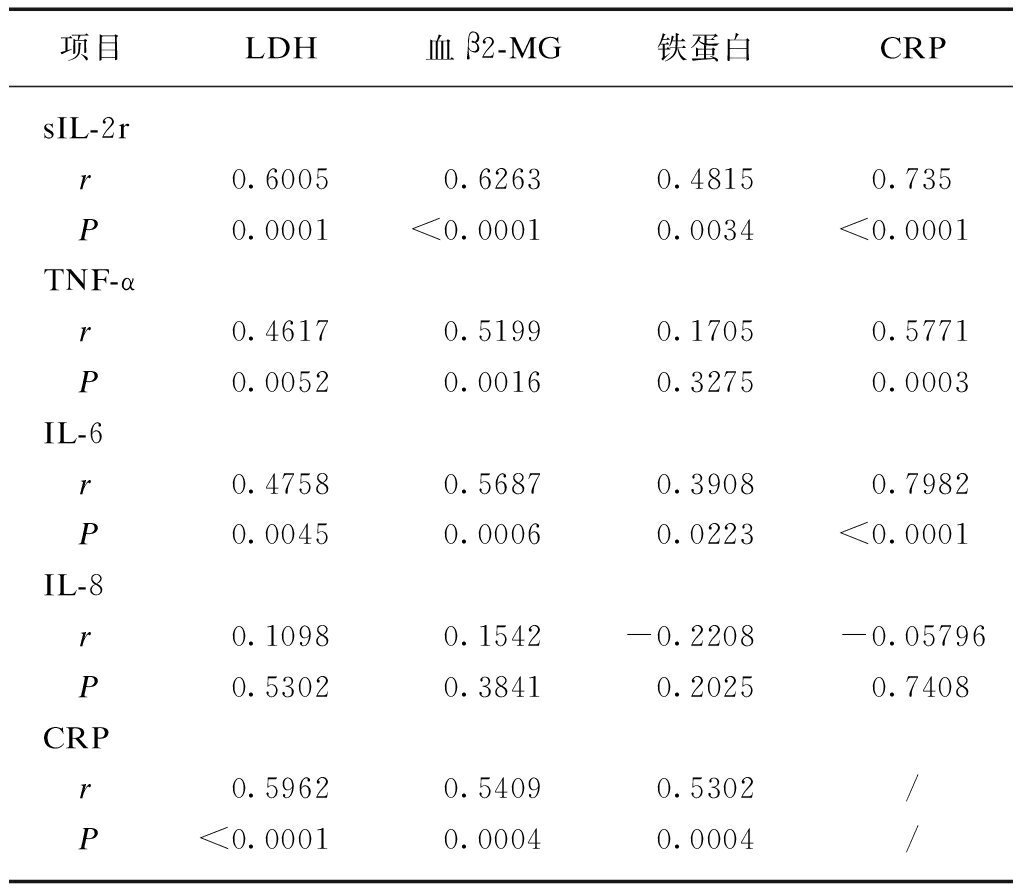
项目LDH血β2-MG铁蛋白CRPsIL-2r r0.60050.62630.48150.735 P0.0001<0.00010.0034<0.0001TNF-α r0.46170.51990.17050.5771 P0.00520.00160.32750.0003IL-6 r0.47580.56870.39080.7982 P0.00450.00060.0223<0.0001IL-8 r0.10980.1542-0.2208-0.05796 P0.53020.38410.20250.7408CRP r0.59620.54090.5302/ P<0.00010.00040.0004/
r值为Spearman相关性系数
3 讨 论
DLBCL是发病率最高的非霍奇金淋巴瘤亚型,患者在临床特征、遗传和分子水平上表现出显著的异质性。IPI虽有助于预测DLBCL患者的预后,但在临床实践中具有相同IPI积分的患者在生存率上表现出显著的变异性,表明有其他因素在患者生存与预后中扮演重要角色。Shi等[6]的研究发现,DLBCL患者炎性因子sIL-2r和IL-6增高导致的肝功能损伤提示患者预后不良![]() 等[2]的研究发现白介素和β2-MG评估应与IPI联合使用,可更准确地预测患者的生存分层。上述研究表明,炎症反应在DLBCL的疾病发生发展和预后中发挥重要作用。
等[2]的研究发现白介素和β2-MG评估应与IPI联合使用,可更准确地预测患者的生存分层。上述研究表明,炎症反应在DLBCL的疾病发生发展和预后中发挥重要作用。
Charbonneau等[1]的研究评估了30种细胞因子与DLBCL的关系,发现在单个细胞因子模型中有12种细胞因子与DLBCL显著相关,其中sIL-2r与DLBCL的相关性最强,IL-6、IL-8、IL-10、IFN-r、IP-10、VEGF等细胞因子也有相关性。除炎性因子外,CRP、血β2-MG、铁蛋白、LDH也在肿瘤的进程中发挥重要作用。CRP是一种由肝脏合成的蛋白质,是较敏感的非特异性炎症反应标志。LDH是一种糖酵解酶,在淋巴瘤患者中,LDH增高多提示预后不良,可作为监测肿瘤负荷的常用指标。β2-MG是一种小分子球蛋白,正常人β2-MG的合成与释放相当恒定,淋巴瘤患者肿瘤细胞合成β2-MG显著增加。铁蛋白是铁的贮存形式,它是判断机体是否缺铁或铁负荷过多的有效指标。某些恶性肿瘤细胞可以合成和分泌铁蛋白,该指标可用于辅助评估恶性肿瘤。
为了进一步了解炎性反应在DLBCL患者中的临床意义,本研究选取TNF-α、sIL-2r、IL-6、IL-8和CRP作为5种炎性指标,血LDH、β2-MG、铁蛋白作为3种肿瘤负荷指标,并结合患者的临床特征和IPI积分,评估炎症反应在DLBCL中的作用。本研究发现: (1) 初治未达CR患者IPI积分显著增高,炎性指标仅有CRP和IL-8显著增高,其他炎性因子sIL-2r、IL-6、TNF-α虽有增高趋势,但无统计学意义。说明炎性因子在预测患者是否达到CR方面的作用有限,不能仅通过炎症因子水平预测患者能否达到CR。(2) 在合并B组症状患者中,sIL-2r、IL-6、TNF-α和CRP均有显著增高,而肿瘤负荷指标血β2-MG、LDH、铁蛋白也明显增高,此外患者ECOG积分、Ann-Arbor Ⅲ-Ⅳ期比例均明显增高,与Dlouhy等[3]的研究结果一致。(3) 在高IPI分期患者中,炎性指标sIL-2r、IL-6、CRP和肿瘤负荷指标均明显增高。这一结果提示患者疾病越高危,体内的肿瘤负荷越重,机体炎症反应越激烈。(4) 炎症指标CRP、炎性因子sIL-2r、IL-6、TNF-α与肿瘤负荷指标血LDH和β2-MG均存在明显相关性,提示体内肿瘤负荷越高,炎症反应越激烈,患者发热、盗汗、体质量减轻的症状越明显。CRP与3种炎性因子sIL-2r、IL-6、TNF-α和3种肿瘤负荷指标均有显著相关性,肿瘤负荷下降时,CRP则同步降低,而其检测方法快速简便低廉,可作为监测肿瘤负荷和炎症反应的有效指标。
本研究结果显示,合并B组症状和高IPI分期的DLBCL患者血清sIL-2r水平明显增高,与文献报道一致。IL-2r由与膜结合的α、β、γ 3个亚基和可溶性的IL-2rα组成,在T细胞、B细胞和NK细胞上都有表达。Sakai等[7]发现在DLBCL和滤泡淋巴瘤中,肿瘤内巨噬细胞分泌的基质金属蛋白酶-9能够裂解膜结合IL-2rα,从而引起血清可溶性sIL-2r水平增高[7]。在B细胞淋巴瘤中,血清sIL-2r在DLBCL[8]、滤泡淋巴瘤[9-11]、套细胞淋巴瘤[12]、成人T细胞淋巴瘤[13]患者中均显著增高,并与预后不良相关。Yang等[14]研究发现,IL-2r能够促进IL-2信号传递,通过诱导T细胞向Foxp3+的调节性T细胞表达,从而抑制了淋巴瘤内T细胞的活化和增殖。这也可能是炎性因子不能消灭肿瘤细胞,却成为引起患者发热、盗汗和消瘦的原因之一。在治疗合并B组症状患者的方案选择中,需要加强抗炎的治疗策略。
Dlouhy等[3]研究发现,新发DLBCL患者血清sIL2-R、IL-6和TNF-α的水平增高与患者生存期缩短及早期死亡密切相关。本研究由于历时较短,随访时间不够长,暂时还未纳入患者治疗前后数据对比分析及生存率和总体存活时间的数据。此外,因纳入病例数量不多,研究结果存在偏倚可能,有些结果与已报道的研究不完全一致,今后需扩大病例数量及对比治疗前后患者相关数据,从而得出更加可信的结论。
[1] CHARBONNEAU B, MAURER M J, ANSELL S M, et al. Pretreatment circulating serum cytokines associated with follicular and diffuse large B-cell lymphoma: a clinic-based case-control study[J]. Cytokine, 2012,60(3): 882-889.
[2![]() STIFTER S,
STIFTER S, ![]() B, et al. Serum IL-6, IL-8, IL-10 and beta2-microglobulin in association with International Prognostic Index in diffuse large B cell lymphoma[J]. Tumori, 2008,94(4): 511-517.
B, et al. Serum IL-6, IL-8, IL-10 and beta2-microglobulin in association with International Prognostic Index in diffuse large B cell lymphoma[J]. Tumori, 2008,94(4): 511-517.
[3] DLOUHY I, FILELLA X, ROVIRA J, et al. High serum levels of soluble interleukin-2 receptor (sIL2-R), interleukin-6 (IL-6) and tumor necrosis factor alpha (TNF) are associated with adverse clinical features and predict poor outcome in diffuse large B-cell lymphoma[J]. Leuk Res, 2017,59: 20-25.
[4] 朱宏丽,汪月增,韩小萍.恶性淋巴瘤患者血清中IL-2、sIL-2R、IL-6、IL-8和TNFα的测定[J].中华血液学杂志,1998,19(2): 85-88.
[5] 魏征,施淼颉,邹善华,等.合并乙型肝炎病毒感染对弥漫大B细胞淋巴瘤患者血清TNF-α、sIL-2r、IL-6及IL-10水平的影响[J].中国临床医学,2017,24(3): 343-347.
[6] SHI Q, SHEN R, WANG C F, et al. Pretreatment liver injury predicts poor prognosis of DLBCL patients[J]. Mediators Inflamm, 2017,2017: 7960907.
[7] SAKAI A, YOSHIDA N. The role of tumor-associated macrophages on serum soluble IL-2R levels in B-cell lymphomas[J]. J Clin Exp Hematop, 2014,54(1): 49-57.
[8] MORITO T, FUJIHARA M, ASAOKU H, et al. Serum soluble interleukin-2 receptor level and immunophenotype are prognostic factors for patients with diffuse large B-cell lymphoma[J]. Cancer Sci, 2009,100(7): 1255-1260.
[9] UMINO K, FUJIWARA S I, IKEDA T, et al. Prognostic value of the soluble interleukin-2 receptor level after patients with follicular lymphoma achieve a response to R-CHOP[J]. Hematology, 2017,22(9): 521-526.
[10] KUSANO Y, YOKOYAMA M, TERUI Y, et al. High pretreatment level of soluble interleukin-2 receptor is a robust prognostic factor in patients with follicular lymphoma treated with R-CHOP-like therapy[J]. Blood Cancer J, 2017,7(9): e614.
[11] MIR M A, MAURER M J, ZIESMER S C, et al. Elevated serum levels of IL-2R, IL-1RA, and CXCL9 are associated with a poor prognosis in follicular lymphoma[J]. Blood, 2015,125(6): 992-998.
[12] SONBOL M B, MAURER M J, STENSON M J, et al. Elevated soluble IL-2Rα, IL-8, and MIP-1β levels are associated with inferior outcome and are independent of MIPI score in patients with mantle cell lymphoma[J]. Am J Hematol, 2014,89(12): E223-E227.
[13] KOMIYA I, TOMOYOSE T, GEN O C, et al. Low level of serum HDL-cholesterol with increased sIL-2R predicts a poor clinical outcome for patients with malignant lymphoma and adult T-cell leukemia-lymphoma[J]. Cytokine, 2018,105: 57-62.
[14] YANG Z Z, GROTE D M, ZIESMER S C, et al. Soluble IL-2Rα facilitates IL-2-mediated immune responses and predicts reduced survival in follicular B-cell non-Hodgkin lymphoma[J]. Blood, 2011,118(10): 2809-2820.