子宫内膜息肉是一种妇科常见病,发病率约25%[1]。育龄期及绝经后女性均可发病,部分患者无临床症状,部分患者有月经失调、非经期出血、绝经后子宫出血等临床表现[2],同时该病也是造成女性不孕症的主要原因之一[3]。子宫内膜息肉本质上是由子宫内膜腺体和纤维间质局限性增生隆起而形成的带蒂瘤样病变[4],发病原因及机制不清,但是目前普遍认为子宫内膜息肉是子宫内膜癌的风险因素之一,其恶变率为0.5%~3%[1]。对于有生育要求的女性,子宫内膜息肉影响胚胎着床,导致不孕[5];部分患者因内膜息肉导致月经淋漓不尽或非经期出血,影响生活质量,故临床对子宫内膜息肉的治疗及处理相对积极。超声检查无创并且快速有效地诊断子宫内膜息肉,为临床诊治提供依据。本研究选取同济大学附属第一妇婴保健院超声检查提示为子宫内膜息肉且病史资料完备的患者262例,回顾性分析其超声图像、病理诊断,总结经验,以期提高超声诊断率,为临床提供可靠依据。
1 资料与方法
1.1 一般资料
回顾2016年1月—2017年10月我院超声科通过经阴道超声检查诊断为子宫内膜息肉的患者,筛选其中262例接受宫腔镜手术并获得病理诊断的患者纳入本研究。年龄23~72岁,无症状患者115例,异常子宫出血108例,不孕症39例,其中绝经患者11例,9例无症状,2例绝经后出血。
1.2 方法
育龄期患者均于月经周期第5~7天进行超声检查,检查设备PHILIPS HD15彩色超声诊断仪,使用腔内探头(探头型号: C8-4V)。患者检查前排空膀胱,取膀胱截石位,常规进行子宫纵横切面连续扫查,检查双侧附件区及盆腔,记录子宫及卵巢大小,内膜厚度,息肉内部回声、形态、大小、单发与多发,并利用彩色多普勒超声观察息肉内部的血流信号,图像留取存档。随访所有病例的术后病理诊断结果,进行对比分析。
1.3 诊断
子宫内膜息肉常见的超声表现为均匀的高回声或中高回声团,边界清晰,呈水滴状或舌状,单发或者多发,大小不一,较小的息肉通常不影响内膜连续性,息肉较大时可致宫腔连续性中断,或推挤正常宫腔线,见图1。一些子宫黏膜下肌瘤超声下表现与子宫息肉较相似,宫腔内探及中高回声,边界较清晰,见图2。子宫内膜息肉的病理特点[4]: 由子宫内膜腺体和含胶原纤维的间质组成,表面被覆立方形或低柱形内膜上皮,见图3。
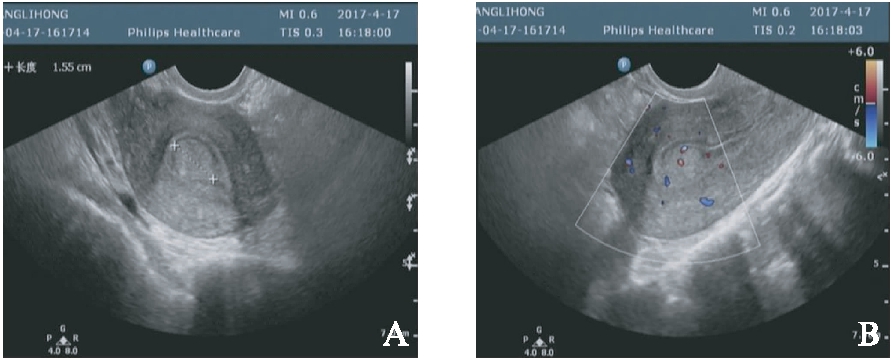
图1 子宫内膜息肉的超声表现
Fig.1 Ultrasonic appearance of endometrial polyp
A: 二维超声图像,病灶呈水滴样中高回声,边界清晰;B: 彩色多普勒超声图像,病灶内见短条状血流信号

图2 子宫黏膜下肌瘤呈息肉样的超声表现
Fig.2 Ultrasonic appearance of submucosal fibroid similar to endometrial polyp
A: 二维超声图像,病灶呈舌状高回声,边界清晰;B: 彩色多普勒超声图像,病灶内见短条状血流信号
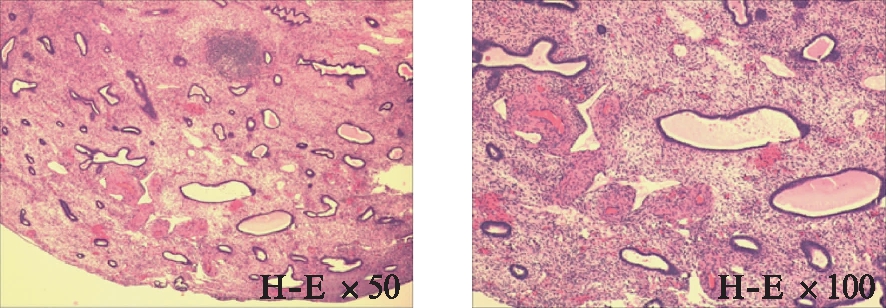
图3 子宫内膜息肉的病理表现
Fig.3 Pathological manifestation of endometrial polyp
子宫内膜息肉由子宫内膜腺体和间质组成,表面被覆一层立方或低柱状上皮, 腺体大小不一,间质纤维化,可见厚壁血管
1.4 统计学处理
采用SPSS 22.0统计学软件进行分析,计量资料以![]() 表示,组间比较用t检验,计数资料比较用χ2检验,采用多因素Logistic回归分析影响超声与病理诊断符合率的因素。P<0.05为差异有统计学意义。
表示,组间比较用t检验,计数资料比较用χ2检验,采用多因素Logistic回归分析影响超声与病理诊断符合率的因素。P<0.05为差异有统计学意义。
2 结果
2.1 超声检查结果
262例患者均由超声初步诊断为子宫内膜息肉,病灶最大者(以最大径线计)31 mm,最小者3 mm;超声提示单发息肉240例,多发22例;彩色多普勒超声探及血流信号者155例。25例伴多发性子宫肌瘤或较大子宫肌瘤或者子宫腺肌症者,子宫体积异常增大,余患者子宫大小正常。
2.2 病理诊断结果
262例病例中,病理诊断子宫内膜息肉228例,超声与病理诊断符合率87%,其中1例息肉腺体复杂性增生;34例误诊,其中1例为子宫内膜复杂性增生过长,3例为黏膜下子宫肌瘤,30例正常子宫内膜,包括29例增生反应内膜和1例分泌反应内膜。
2.3 子宫内膜息肉与正常子宫内膜超声图像对比
本研究将228例病理诊断为子宫内膜息肉的病例(息肉组)与30例病理诊断为正常子宫内膜的病例(正常组)超声图像进行比较,结果见表1。病灶大小、超声检查时子宫内膜厚度,病灶内部回声等两组间差异均无统计学意义(P>0.05)。息肉组204例病灶边界清晰,而正常组边界清晰者仅12例,差异有统计学意义(P<0.05)。息肉组病灶内探及血流信号者146例,而正常组仅7例,23例未探及血流信号,差异有统计学意义(P<0.05)。
2.4 超声与病理诊断符合率的多因素Logistic回归分析
将患者年龄、是否有伴随症状、病灶大小、单发与否、超声检查时内膜厚度、病灶内回声均匀与否、边界清晰与否、内部有无血流信号等进行多因素回归分析,结果提示年龄是降低诊断符合率的因素(OR=0.923,95%CI: 0.862~0.989),年龄越大,诊断符合率越低。病灶边界清晰(OR=10.544,95%CI: 4.249~26.167),病灶内探及血流信号(OR=4.816,95%CI: 1.856~12.501)是提高诊断符合率的因素,见表2。超声提示病灶边界清晰、内探及血流信号的病例,其超声与病理诊断符合率高。
表1 病理诊断为子宫内膜息肉组与正常子宫内膜组比较
Tab.1 Comparison of characteristics on endometrial polyps and normal endometrium by sonography

组别n病灶大小/mm子宫内膜厚度/mm病灶回声边界血流均匀不均清晰不清可见未见子宫内膜息肉22811.75±4.629.34±4.62209192042414682正常子宫内膜3010.40±4.379.00±3.392551218723
*P<0.05
表2 子宫内膜息肉诊断相关因素分析
Tab.2 Multivariate logistic regression analysis of endometrial polyps
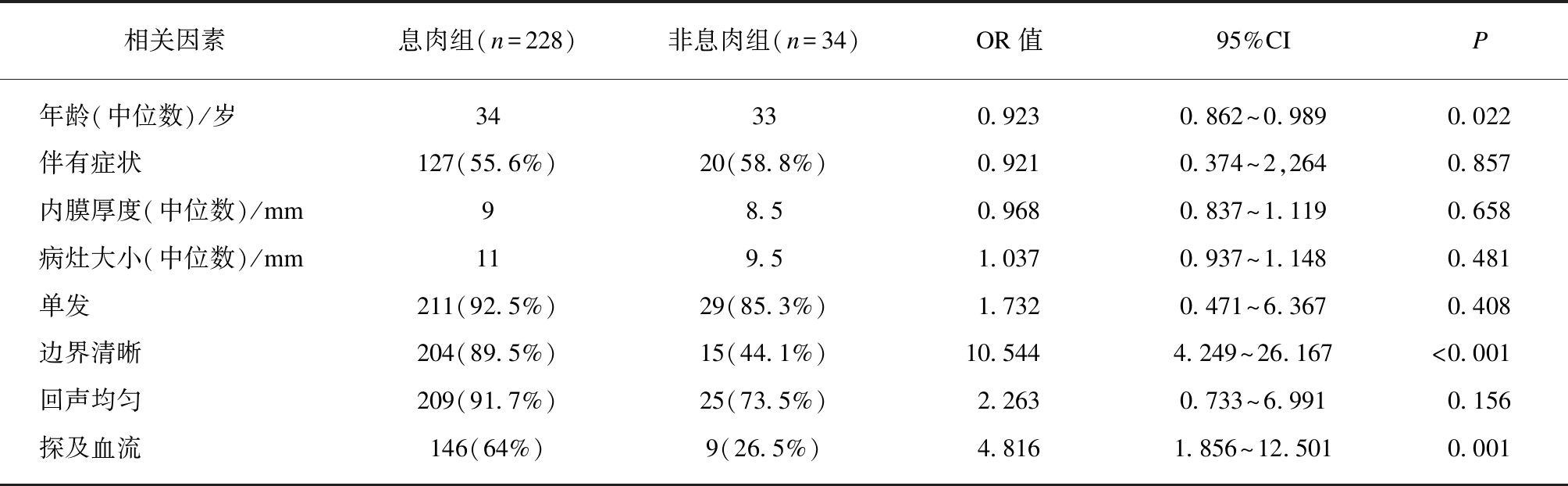
相关因素 息肉组(n=228)非息肉组(n=34)OR值95%CIP年龄(中位数)/岁34330.9230.862~0.9890.022伴有症状127(55.6%)20(58.8%)0.9210.374~2,2640.857内膜厚度(中位数)/mm98.50.9680.837~1.1190.658病灶大小(中位数)/mm119.51.0370.937~1.1480.481单发211(92.5%)29(85.3%)1.7320.471~6.3670.408边界清晰204(89.5%)15(44.1%)10.5444.249~26.167<0.001回声均匀209(91.7%)25(73.5%)2.2630.733~6.9910.156探及血流146(64%)9(26.5%)4.8161.856~12.5010.001
3 讨 论
子宫内膜息肉是妇科常见病种之一,其发病机制仍不明确。目前认为其发病与子宫内膜受雌激素刺激,而无孕激素拮抗有关,是一种雌激素依赖性疾病[6]。同时,炎症、高血压、肥胖、糖尿病等都是子宫内膜息肉的危险因素[7]。因异常子宫出血而就诊的患者中,子宫内膜息肉最为常见[8]。本研究中因异常子宫出血而就诊的患者比例高达41.2%。子宫内膜息肉也是造成女性不孕症的主要原因之一。在本研究中,不孕症患者比例为14.9%。子宫内膜息肉是一种良性病变,但有恶变可能,但本研究仅发现1例子宫内膜息肉腺体复杂性不典型增生。综上原因,临床上处理子宫内膜息肉比较积极,需要快速、廉价、受干扰因素少,且准确率高的检查方法,为临床诊治提供可靠依据。
正常子宫内膜随着雌孕激素水平周期性变化,内膜增生、腺体增长扭曲会在宫腔内形成息肉状结节,因此超声常常探及不均匀增厚的子宫内膜,与子宫内膜息肉难以区分,这也是误诊的重要原因。因此,超声检查应在月经刚刚结束时进行,子宫内膜处于增生期且较薄,可以最大限度避免干扰。
本研究将子宫内膜息肉病例与正常子宫内膜的病例超声图像进行对比,结果发现: 息肉组病灶边界清晰比例89.5%,而正常组病灶边界清晰比例仅40%,两组间差异有统计学意义。同时彩色多普勒超声发现,息肉组高达64%的病例可探及血流信号,而正常组仅23.3%。因此,超声提示病灶边界清晰且探及血流信号时,做出子宫内膜息肉诊断的准确率更高。
本研究将患者年龄、临床症状及病灶的超声表现等因素进行相关分析,发现年龄是影响子宫内膜息肉超声与病理诊断符合率的因素之一,随着年龄增长,诊断符合率下降。病灶边界清晰,病灶内探及血流信号是提高诊断符合率的因素,这与前述组间对比结果相似,提示在进行检查时应仔细观察病灶边界及内部血流,同时应考虑患者的年龄因素。
本研究中3例黏膜下子宫肌瘤超声误诊为子宫内膜息肉,回顾图像发现,其超声表现均与子宫内膜息肉相像,这也是误诊的重要原因[9]。值得注意的是,3例患者均合并多发性子宫肌瘤,且病灶相对较大,这提示遇到合并多发性子宫肌瘤的患者,尤其是病灶相对较大时,应仔细鉴别[10]。1例病理诊断为子宫内膜复杂性增生过长,超声表现为宫腔内团状中低回声,边界不清晰,未见宫腔线受推挤,彩色多普勒超声未探及血流信号。子宫内膜增生过长超声表现通常内膜均匀增厚,双侧内膜对称,宫腔线居中,因此鉴别时应仔细观察双侧内膜是否对称及宫腔线是否受到推挤。
综上所述,本研究中超声与病理诊断相符率87%,充分说明经阴道多普勒超声诊断子宫内膜息肉诊断率高,且操作无创、便捷、费用低,可以为临床医生提供快速有效的诊断依据。同时,超声医生要切实以超声图像为诊断基本依据,多切面观察,尤其重视病灶边界及血流情况,同时充分了解患者年龄、病史等因素,排除干扰因素,作出正确判断。
[1] BEN-ARIE A, GOLDCHMIT C, LAVIV Y, et al. The malignant potential of endometrial polyps[J]. Eur J Obstet Gynecol Reprod Biol, 2004,115(2): 206-210.
[2] 刘雨声,郭银树,段华,等.绝经期子宫内膜息肉临床特点分析[J].中国微创外科杂志,2017,17(7): 627-629.
[3] SHARMA M, TAYLOR A, MAGOS A. Management of endometrial polyps: a clinical review[J]. Rev Gynaecol Pract, 2004,4(1): 1-6.
[4] 谢红宁.妇产科超声诊断学[M].北京: 人民卫生出版社,2005: 225.
[5] 任奇志.子宫内膜息肉对不孕患者临床妊娠的影响分析[J].临床医药文献电子杂志,2017,4(49): 9541.
[6] KILICDAG E B, HAYDARDEDEOGLU B, COK T, et al. Polycystic ovary syndrome and increased polyp numbers as risk factors for malignant transformation of endometrial polyps in premenopausal women[J]. Int J Gynaecol Obstet, 2011,112(3): 200-203.
[7] 黄海英.子宫内膜息肉发病相关高危因素的临床调查分析[J].中国医药科学,2018,8(18): 167-170,192.
[8] 唐华栋,王慧英,郝增平,等.子宫内膜息肉与异常子宫出血的相关特点分析[J].中国妇产科临床杂志,2014,15(1): 29-32.
[9] 新瑜,吴献.超声对子宫内膜息肉和黏膜下小肌瘤的鉴别诊断价值[J].中国现代医药杂志,2015,17(3): 82-84.
[10] 刘方方,贺其志,朱慧庭.子宫静脉内平滑肌瘤病病理特征[J].同济大学学报(医学版),2018,39(2): 90-93,98.