宫颈癌是最常见的妇科恶性肿瘤之一,发病率位于女性恶性肿瘤第2位,仅次于乳腺癌。据统计,2013年全球新发宫颈癌病例约52.8万,发展中国家约占其中的70%,每年大约27.5万名妇女死于宫颈癌。宫颈癌有较长的癌前病变期,因此初筛在早期诊断和治疗宫颈癌前病变、改善宫颈癌预后方面具有极其重要的临床价值。宫颈癌的筛查方法历经变革,目前HR-HPV(high risk human papilloma virus, HR-HPV)联合宫颈脱落细胞学检测(thinprep cytology test, TCT)是较为公认的初筛方式[3-4]。
TCT技术是应用于妇女宫颈癌筛查的一项先进技术,然而,TCT也存在一些弊端,诸如价格较贵、保存期短(只有21d)、检测多个指标需要重复制片等。细胞蜡块具有价格低廉、操作简便、可长期保存、制片便捷等优势,研究认为细胞蜡块是行之有效的筛查、诊断手段,尤其应用于胸腹水的病理学诊断。国外研究发现,同时检测宫颈脱落细胞中Ki-67和P16INK4的表达,对CIN2/3的敏感性和特异性分别为91.9%和82.1%,对CIN3及以上病变的敏感性和特异性分别为96.4%和76.9%,该方法能够提高宫颈癌前病变的检出率并缩短人员培训周期,适宜用于宫颈癌的大人群初筛[7-8]。
本课题拟首先探索将细胞蜡块制片技术应用于宫颈脱落细胞的临床可行性、摸索其相关实验条件;其次,探索细胞蜡块制片对比现行TCT制片病理诊断的可行性;最后,对比细胞蜡块制片与TCT制片IHC检测Ki-67、P16INK4的差异,综合评估宫颈脱落细胞蜡块制片用于宫颈病变初筛的临床可行性。
1 资料与方法
1.1 一般资料
收集2017年1月—2017年11月在同济大学附属第一妇婴保健院进行宫颈TCT检查,并有宫颈活组织病理诊断的宫颈TCT样本共120例,分别为未见上皮内病变或恶性细胞(negative for intraepithelial lesion or malignancy, NILM)、低级别鳞状上皮内病变(low-grade squamous intraepithelial lesion, LSIL)、高级别鳞状上皮内病变(high-grade squamous intraepithelial lesion, HSIL)及鳞状细胞癌(squamous cell carcinoma of cervix, SCC)组,每组各30例,TCT与宫颈活组织样本均由2名高年资病理医师确诊。患者年龄24~67岁,平均(40.55±0.93)岁,排除其他恶性肿瘤疾病史,临床及病理资料完整。
1.2 主要材料及试剂
苏木精及伊红(H-E)染料购自上海威奥生物科技有限公司,兔单克隆抗体Ki-67购自美国Abcam公司,兔单克隆抗体P16INK4购自美国Proteintech公司,抗体稀释液及聚合HRP标记抗兔IgG购自上海威奥生物科技有限公司,DAB显色剂购自美国Cell Signaling公司。
1.3 方法
1.3.1 宫颈脱落细胞的收集 窥器暴露宫颈外口,使用TCT宫颈刷外缘抵住宫颈口,顺时针旋转5~7周,采集宫颈移行带脱落细胞,保存液瓶身标注患者姓名、样本采集日期。
1.3.2 TCT制片及巴氏染色 使用ThinPrep2000全自动细胞检测仪(美国)制作白片,制片后剩余TCT样本常温保存,于1周内进行细胞蜡块的制作。白片使用苏木精染色20min,自来水冲洗至水色变清(约10s),1%盐酸乙醇分化2s,70%、80%、95%乙醇逐级脱水各1min,橙黄G6浸3min,95%乙醇Ⅰ、Ⅱ各1min;EA50液浸5min,95%乙醇Ⅰ、Ⅱ各1min;无水乙醇Ⅰ、Ⅱ各1min;二甲苯Ⅰ、Ⅱ透明各1min,即刻中性树脂封片。
1.3.3 细胞蜡块制作 收集TCT保存液剩余标本约10mL于50mL离心管中,离心半径10cm,3000r/min,离心15min;小心弃上清液,加入10%中性缓冲福尔马林固定液10倍于沉淀物的量,用吸管轻轻吹打,静置、固定12h。再次3000r/min离心15min,弃上清液,刮匙将沉淀刮至擦镜纸上,取另一张擦镜纸小心吸除多余液体后,将沉淀物集中于擦镜纸中,折叠包裹放入包埋盒中;脱水(方案1: 分别置于50%、60%、70%、80%、90%乙醇、95%乙醇Ⅰ、95%乙醇Ⅱ各20min、无水乙醇Ⅰ、无水乙醇Ⅱ各10min;方案2: 分别置于50%、60%、70%、80%、90%乙醇、95%乙醇Ⅰ、95%乙醇Ⅱ、无水乙醇Ⅰ、无水乙醇Ⅱ各30min);吸水纸吸干乙醇后置于50℃二甲苯Ⅰ、二甲苯Ⅱ各5min,浸腊Ⅰ、Ⅱ、Ⅲ各1h,常规石蜡包埋制备蜡块。
1.3.4 细胞蜡块切片及H-E染色 将细胞蜡块均行常规3μm组织切片并H-E染色。常规脱蜡、水化,苏木精染色10min,自来水冲洗3遍、流水冲洗5min,3%酸乙醇浸洗分化3s,流水洗15min,单蒸水浸2min,70%、80%、90%乙醇各脱水2min,伊红(醇溶性)浸3s,95%乙醇Ⅲ、95%乙醇Ⅳ脱水各5min、无水乙醇Ⅰ、无水乙醇Ⅱ各脱水5min,二甲苯Ⅰ、Ⅱ、Ⅲ各透明5min,即刻中性树脂封片。
1.3.5 IHC检测细胞蜡块制片和TCT制片中Ki-67及P16INK4的表达 采用EnVision二步法检测。常规脱蜡,放入pH值为6.0的改进型柠檬酸钠抗原修复液,盒装水浴锅中加热18min抗原修复(TCT制片不需要以上步骤,直接入95%乙醇固定5min后自来水冲洗3min)。3%H2O2避光灭活10min,pH值为7.4的磷酸盐缓冲液(PBS)漂洗3次,每次5min;分别滴加相应抗体,4℃孵育过夜。PBS漂洗3次,每次5min,聚合HRP标记抗兔IgG二抗,37℃孵育30min,二氨基联苯胺(DAB)显色,苏木精复染,常规脱水,透明、封片。
1.4 结果判读
1.4.1 H-E部分 组织学诊断参考WHO(2014)女性生殖器官肿瘤分类标准。
1.4.2 IHC部分 Ki-67、P16INK4表达情况采用半定量法判定。每张切片在高倍镜(×400)下随机选取5个视野,观察染色阳性细胞比例。以胞质中出现棕黄色或棕褐色颗粒为阳性表达。Ki-67、P16INK4免疫组化结果判读: 计数5个高倍视野或500个细胞。根据阳性范围占整个切片的百分比判读染色结果。将染色范围分为0%(阴性-),1%~25%(弱阳性+),26%~50%(中度阳性++),>50%(强阳性+++)。已知小肠组织、宫颈癌石蜡切片分别作为Ki-67、P16INK4的阳性对照,PBS代替一抗作为阴性对照。由两位病理专家双盲阅片并评分,两位专家意见不一致时请第三位病理专家阅片,最终判定免疫组化结果。
1.5 统计学处理
所有数据均用SPSS 20.0统计软件包分析。对Ki-67、P16INK4蛋白表达采用阳性率(%)进行描述,组间Ki-67和P16INK4表达阳性率的比较采用χ2检验或Fisher精确概率法,采用两相关样本率的χ2检验比较两种检测方法的阳性率是否不同。P<0.05为差异有统计学意义。
2 结 果
2.1 宫颈脱落细胞蜡块制作流程的优化方案
将收集的120例TCT保存液标本(此为经由临床常规TCT制片诊断后剩余液基保存液再次制片)依次进行TCT、细胞蜡块制片,结果有111例完成满意的TCT制片,制片成功率约为92.5%(111/120);109例成功完成细胞蜡块制片,制片成功率约为90.8%(109/120),两者差异无统计学意义(χ2=0.218,P>0.05)。在细胞蜡块制片中,本研究发现将离心后的细胞沉淀物在10%中性缓冲甲醛固定液中固定12h更易于组织回收、石蜡包埋;细胞脱水时间控制在50%、60%、70%、80%、90%乙醇、95%乙醇Ⅰ、95%乙醇Ⅱ各20min,无水乙醇Ⅰ、无水乙醇Ⅱ各10min,可保持正常细胞形态及结构,避免胞质的萎缩(图1A);用90%乙醇可满意去除含血宫颈细胞沉淀物中的红细胞,减少镜下观察的混杂因素(图1B)。
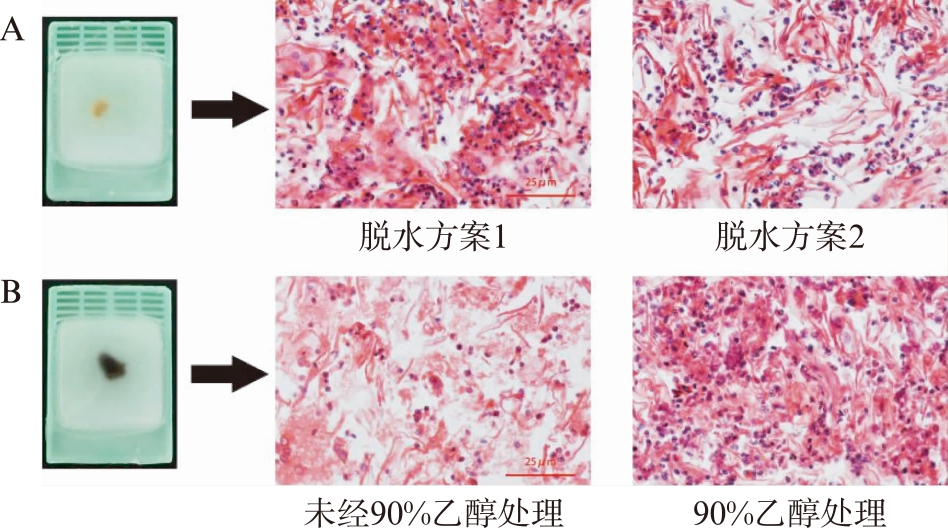
图1 宫颈脱落细胞蜡块制片在不同条件下H-E染色
Fig.1 Representative diagrams of H-E staining in cervical
exfoliated cell wax block under different conditions
A: 含血较少;B: 含血较多(标尺: 25μm)
2.2 TCT制片及宫颈脱落细胞蜡块制片H-E染色的镜下特点比较
TCT制片具有细胞片背景干净,细胞平铺,细胞结构清晰等特点;宫颈脱落细胞蜡块制片,细胞相对丰富、分布均匀,细胞结构清晰,核质分明,颜色鲜艳,保持了宫颈脱落细胞的病理学特征,见图2。
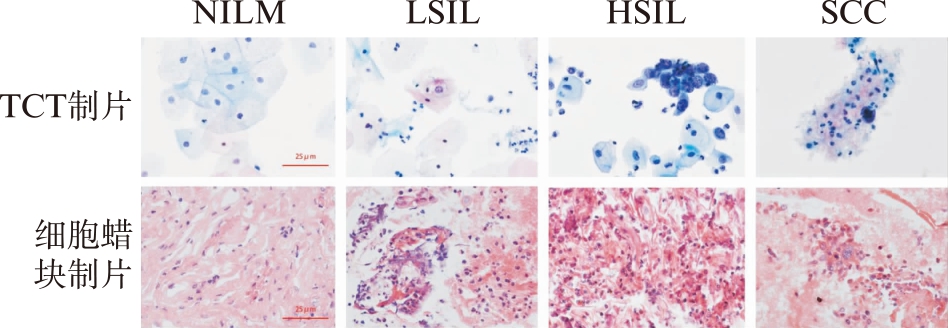
图2 宫颈脱落细胞蜡块制片对比TCT制片H-E染色
不同级别宫颈病变(标尺: 25μm)
Fig.2 Representative diagrams of H-E staining in different
levels of cervical lesions observed by cervical exfoliated
cell wax block in comparison with TCT
2.3 TCT制片和宫颈脱落细胞蜡块制片满意度及诊断符合率
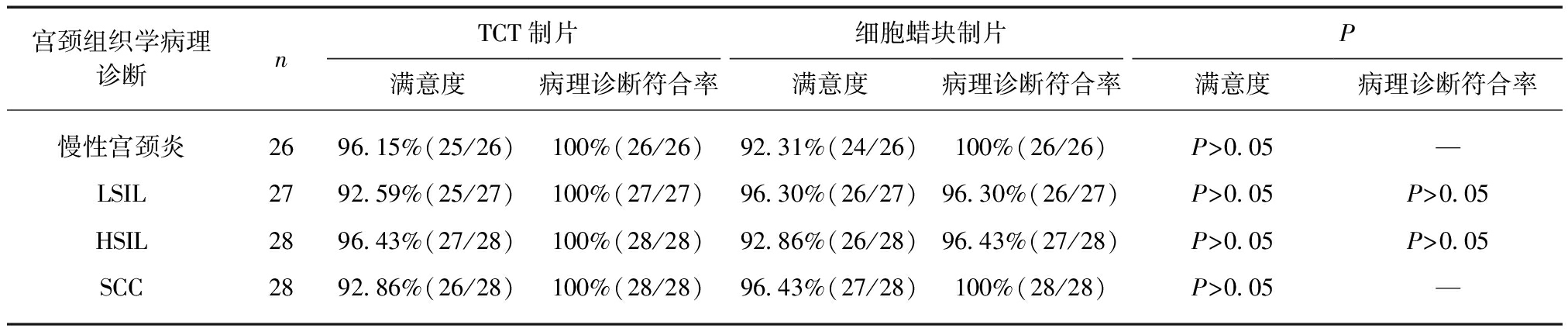
成功制备成宫颈脱落细胞蜡块的109例标本中,2名病理科医师阅片判断制片的满意度,不同宫颈病变组别中使用不同制片方式的阅片满意度差异无统计学意义(P>0.05);不同宫颈病变组别中使用不同制片方式的病理诊断符合率差异无统计学意义(P>0.05),见表1。
2.4 TCT制片及宫颈脱落细胞蜡块制片中Ki-67、P16INK4表达
TCT制片中,Ki-67在NILM、LSIL、HSIL、SCC中的阳性表达率呈现逐渐递增的趋势,各组间差异有统计学意义(P<0.05);Ki-67阳性表达率在NILM、LSIL、HSIL、SCC之间存在差异有统计学意义(P<0.05),见表2、图3。
表1 109例宫颈脱落细胞蜡块制片对比TCT制片满意度及病理诊断符合率
Tab.1 The satisfaction and pathological diagnosis coincidence rate of 109 cases of cervical exfoliated cell wax block
compared with TCT
宫颈组织学病理诊断nTCT制片细胞蜡块制片P满意度病理诊断符合率满意度病理诊断符合率满意度病理诊断符合率慢性宫颈炎2696.15%(25/26)100%(26/26)92.31%(24/26)100%(26/26)P>0.05—LSIL2792.59%(25/27)100%(27/27)96.30%(26/27)96.30%(26/27)P>0.05P>0.05HSIL2896.43%(27/28)100%(28/28)92.86%(26/28)96.43%(27/28)P>0.05P>0.05SCC2892.86%(26/28)100%(28/28)96.43%(27/28)100%(28/28)P>0.05—
宫颈脱落细胞蜡块制片中,Ki-67在NILM、LSIL、HSIL、SCC中的阳性表达率呈现逐渐递增的趋势,Ki-67阳性表达率在NILM、LSIL、HSIL、SCC之间差异有统计学意义(P<0.05),见表2、图3。
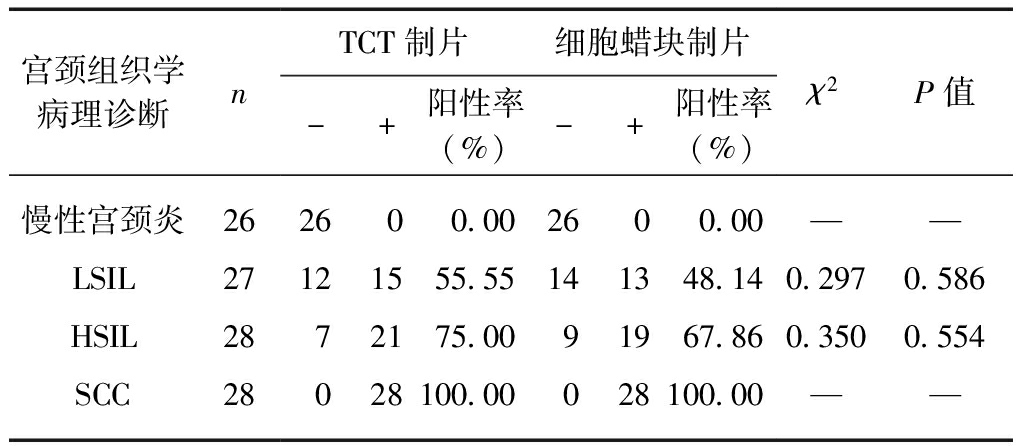
表2 宫颈脱落细胞蜡块制片组与TCT制片组Ki-67
表达情况
Tab.2 The expression of Ki-67 detected by cervical
exfoliated cell wax block in comparison with TCT
宫颈组织学病理诊断nTCT制片细胞蜡块制片-+阳性率(%)-+阳性率(%)χ2P值慢性宫颈炎262600.002600.00——LSIL27121555.55141348.140.2970.586HSIL2872175.0091967.860.3500.554SCC28028100.00028100.00——
对比TCT和宫颈脱落细胞蜡块制片方式,IHC检测Ki-67的表达阳性率,采用四格表资料的Fisher精确概率法,差异无统计学意义。因此,Ki-67在TCT组和宫颈脱落细胞蜡块组中表达对宫颈病变的检出率差异无统计学意义,见表2。
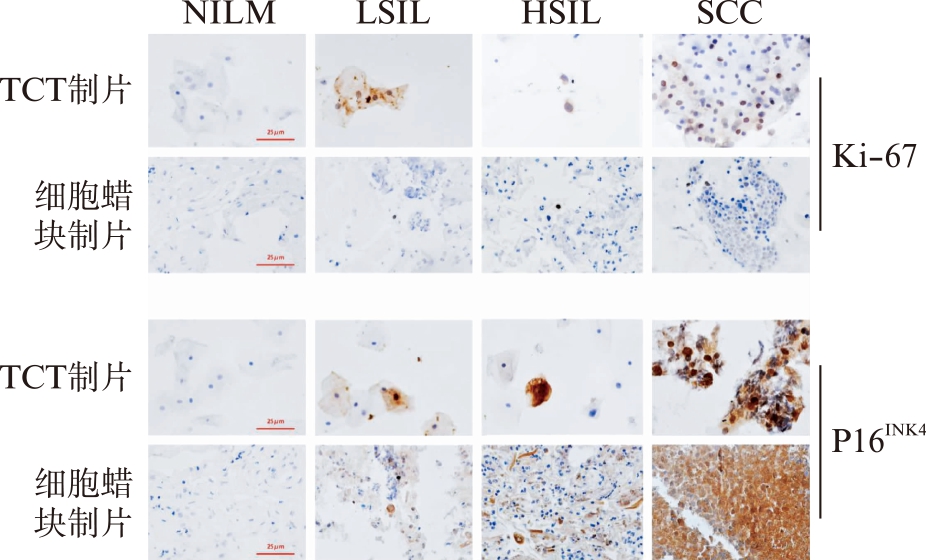
图3 宫颈脱落细胞蜡块制片对比TCT制片IHC检测
不同级别宫颈病变Ki-67及P16INK4(标尺: 25μm)
Fig.3 Representative diagram of IHC for Ki-67and P16INK4
in different levels of cervical lesions detected by cervical
exfoliated cell wax block in comparison with TCT
通过免疫组化EnVision两步法分别检测TCT制片及宫颈脱落细胞蜡块制片中P16INK4的表达情况。P16INK4阳性表达定位于胞质/核中,阳性表达呈浅棕、深棕色。
TCT制片中,P16INK4在NILM、LSIL、HSIL、SCC中的阳性表达率呈现逐渐递增的趋势,各组间差异有统计学意义(P<0.05);P16INK4阳性表达率在NILM、LSIL、HSIL、SCC之间差异有统计学意义(P<0.05),见表3、图3。
宫颈脱落细胞蜡块制片中,P16INK4在NILM、LSIL、HSIL、SCC中的阳性表达率呈现逐渐递增的趋势,各组间差异有统计学意义(P<0.05);P16INK4阳性表达率在NILM、LSIL、HSIL、SCC之间差异有统计学意义(P<0.05),见表3、图3。
对比TCT和宫颈脱落细胞蜡块制片方式,IHC检测P16INK4的表达阳性率,采用四格表资料的Fisher精确概率法,结果P16INK4在TCT组和宫颈脱落细胞蜡块组中表达对宫颈病变的检出率差异无统计学意义,见表3。
表3 宫颈脱落细胞蜡块制片组与TCT制片组P16INK4
表达情况
Tab.3 The expression of P16INK4 detected by cervical
exfoliated cell wax block in comparison with TCT
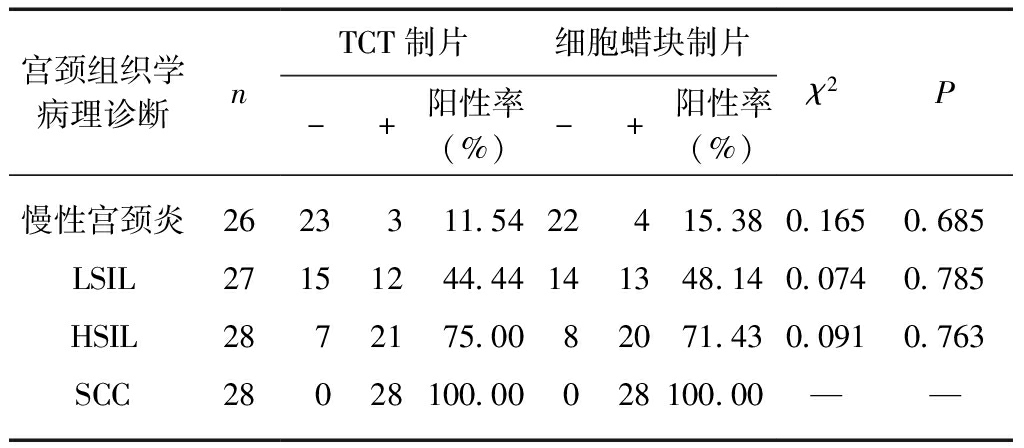
宫颈组织学病理诊断nTCT制片细胞蜡块制片-+阳性率(%)-+阳性率(%)χ2P慢性宫颈炎2623311.5422415.380.1650.685LSIL27151244.44141348.140.0740.785HSIL2872175.0082071.430.0910.763SCC28028100.00028100.00——
3 讨 论
HR-HPV持续感染是目前较为公认的宫颈癌病因,由此开发的HR-HPV疫苗作为宫颈癌的一级预防已在全球多个国家和地区应用[10]。然而HR-HPV疫苗存在价格昂贵、接种人群有限、不能涵盖所有HR-HPV且远期临床效果不确定等局限[11]。鉴于宫颈癌的发生会经历较长的癌前病变阶段,目前宫颈癌的预防仍以早期诊断和治疗宫颈癌前病变的二级预防为主要手段。
宫颈脱落细胞学病检作为宫颈癌“三阶梯”筛查中的第一阶段,是临床最常用的宫颈癌初筛方法。本研究在探索宫颈脱落细胞蜡块制作方法的过程中发现,石蜡与细胞块较易分离,导致切片时细胞块破裂,这将影响制片和阅片效果。本研究反复摸索实验条件,发现用10%中性缓冲福尔马林将细胞沉淀固定的方法,可以避免细胞块松散,极大的提高了石蜡包埋及切片制作的成功率。再者,本研究起初将宫颈组织的脱水条件应用于宫颈脱落细胞蜡块,发现细胞蜡块的细胞浆萎缩过度,细胞变形明显,极大的影响了病理诊断。本研究尝试摸索针对细胞蜡块不同的脱水条件,发现脱水方案1可以更好地保持宫颈脱落细胞的形态,更易于镜下观察细胞结构,从而提高病理医师阅片满意度。第三,宫颈病变尤其是高级别宫颈病变和宫颈癌极易接触性出血,本研究发现含血的宫颈脱落细胞在制作细胞蜡块时存在细胞不易成团、蜡块制作困难、切片后观察细胞分散、背景浑浊等弊端。本研究利用高浓度的乙醇溶液可破坏红细胞的原理[12],使用90%乙醇溶液处理含血较多的宫颈脱落细胞,处理后细胞蜡块制作成功率提高、镜下观察细胞背景清晰、病理阅片满意度显著提高。
20世纪90年代问世的TCT,是宫颈脱落细胞学检查的新技术,自1998年起,美国食品药物管理局FDA批准将TCT用于年龄在25岁以上妇女的宫颈癌初筛。广泛应用的TCT克服了既往巴氏涂片的缺点,单层细胞平铺,细胞结构清晰,背景干净,使宫颈病变的检出率进一步提高。但与此同时,TCT制作过程中材料成本较高,在推广中带来了一定的不利因素;再者,宫颈脱落细胞在TCT液基保存液中保存天数较短仅约21d,也是其应用的限制因素。国外有相关报道,细胞蜡块技术可以提高细胞病理学诊断的敏感性和特异性[13]。将TCT剩余标本制成细胞蜡块,便可以避免不能长期保存的不利因素,同时能观察到更多刷取的脱落细胞,即使较少量的脱落细胞亦可离心出较多量的沉淀物,实现组织学的重构,可实现反复、连续切片,便于行特殊染色及基因检测,为细胞学诊断提供更多的诊断依据。本实验中,宫颈脱落细胞蜡块制片较TCT制片在病理科医师阅片满意度中差异无统计学意义(P>0.05),在诊断符合率中亦差异无统计学意义(P>0.05)。
然而,TCT诊断基于宫颈脱落细胞的形态学特征,并未从更微观的分子水平评估、鉴别不同级别的宫颈病变,并且在诊断过程中由于容易受到病理科医师主观影响而产生偏倚。有学者认为,Ki-67和P16INK4阳性率的升高与宫颈病变严重程度相关性显著,通过IHC双染有助于提高细胞学诊断的敏感度[14],更有益于科学实施妇女宫颈病变的临床管理。本实验中发现Ki-67及P16INK4在NILM、LSIL、HSIL、SCC中的阳性表达率呈递增趋势,在各组中的表达具有显著的统计学差异(P<0.05),与既往研究结果一致。对比宫颈脱落细胞蜡块制片与TCT制片,IHC检测不同级别宫颈病变Ki-67及P16INK4表达均无统计学差异(P>0.05)。
综上所述,首先本实验探索出了一套宫颈脱落细胞蜡块的制作方法及条件: 使用10%中性缓冲福尔马林固定细胞块;严格控制细胞脱水时间;使用90%乙醇去除宫颈脱落细胞中的红细胞。其次,采用上述细胞蜡块制片方法在病理医师阅片满意度及诊断符合率上均不差于TCT制片。最后,宫颈脱落细胞蜡块制片对比TCT制片IHC检测Ki-67及P16INK4表达阳性率在不同级别宫颈病变中无统计学差异。基于上述研究结果,本研究认为宫颈脱落细胞蜡块制片用于宫颈病变初筛的技术方法具有临床可行性,结合其优势可考虑替代TCT制片在临床推广。
[1] SIEGEL R, DEEPA NAISHADHAM M A M S, AHMEDINJEMAL DVM PHD. Cancer statistics, 2013. Ca A Cancer J Clin, 2013,63(1): 277.
[2] 徐军,金龙妹,杨宝华,等.社区早期健康干预对提高中青年妇女宫颈癌预防知识知晓率及依从性的影响.同济大学学报(医学版),2017,38(1): 94-98.
[3] 彭书敏,王凯,詹光熙,等.MTA3通过β-hCG调控上皮性卵巢癌侵袭转移的机制研究.同济大学学报(医学版),2017,38(4): 1-5.
[4] ALLIA E, RONCO G, COCCIA A, et al. Interpretation of p16INK4a/Ki-67 dual immunostaining for the triage of human papillomavirus-positive women by experts and nonexperts in cervical cytology. Cancer Cytopathol, 2015,123(4): 212-218.
[5] 罗莹,吴荔香,詹燕美.RASSF1A,p16及Ki67在宫颈液基细胞蜡块中的表达及意义.福建医药杂志,2016,38(6): 92-96.
[6] 邱前程,卢善明,黄杰雄.胸腹水细胞块石蜡包埋及免疫细胞化学染色在胸腹水细胞病理学诊断中的价值.汕头大学医学院学报,2005,18(1): 43-44.
[7] U.S. Preventive Services Task Force. Screening for cervical cancer: recommendation statement.. Am Fam Physician, 2012,86(6): 555-559.
[8] KIRAN T, KOPP A, GLAZIER R H. Those left behind from voluntary medical home reforms in ontario, Canada. Ann Fam Med, 2016,14(6): 517.
[9] 卢朝辉,陈杰.WHO女性生殖器官肿瘤学分类(第4版)解读.中华病理学杂志,2014,43(10): 649-650.
[10] ZHU F C, HU S Y, HONG Y, et al. Efficacy, immunogenicity, and safety of the HPV-16/18 AS04-adjuvanted vaccine in Chinese women aged 18-25 years: event-triggered analysis of a randomized controlled trial: . Can Med, 2017,6(1): 12.
[11] TSUI J, GEE G C, RODRIGUEZ H P, et al. Exploring the Role of Neighborhood Socio-Demographic Factors on HPV Vaccine Initiation Among Low-Income, Ethnic Minority Girls. J Immigrant Minority Health, 2013,15(4): 732-740.
[12] 潘红然.细胞蜡块技术在胸腔积液诊断中的应用.石家庄: 河北医科大学,2016.
[13] CRAIG F, SOMA L, MELAN M, et al. MUM1/IRF4 expression in the circulating compartment of chronic lymphocytic leukemia.. Leukemia & Lymphoma, 2008,49(2): 273.
[14] LIM S, LEE M J, CHO I, et al. Efficacy of p16 and Ki-67 immunostaining in the detection of squamous intraepithelial lesions in a high-risk HPV group. Oncology Letters, 2016,11(2): 1447.