气管狭窄,是临床上经常遇到的难题,除手术外,支架植入术是治疗气管狭窄较为理想的方法[1-2]。常用的有硅酮类和金属类支架,不论是硅酮、还是金属支架,作为一种异物在气管腔内,均可引起气管组织的慢性损伤,造成管壁组织的萎缩、反应性的内膜增生甚至引起周围组织的损伤[1-3]。
生物可降解材料的发展,为解决支架机械性损伤和材料相关性并发症提供了可能。
目前,美国食品药品监督管理局(FDA)批准了数个生物可降解材料,如聚二恶烷酮(polydioxanone, PDO),聚L-乳酸(poly-L-lactic acid)和聚己内酯(polycaprolactone),制造医用材料应用于临床。近年来,也被尝试应用于气管支架的研制[4-6]。动物实验表明,可降解气管支架,也有适宜的机械性能,同样能够达到维持气道通畅,但有几个问题尚未解决,一是材料相关性并发症未完全避免,如降解产物或其碎片对气道的阻塞;二是气道分泌物较多和黏稠;三是即便是同一种材料,降解的时间有较大的差异。
尽管如此,临床上尝试应用可降解支气管支架也取得了良好的效果,如PDO支架被应用于肺移植后期或生长期儿童的气管狭窄,进一步激发了研究者的兴趣[7-9]。其最大的优势是能够自行降解,避免再次取出。
PDO材料是生物可降解材料,已经被制作成医用缝线和各类管道(血管支架、胆管支架、胃肠支架等)等应用于临床[10-12]。
先前,利用PDO制作的网状补片,应用于大面积胸壁缺损的动物实验研究,发现术后犬胸壁稳定,呼吸和运动功能良好,伤口愈合良好。证明其具有足够的机械性能和较长的降解时间,以及良好的生物相容性[13]。在另一个实验中,应用PDO材料,采用编织技术中的基本纱罗结构成功制造了多种管状支架,具有良好的机械性能、径向支撑力和弹性回缩率[14]。
本研究目的是评估PDO气管支架,与离体兔颈部气管进行力学性能的比较;同时,进行动物实验,将支架植入健康的新西兰大白兔,进行气管镜、电子显微镜扫描等观察,以期望证明具有良好的生物降解性和适用性。
1 材料与方法
1.1 PDO支架的组成及机械性能测定
支架由直径0.15~0.2mm的PDO单丝纤维,应用基本纱罗结构编织而成,再经过100℃、10min热塑型。支架内径6mm,外径7~8mm,支架长度可根据需要用超声刀进行裁剪,见图1。环氧乙烷消毒,4℃的冰箱中保存。打开后即刻使用,避免受湿度影响降解。
测定试验样品被压缩到其直径(横径)的50%时,用YG061电子测试机测定PDO支架的机械性能。测试样品长度: 3cm;温度: 20℃;湿度: 65%;压缩速度: 10mm/min。

图1 PDO气管支架
Fig.1 Polydioxanone tracheal stent
1.2 离体兔颈段气管力学性能测定
安乐死处死试验兔。分离兔颈部气管,即刻浸入生理盐水中,去除附着在管腔外的软组织,冲洗腔内的分泌物,用吸水纸吸尽水渍,送入实验室测定。考虑到气管膜部的构造,以及测定的简易性,气管直径取平均值6mm。测定方法同PDO支架测定。
1.3 动物分组
选取健康的新西兰大白兔,体质量3kg左右,由上海甲干生物科技有限公司提供。实验组(n=20)植入气管支架,对照组(n=6)进行除支架植入外的外科手术。
1.4 方法
1.4.1 动物麻醉及手术 实验兔用氯胺酮(30mg/kg)肌内注射进行麻醉,动物能够自发呼吸,不需要气管插管。外科消毒铺巾,经颈中线切开皮肤,牵开颈前肌群,暴露颈部气管,在软骨环之间,横行切开约2/3圈气管,植入气管支架,见图2。吸尽气管腔内的血液和分泌物,用5-0 PDS缝线(Ethicon)间断缝合。在手术操作中,尽量不损伤气管的血供,减少不必要的手术操作。对照组、实验组兔行气管切开后,直接用5-0 PDS缝线缝合。
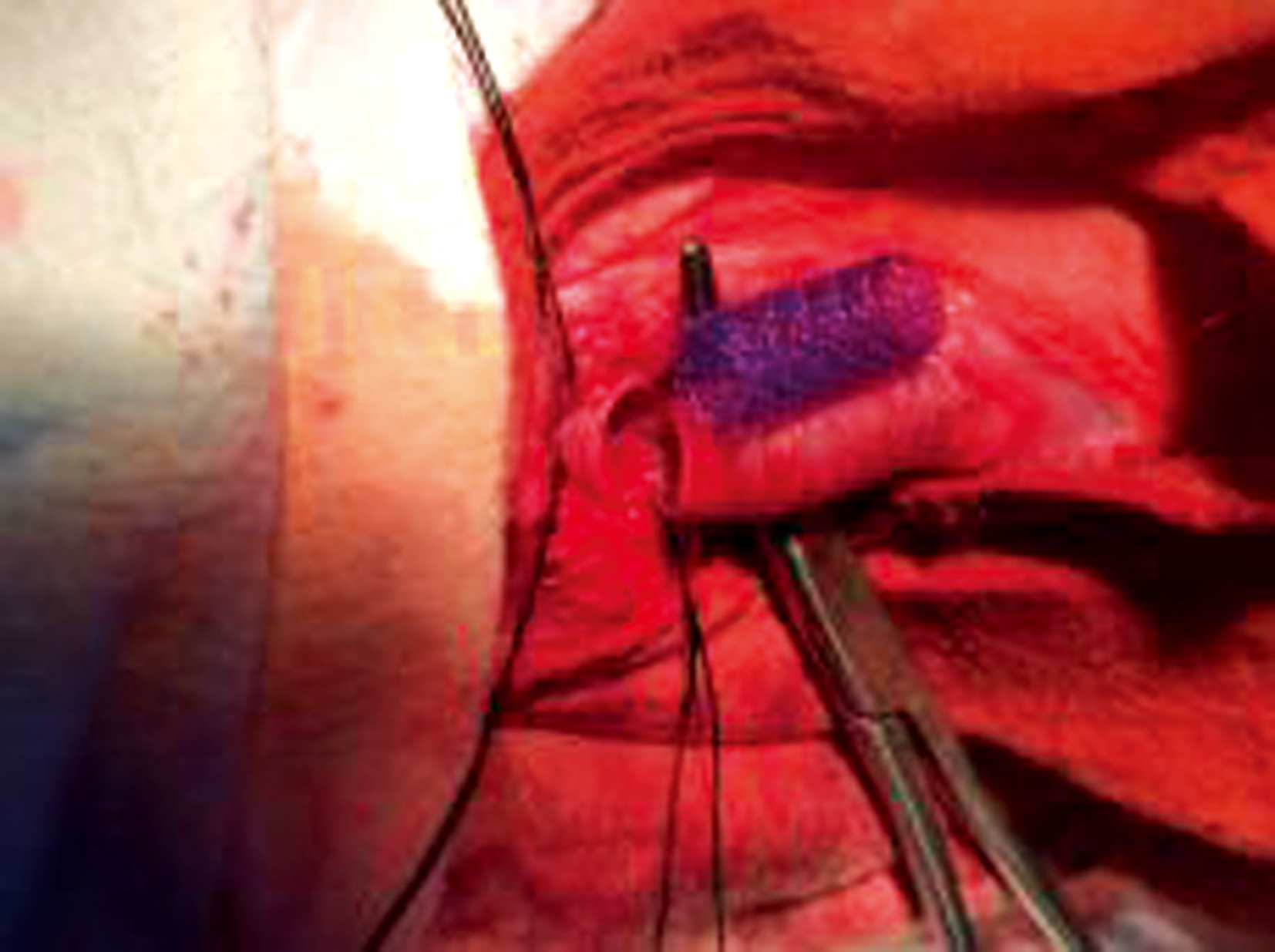
图2 气管切开和支架植入
Fig.2 Tracheotomy and stent implantation
1.4.2 术后一般情况 观察和记录实验兔的日常活动、饮食、耳温、有无喘鸣音及鼻分泌物。
1.4.3 组织学及电子显微镜检查 术后4、8、12周,每次选4只术后恢复良好的实验组兔和2只对照组兔,进行纤维气管镜检查后安乐死法处死实验兔。将实验组兔和对照组兔的颈部气管整体取下,沿膜部被打开。标本分为两部分,一部分应用4%福尔马林液固定,石蜡包埋,H-E染色,应用于光学显微镜组织学检查;另一部分,2.5%戊二醛液固定,应用于电子显微镜扫描观察。
2 结 果
2.1 PDS气管支架的力学性能和兔颈段气管力学性能
体外测定气管支架的机械性能,直径6mm PDO气管支架,径向支撑力、弹性回缩率分别是192.43cN、96.8%;体外测定离体兔颈部气管的机械性能,径向支撑力、弹性回缩率分别为157.8cN、93.42%。
2.2 术后一般情况观察
植入PDO气管支架的20只实验组兔,术后短期内多有食欲下降。1只实验兔有颈部皮下气肿,4只出现脓血性鼻分泌物,5只出现间歇性喘鸣音。术后1、2周,各有1只兔死于分泌物气道阻塞,尸检发现合并有肺部感染,但支架均完全性膨胀。术后4周,实验兔食欲和活动均正常。对照组6只兔,术后恢复良好,无皮下气肿,无脓血性鼻分泌物,无间歇性喘鸣音。
2.3 支架组实验兔术后大体标本、支气管镜、组织学及电子显微镜检查
术后发现支架固定良好,气管的管腔始终开放良好,但均有程度不一的气道分泌物。
术后1个月,大体标本可见支架两端的气管黏膜充血肿胀明显,支架表明覆盖有黏性分泌物,程度不一,支架完整,支架能够勉强与气管壁分离。支气管镜检查显示,支架完全打开,纤维完整,色泽正常,有程度不等的分泌物覆盖。组织学检查显示,支架与黏膜接触部位,有坏死和脱落的黏膜,有脓性炎症性浸润;有明显的杯状细胞增生,纤毛细胞脱落,受损;有纤维增生和新生血管生成,软骨层和外膜是正常的。电子显微镜扫描显示,支气管黏膜上覆盖有气道分泌物和炎症细胞,PDO纤维完整,但纤维外表面出现开裂,见图3。
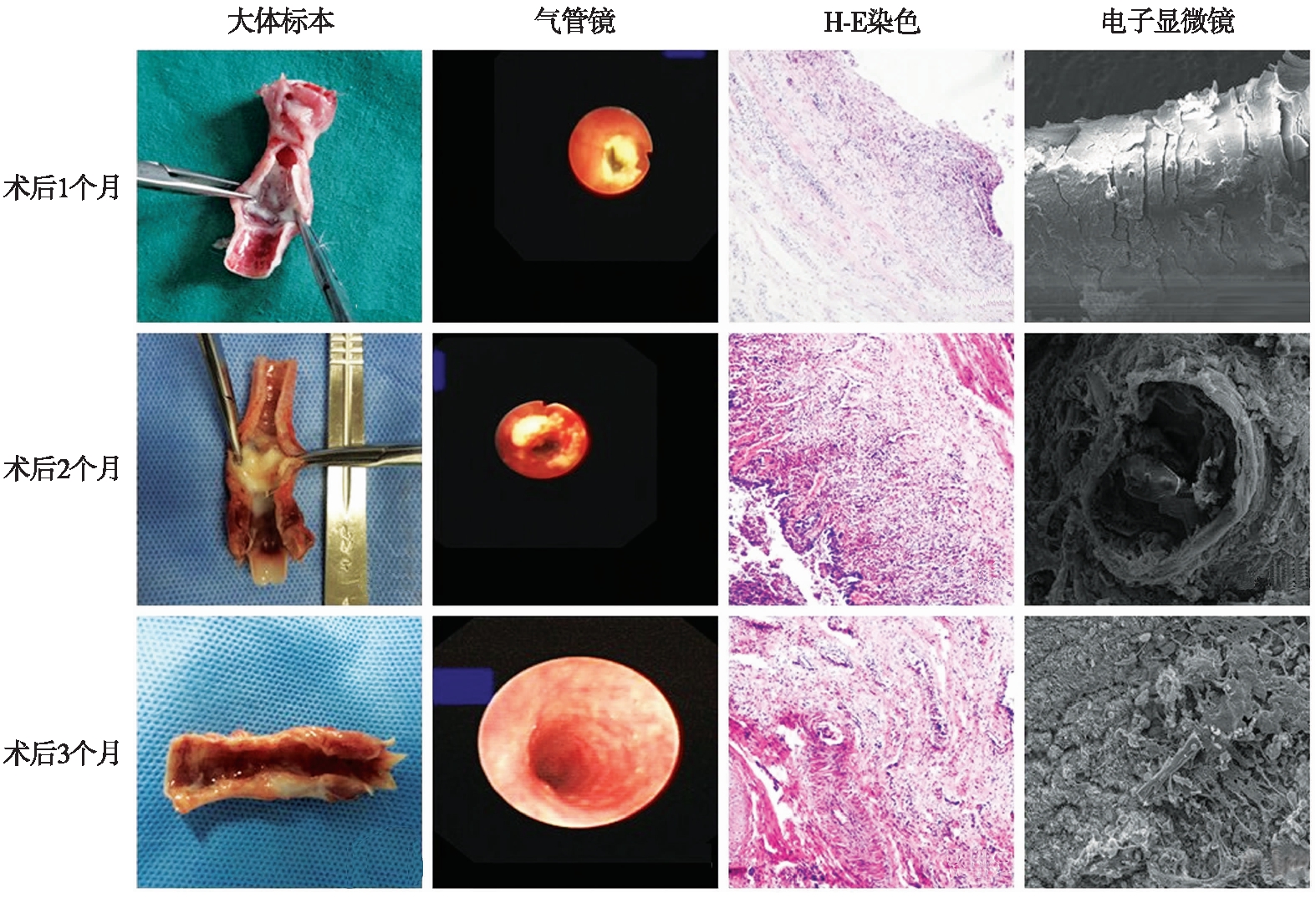
图3 实验兔术后大体标本、支气管镜、组织学及电子显微镜检查
Fig.3 General, pathological observation and bronchoscopy, electron microcopy examination after operation
术后2个月大体标本可见,支架两端的气管黏膜充血肿胀缓解,支架外观轮廓可见,被增生组织包裹,无法分离。支气管镜检查显示,支架开放,色泽改变,形态尚可见,有程度不等的分泌物覆盖。组织学检查显示,支架纤维有断裂,黏膜增生和大量分泌物,纤维肉芽组织增生明显,在某些受腐蚀的上皮区域,有慢性的淋巴细胞炎症,大量新生血管,有明显的纤维增生。电子显微镜扫描显示,可见杯状细胞增生,PDO纤维出现崩裂和断裂,部分吸收。
术后3个月,大体标本可见,支架结构肉眼观无法辨清,有明显增厚的组织,支架邻近区黏膜充血减退。支气管镜显示,未见支架纤维,气管通畅,有散在管壁增厚结节。组织学检查显示,气管黏膜增生的,有明显炎症细胞浸润,以及纤维组织增生。电子显微镜扫描显示,PDO纤维消失,在气管黏膜上可见残留的PDO分解的碎片。
对照组兔,术后1个月,大体标本未见PDS缝线,气管黏膜色泽接近正常。支气管镜检查显示,气管通畅,无明显分泌物。组织学检查和电子显微镜扫描显示正常气管黏膜。
3 讨 论
3.1 临床现象与实验结果的解释
本研究应用0.2~0.15mm管径的PDO纤维制造了生物可降解气管支架。体外力学性能测定,证实了PDO气管支架与离体颈部气管有类似的力学性能。动物实验说明了PDO气管支架的生物可降解性及机械扩张气管的功效。大体检查,光学显微镜和扫描电子显微镜的表现是相符的,也符合生物可降解材料在管腔内的代谢降解的一般规律。
本实验发现,实验兔死亡以及呼吸道并发症现象,如间歇性喘鸣音,鼻部脓血性分泌物等。支架植入后,PDO支架始终处于开放状态,支架在压迫管壁组织,造成黏膜损伤或坏死或脱落,黏性分泌物的产生,覆盖于支架上,明显减少了气道的有效管径,导致产生喘鸣音。实验兔也可能合并有肺部的感染,加重了这种气管阻塞状态。因此,也可以部分解释鼻部的脓血性分泌物的产生。当然,不能够完全排除实验兔手术耐受性差,以及早期支架产生轻微移动造成支气管黏膜破裂出血。无论上述何种情况,均值得进一步研究和改进。
其他材料制作的支架,均有其降解产物被咳出的现象,甚至于支架的碎片被送入气管的远端,造成肺部感染或堵塞[14]。Novotny等[5]认为造成支架的消失,理论上可通过咳嗽,吞咽和消化来清除碎片。本研究未发现有支架碎片的咳出,认为PDO降解具有均一性,也就是其引发的组织反应在整个支架大致处于同一水平,被肉芽组织迅速包绕和代谢,通过水解作用被降解。另外,本研究也观察到气管黏膜表面有PDO降解的微小产物,应用0.15~0.2mm 的PDO单丝纤维,即便是碎片,其降解产物更为微小,也不足以引起临床症状。
3.2 PDO气管支架的优势和特点
生物支架最大的特点,在疾病或是损伤愈合的特定时间内,能够对病变的管腔组织提供足够的机械支撑,起到扩张的作用,在达到治疗的目的后,支架自身能够被降解,不必再次从气道中取出,减少再次麻醉和手术的风险。
支架的制造,涉及材料、工艺及设计构型等。材料是影响支架力学性能的重要因素。理想的气管支架应具有如下特性: 支撑强度高、轴向收缩少、柔韧性好、扩张率较高、耐疲劳等。其中,径向支撑力最为重要。适当的径向支撑力,能够抵抗管腔及病变组织的作用力,以撑开狭窄管腔,也要适应导致管腔受压变形、扭曲的外力作用,维持支架在治疗期间不会被损坏,保证支架位置稳定,又不要引起气管黏膜的过度损害[1]。
对于气管支架的制作,尤其是孔径、孔隙率、孔隙连接等还没有公认的指标。本研究应用PDO材料进行气管支架的制造,工艺包括罗纱结构及热塑工艺后处理。气管支架的孔径控制在0.2~0.3mm,一是能够满足细胞和组织的生长,二是有利于附着固定,三是有利于分泌物的引流。因此,在编织技术中的罗纱,最有优势,能够产生足够的径向支撑力和弹性回缩率;同时,再用热塑工艺后处理,确保在植入气管腔后保证其管状的结构和外形处于稳定状态[14]。
考虑到健康兔的气管直径在5~6mm,植入后需要有一点的扩张性,本研究设计6mm管径的气管支架,能够起扩张的作用,测定的离体兔颈部气管径向支撑力为157.8cN,弹性回缩率93.42%;而应用 6mm 的PDO气管支架的相应数据分别是192.43cN、96.8%。由于气管的力学性能受多种因素的影响,本课题组推测,体内的兔颈部气管的力学性能可能会高于离体气管的测定值。但6mm的PDO气管支架的力学性能足以满足扩张的需要。但是,6mm 的PDO支架,其有效内径是5mm左右,造成了实验兔气道的轻微的狭窄,这也是设计制作的不足之处。Fu等[14]的研究表明,直径6mm、8mm、10mm气管支架产生的力学性能,是明显增加的,但是为非线性关系[14],说明若是选用管径大的PDO支架,可能或有更好的力学性能,这也是进一步开展大动物气管支架研究的基础。
本研究选择PDO制造气管支架的理由,在于其初始强度大、模量适中、柔韧性好、抗张力强,有良好的形状记忆功能;降解速度缓慢,在体内可以维持更长时间的机械强度,靠水解作用降解,组织反应小,异物反应轻[15]。PDO材料的特性,决定其较适合气管支架的研制。
本研究发现,PDO气管支架的降解与通常对PDO材料的理解的有所差别。以往对PDO材料的认识是4~6周被降解,损失大部分机械性能,其依据多来自于对缝线的研究。实质上,缝线在不同的组织环境中,其降解的半衰期也是明显不同[15]。PDO材料被制作成管状支架,Zilberman等[16]认为PDO管状结构的降解依赖于纤维的直径、支架的结构、应用环境。微生物的存在,炎性反应,低pH值可能会加速PDO的降解和快速丢失初始张力。PDO支架位于开放性腔道,处于温暖潮湿环境中,又有气流,加之细菌可繁殖,推测气管支架降解速度应该较快,而实际观察中,2个月后,支架的外观轮廓存在,机械性能有所保留,推测编织结构对延迟降解时间可能有所影响。
3.3 本研究的不足
关于自制PDO气管支架的机械性能,取决于市售的PDO单丝纤维的直径和力学性能,另一方面,也取决于支架的制造及后处理工艺。
本研究设计的是管状支架,支架的直径及编织经纬线密度所决定的孔径,是人为决定的,缺乏个性化制作,同一规格的气管支架与每一实验兔的气管壁并不是精密地贴壁,因此是否会影响其组织反应和其降解性能,并不清楚。
实验研究应用健康兔,只能够说明在健康状态下,气管支架的组织反应和生物降解,不能够推测在气管狭窄的病理状态下(如伴有肉芽肿、炎症或肿瘤状态)的组织反应和生物降解,因为只有在那种状态下才能真正反映支架的机械性能和降解性能。
体外实验来测定支架的性能,尤其是离体颈部气管的测定,干扰因素特别多,尤其是气管膜部,本研究做了近似化的处理,是个可行的方法。
应用PDO纤维制作气管支架,具有适宜的机械性能,能够起到扩张支撑气管的作用;同时,具有良好可降解性,在短期内能够被完全降解消失。在实验中产生的短暂性的呼吸症状,与支架的管径和材料性能有关,也是需要改进的方向。
【参考文献】
[1] AYUB A, AL-AYOUBI A M, BHORA FY, et al. Stents for airway strictures: selection and results[J]. J Thorac Dis, 2017,9(Suppl 2): S116-S121.
[2] CHUNG F T, CHEN H C, CHOU C L, et al. An outcome analysis of self-expandable metallic stents in central airway obstruction: a cohort study[J]. J Cardiothorac Surg, 2011,6: 46.
[3] KIM Y H, SHIN J H, SONG H Y, et al. Tracheal stricture and fistula: management with a barbed silicone-covered retrievable expandable nitinol stent[J]. AJR Am J Roentgenol, 2010,194(2): W232-W237.
[4] WANG J, BOUTIN K G, ABDULHADI O, et al. Fully biodegradable airway stents using amino alcohol-based poly(ester amide)[J]. Adv Healthc Mater, 2013,2(10): 1329-1336.
[5] NOVOTNY L, CRHA M, RAUSER P, et al. Novel biodegradable polydioxanone stents in a rabbit airway model[J]. J Thorac Cardiovasc Surg, 2012,143(2): 437- 444.
[6] LIU K S, LIU Y H, PENG Y J, et al. Experimental absorbable stent permits airway remodeling[J]. J Thorac Cardiovasc Surg, 2011,141(2): 463- 468.
[7] VONDRYS D, ELLIOTT M J, MCLAREN C A, et al. First experience with biodegradable airway stents in children[J]. Ann Thorac Surg, 2011,92(5): 1870-1874.
[8] LISCHKE R, POZNIAK J, VONDRYS D, et al. Novel biodegradable stents in the treatment of bronchial stenosis after lung transplantation[J]. Eur J Cardiothorac Surg, 2011,40(3): 619- 624.
[9] STEHLIK L, HYTYCH V, LETACKOVA J, et al. Biodegradable polydioxanone stents in the treatment of adult patients with tracheal narrowing[J]. BMC Pulm Med, 2015,15: 164.
[10] KARAKAN T, UTKU O G, DORUKOZ O, et al. Biodegradable stents for caustic esophageal strictures: a new therapeutic approach[J]. Dis Esophagus, 2013,26(3): 319-322.
[11] REPICI A, PAGANO N, RANDO G, et al. A retrospective analysis of early and late outcome of biodegradable stent placement in the management of refractory anastomotic colorectal strictures[J]. Surg Endosc, 2013,27(7): 2487-2491.
[12] PETRT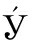 L J, BR
L J, BR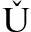 HA R, HOR
HA R, HOR K L, et al. Management of benign intrahepatic bile duct strictures: initial experience with polydioxanonebiodegradable stents[J]. Endoscopy, 2010,42(Suppl 2): E89-E90.
K L, et al. Management of benign intrahepatic bile duct strictures: initial experience with polydioxanonebiodegradable stents[J]. Endoscopy, 2010,42(Suppl 2): E89-E90.
[13] ZHENG R, YONG-WU W, YONG-XING Z, et al. Primary results of chest wall reconstruction with polydioxanone mesh on animals[J]. Eur Rev Med Pharmacol Sci, 2012,16(7): 942-948.
[14] FU B S, LI Y L, RUAN Z et al. Development and mechanical properties of a novel woven artificial tracheal stent[J]. J Donghua Univ(Eng Ed), 2014,31(5): 643- 645.
[15] BOLAND E D, COLEMAN B D, BARNES C P, et al. Electrospinning polydioxanone for biomedical applications[J]. Acta Biomater,2005,1(1): 115-123.
[16] ZILBERMAN M, NELSON K D, EBERHART R C. Mechanical properties and in vitro degradation of bioresorbable fibers and expandable fiber-based stents[J]. J Biomed Mater Res, 2005,74B(2): 792-799.