·临床研究·
【摘要】目的 探究CYP2C19基因多态性与氯吡格雷治疗脑梗死患者疗效的相关性。方法 选取我院2012年1月至2015年1月的脑梗死患者200例。根据基因型分为高、中间、弱代谢型三组。统计口服氯吡格雷前、第1天、第6天、第8周患者的血小板聚集抑制率、美国国立卫生研究院脑卒中量表(National Institute of Health stroke scale, NIHSS)评分、日常生活能力评分(Activities of Daily Living, ADL)和1年内心脑血管不良事件的发生率。结果 治疗后第1天和第6天,三组血小板聚集抑制率差异均有统计学意义(P<0.05),由高到低依次为强、中间、弱代谢型组,两两比较差异明显,第6天和第8周差异无统计学意义。治疗后1、3和6个月,三组NIHSS、ADL评分差异均有统计学意义(P<0.05),治疗效果由高到低依次为高、中间、弱代谢型组,两两比较差异明显。1年内强代谢型组心脑血管不良事件总的发生率明显低于中间和弱代谢型组,差异具有统计学意义(P<0.05)。结论 CYP2C19基因多态性与脑梗死患者氯吡格雷治疗效果与预后有关,其机制可能与代谢酶活性有关。
【关键词】脑梗死; 氯吡格雷; CYP2C19; 基因多态性
脑梗死(cerebral infarction, CI)是因脑血液供应障碍造成脑部缺血、缺氧,从而使脑组织出现局限性缺血性坏死或脑软化病变[1]。在脑梗死病理生理中血小板的活化、聚集起着重要阻作用。抗血小板聚集治疗对脑梗死患者治疗及预防具有重要的临床意义。氯吡格雷是脑梗死患者最常用的抗血小板聚集药物之一。脑梗死患者规范服用氯吡格雷,大多数患者明显受益,但仍有一部分患者临床效果欠佳,以往的研究提示药物代谢过程中涉及的基因多态性可能是一个重要因素。氯吡格雷是无活性的药物前体,需经肝CYP450代谢酶活化,才能与血小板表面P2Y12受体结合发挥作用。CYP2C19是一种从属CYP450酶亚家族的重要代谢酶[2]。CYP450酶系中多种代谢酶具有基因多态性,有文献报道,CYP2C19基因多态性引起的原因主要包括两类突变: 一类是增强酶活性的突变,另一类是降低酶活性的突变,相应其表型则有三种,即快代谢型(携带两个增强酶活性的突变位点)、慢代谢型(携带两个降低酶活性的突变位点)和中间代谢型(只携带一个降低或增强酶活性的突变位点)[3]。本研究采用血小板抑制率(impedance platelet aggregometry, IPA)来评估氯吡格雷疗效。IPA是由最大血小板聚集率(maxium agglutination of platelet, MPA)间接计算得出的指标,其数值越大代表氯吡格雷的抗血小板作用越强[4]。为探究CYP2C19基因多态性与脑梗死患者氯吡格雷疗效的相关性,本研究对200例脑梗死患者进行抗血小板聚集治疗和持续随访,现报道如下。
1.1 一般资料
经我院伦理委员会同意,选取2012年1月~2015年1月同济大学附属同济医院分院收治的急性脑梗死患者200例,其中男109例,女91例,年龄52~79岁,平均(68.3±5.2)岁。纳入标准: (1) 年龄<80岁,男女不限;(2) 首次发病,对急性脑梗死的诊断标准[5]参照《中国急性缺血性脑卒中诊治指南》(2010版);(3) 病 程<3d。排除标准: (1) 存在氯吡格雷使用禁忌者;(2) 入院前1个月内使用质子泵抑制剂、抗癫痫药、抗抑郁药、镇静催眠药、抗真菌药及其他抗血小板聚集药者;(3) 合并神经精神类疾病者;(4) 合并心肾肝等脏器严重功能损害者;(5) 有出凝血障碍者;(6) 1个月内有重大手术者;(7) 合并肿瘤、免疫系统、呼吸系统疾病及感染性疾病者;(8) 依从性差的患者;(9) 血小板计数异常者。所有患者对本次研究知情并签署同意书。
1.2 方法
1.2.1 基因多态性检测 入院后采集患者空腹静脉血5ml,通过限制性片段长度多态性聚合酶链反应(PCR-RFLP)方法进行基因检测。首先使用DNA提取试剂提取DNA,PCR扩增引物选择根据CYP2C19的核苷酸序列。扩增后按照每20μl PCR产物,添加 1μl 限制性内切酶和4μl缓冲液进行酶切,对其进行凝胶电泳后分析结果,判断基因型。而后根据患者体内CYP2C19酶活性将患者分为强代谢型组(extensive metabolizer, EM)基因型为CYP2C19*1/*1、中间代谢型组(inter mediate metabolizer, IM)基因型为CYP2C19*1/*2或*1/*3、弱代谢型组(poor metabolizer, PM)基因型为CYP2C 19*2/*2, CYP2C19*3/*3或*2/*3[6]。
1.2.2 药物治疗 200例患者均口服氯吡格雷(深圳信立泰药业股份有限公司/国药准字H20000542)治疗,口服剂量为初次300mg,24h后75mg/d维持,并禁用其他抗血小板药物、抗凝药和溶栓药,不采取介入治疗或其他非药物治疗手段。
1.2.3 IPA测定 分别于口服氯吡格雷前、服用氯吡格雷后第1、6天、第8周采集患者空腹静脉血5ml,采用光透过集合度测定(light transmission aggregometry,LTA)检测血小板的聚集功能。根据血小板聚集仪转速不同,分离产物分别为富血小板血浆和贫血小板血浆。在富血小板血浆中加入0.5ml 浓度为10mol/L的ADP。以贫血小板血浆为参照,记录光透过率的改变,取最大值为最大血小板聚集率(MPA,%)。正常参考值: 46.6%~78.8%。低于下限表明血小板聚集功能受抑制,而高于上限则表明血小板聚集功能增强。IPA=(治疗前MPA- 治疗后MPA)/治疗前MPA×100%。
1.3 观察指标
(1) 三组治疗前及治疗后第1天、第6天、第8周IPA;(2) 三组治疗前及治疗后2周、4周和8周进行NIHSS及ADL评分。(3) 三组发病后1年内脑出血、急性心肌梗死、再发脑梗死等心脑血管不良事件发生率。NIHSS评分分为意识水平、凝视、视野等15项内容,共42分,均为负向问题,得分越高神经功能缺损越严重。ADL评分分为进食、洗澡等10项日常活动,共100分,均为正向问题,得分越高生活质量越高[7]。
1.4 统计学处理
采用SPSS 22.0统计学分析软件处理,计量资料采用![]() 表示,组间比较使用方差分析、卡方检验,组内采用t检验;计数资料用频数、百分率表示,采用方差分析,以P<0.05为差异有统计学意义。
表示,组间比较使用方差分析、卡方检验,组内采用t检验;计数资料用频数、百分率表示,采用方差分析,以P<0.05为差异有统计学意义。
2.1 三组一般资料比较
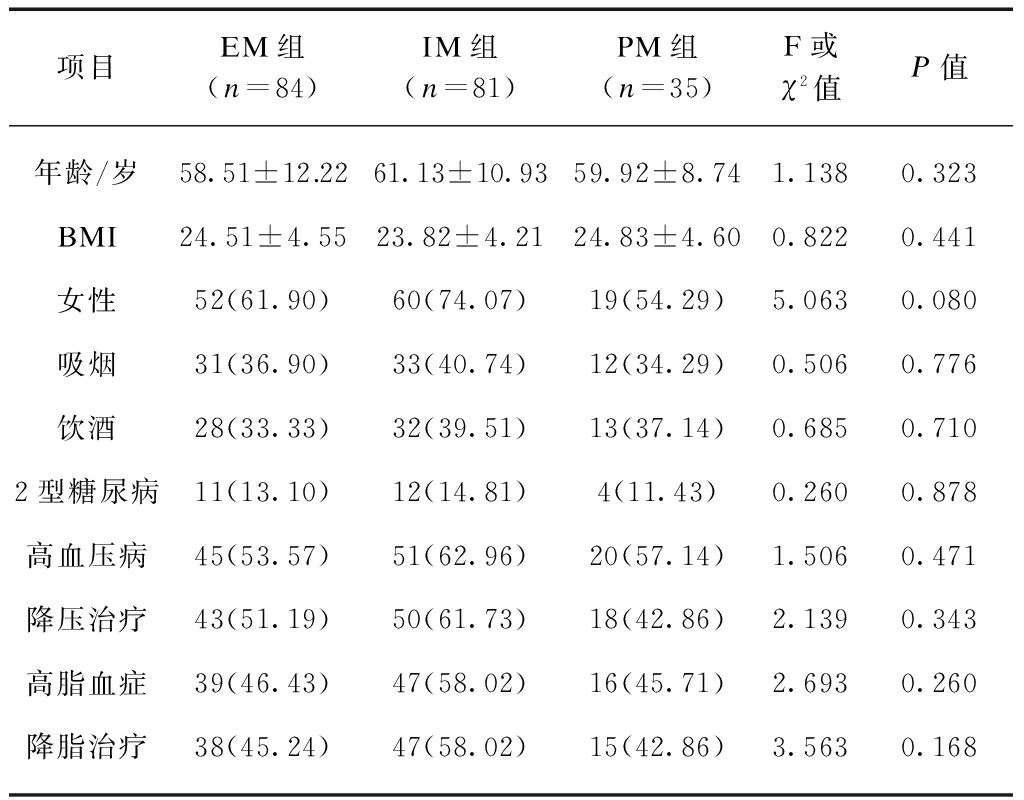
根据基因分型,200例患者中EM组84例;IM组81例,其中CYP2C19*1/*2为58例和CYP2C19*1/*3为23例;PM组35例,其中CYP2C19*2/*2为20例,CYP2C19*3/*3为12例,CYP2C19*2/*3为3例。三组在年龄、性别、体质量指数、吸烟、饮酒史及疾病史方面具有可比性,差异均没有统计学意义(P>0.05),见表1。
表1 三组一般资料比较
Tab.1 Comparison of general information in three groups![]()
项目EM组(n=84)IM组(n=81)PM组(n=35)F或χ2值P值年龄/岁58.51±12.2261.13±10.9359.92±8.741.1380.323BMI24.51±4.5523.82±4.2124.83±4.600.8220.441女性52(61.90)60(74.07)19(54.29)5.0630.080吸烟31(36.90)33(40.74)12(34.29)0.5060.776饮酒28(33.33)32(39.51)13(37.14)0.6850.7102型糖尿病11(13.10)12(14.81)4(11.43)0.2600.878高血压病45(53.57)51(62.96)20(57.14)1.5060.471降压治疗43(51.19)50(61.73)18(42.86)2.1390.343高脂血症39(46.43)47(58.02)16(45.71)2.6930.260降脂治疗38(45.24)47(58.02)15(42.86)3.5630.168
2.2 三组IPA比较
治疗前,三组患者IPA差异无统计学意义(P>0.05)。治疗后第1、6天,三组患者IPA差异具有统计学意义,由高到低依次为EM组、IM组和PM组,两两比较,差异均有统计学意义(P<0.05)。治疗后6d、8周,三组患者IPA差异无统计学意义(P>0.05)。治疗后第1、6天,治疗后8周,三组IPA均升高,组内比较,差异均有统计学意义(P<0.05),由高到低依次为EM组、IM组和PM组,两两比较,差异有统计学意义(P<0.05)。三组患者治疗后第6天和第8周差异无统计学意义(P>0.05),三组患者之间两两比较,差异有统计学意义(P<0.05),见表2。
表2 三组患者治疗前后IPA比较
Tab.2 Comparison of IPA in three groups before and after treatment ![]() ±s)
±s)

组别治疗前治疗后第1天治疗后第6天治疗后8周EM组18.35±2.2555.16±12.25#62.31±14.62#63.34±14.05#$IM组17.98±2.1746.57±11.94*#51.28±12.58*#52.24±10.08*△#PM组18.20±2.8530.14±12.82*△#32.20±10.80*△#33.65±8.57*△#$F值0.52151.97564.85080.406P值0.595<0.001<0.001<0.001
与EM组相比,*P<0.05;与IM组相比,△P<0.05;与治疗前相比,#P<0.05;与治疗后6天相比,$P>0.05
2.3 三组NIHSS和ADL评分比较
治疗前,三组NIHSS和ADL评分差异均无统计学意义(P>0.05);治疗后1、3、6个月,三组NIHSS评分差异均有统计学意义,由高到低依次为PM组、IM组和EM组,两两比较,差异均有统计学意义(P<0.05)。治疗后1、3、6个月,三组ADL评分差异均有统计学意义,由高到低依次为EM组、IM组和PM组,两两比较差异均有统计学意义(P<0.05),见表3。
表3 三组治疗前后NIHSS和ADL评分比较
Tab.3 Comparison of NIHSS and ADL scores in three groups before and after treatment ![]() ±s)
±s)

组别NIHSS评分ADL评分治疗前治疗后1个月治疗后3个月治疗后6个月治疗前治疗后1个月治疗后3个月治疗后6个月EM组14.26±5.246.56±3.65#6.06±3.12#5.88±6.23#31.45±5.6173.26±8.85#77.40±11.12#83.72±10.03#IM组14.08±4.5610.87±3.15*#10.92±3.80*#9.05±3.25*#30.12±6.2550.54±8.45*#52.32±9.14*#57.66±7.80*#PM组14.18±4.1611.95±4.38*△#11.26±4.75*△#10.86±5.26*△#31.83±5.7044.38±8.74*△#46.02±9.13*△#46.92±8.05*△#F值0.02941.51643.38814.8101.494201.917181.440285.184P值0.971<0.001<0.001<0.0010.227<0.001<0.001<0.001
与EM组相比,*P<0.05;与IM组相比,△P<0.05;与治疗前相比,#P<0.05
2.4 三组心脑血管不良事件发生率比较
出院后1年内EM组心脑血管不良事件的发生率明显低于IM组和PM组,不良事件的总数差异具有统计学意义(P<0.05),见表4。
表4 三组心脑血管不良事件情况比较
Tab.4 Comparison of cardio-cerebrovascular events in three groups [n(%)]

组别脑梗死脑出血急性心肌梗死猝死合计EM组3(3.57)0003(3.57)IM组7(8.64)2(2.47)2(2.47)1(1.23)12(14.81)*PM组6(17.14)2(5.71)1(2.86)1(2.86)10(28.57)*χ2值6.264.272.232.1114.78P值0.04370.11820.32790.34820.0006
与EM组相比,*P<0.05
氯吡格雷是临床上应用较为广泛的一种抗血小板聚集药物,充分的抑制血小板聚集可以降低心脑血管事件发生率。但其抗血小板反应存在个体差异性,临床上有4%~30%的患者服用氯吡格雷后,血小板活性并未降低,此种现象称为氯吡格雷抵抗(clopidogrel resistance, CR)。基因多态性对药物治疗影响较大[8-10]。有研究表明氯吡格雷在体内吸收、代谢和药理作用的发挥受基因多态性调节,且遗传多样性是其独立的相关因素[11]。研究表明[12]造成人群中氯吡格雷药效差异的主要原因可能是药物代谢酶的基因多态性,对氯吡格雷代谢有关的药物代谢酶比较多,目前已知的主要有CYP2C19、CYP3A4、CYP3A5、CYP2C9、CYP2B6等,而代谢氯吡格雷的关键酶普遍认为是CYP2C19。CYP2C19*1 是编码正常代谢酶酶活性的基因,而CYP2C19*2和CYP2C19*3是汉族人群中主要的突变。张海涛等[13]研究表明,CYP2C19基因多态性对氯吡格雷疗效有影响。在本次研究中,根据基因型和代谢差别,将患者分为EM、IM和PM三组,经方差分析,其组间差异并无统计学意义(P>0.05),表明年龄、性别、高血压病等一般资料与CR并无关系。MPA是血小板功能的一个检测指标,其升高时,血小板容易聚集形成血栓,数值越大形成血栓的可能性越大。而IPA是由MPA间接计算得出的指标,其数值越大代表氯吡格雷的抗血小板作用越强,此次研究中EM组优于IM和PM组,表明CYP2C19*2和CYP2C19*3的存在与CR的发生正相关。治疗后1、3、6个月三组NIHSS评分差异均有统计学意义,由高到低依次为PM组、IM组和EM组,两两比较差异均有统计学意义(P<0.05)。治疗后1、3、6个月三组ADL评分差异均有统计学意义,由高到低依次为EM组、IM组和PM组,两两比较差异均有统计学意义(P<0.05),充分证明了CYP2C19基因多态性对脑梗死患者氯吡格雷临床疗效的意义,氯吡格雷在强代谢型即EM组患者上,氯吡格雷活性代谢物水平较高,抗血小板作用发挥较好,患者预后亦较好,而以CYP2C19*2和CYP2C19*3为主的IM和PM患者,会存在CR现象,从而影响神经功能的恢复。出院后1年内EM组心脑血管不良事件的发生率明显低于IM组和PM组,差异均有统计学意义(P<0.05)。有文献报道,CR的发生除与CYP2C19基因多态性有关外,还与P2Y12基因多态性和胰岛素抵抗等因素相关[14]。这提示在临床中要关注多影响氯吡格雷疗效的因素,合理指导用药。然而,本研究仍存在以下不足: (1) 血小板聚集、活化过程极其复杂,参与因素众多,单使用IPA很难做出全面、正确的判断,因此亦具有一定的局限性;(2) 与血小板聚集率相比,血浆氯吡格雷或其活性代谢产物的浓度更能直接反应氯吡格雷抵抗,而且不受转运体和受体基因多态性的影响,本研究因实验材料、技术等原因未对此进行探讨;(3) 因本研究样本数量有限,在比较各种心脑血管发生率之上存在较大误差,因此在以后研究中可增多样本量来统计各种心脑血管病发生情况。
综上所述,本次研究通过基因分型,从基因水平证实了CYP2C19基因多态性影响氯吡格雷在治疗脑梗死患者时的疗效,对临床中氯吡格雷的应用有重要的指导意义,提示医师在用药时应注重实施个体化方案,根据患者的基因型合理选择药物。基因多态性对氯吡格雷这种抗血小板聚集药物的疗效具有重要影响,因此也可以采用与本文类似的方法检测研究基因多态性对其他抗血小板聚集药物如阿司匹林疗效的影响。
【参考文献】
[1] 谢婧,胡欣,杨莉萍.CYP2C19*17多态性对氯吡格雷临床疗效影响的系统评价[J].中国循证医学杂志,2014(3): 271-276.
[2] BATES E R, LAU W C, ANGIOLOLLO D J. Clopidogrel-drug interactions [J]. J Am Coll Cardiol, 2011,57(11): 1251-1263.
[3] 中华医学会神经病学分会脑血管病学组急性缺血性脑卒中诊治指南撰写组.中国急性缺血性脑卒中诊治指南2010[J].中国全科医学,2011,14(12B): 4013-4017.
[4] 祝锦,刘丽宏.氯吡格雷药物基因组学研究进展[J].中国新药杂志,2013(15): 1774-1778.
[5] 王雷,袁良津,唐向阳.CYP2C19基因多态性与急性脑梗死患者氯吡格雷疗效的相关性研究[J].临床神经病学杂志,2015(2): 99-102.
[6] 孙硕,孙凌,周颖玲,等.CYP2C19*2基因多态性与经皮冠状动脉介入治疗后氯吡格雷抗血小板临床疗效的相关性[J].岭南心血管病杂志,2014(3): 275- 289.
[7] MEGAJ L, CLOSE S L, WIVIOTT S D, et al. Genetic variants in ABCB1 and CYP2C19 and cardiovascular outcomes after treatment with clopidogrel and prasugrel in the TRITON-TIMI 38 trial: a pharmacogenetic analysis[J]. Lancet, 2010,37(6): 1312-1319.
[8] 陆晶晶,黄建浩,尹琦,等.烟碱型乙酰胆碱受体基因多态性与NSCLC的相关性研究[J].同济大学学报(医学版),2016,38(3): 36-39.
[9] 丛培丽,方舟,荆洪英,等.CYP2C19*1、*17基因多态性对氯吡格雷临床疗效、不良反应影响的系统评价[J].黑龙江医药科学,2014(2): 47-49.
[10] 喻良,黄雨兰,黄斌,等.CYP2C19基因多态性对长期服用氯吡格雷脑梗死患者卒中复发的影响[J].中风与神经疾病杂志,2015(1): 41-44.
[11] 江秀龙,张旭,陈兴泳,等.CYP2C19基因多态性与急性脑梗死患者氯吡格雷抵抗的关系[J].临床神经病学杂志,2015(4): 255-258.
[12] 金欣,陈水平,左向华,等.荧光PCR检测CYP2C19基因分型与氯吡格雷临床疗效的相关性研究[J].中国实验诊断学,2014,18(12): 1948-1950.
[13] 张海涛,苟文,秦华迪,等.CYP2C19基因多态性对氯吡格雷抵抗患者预后的影响[J].检验医学与临床,2014,11(13): 1761-1766.
[14] 石少亭,李亚军,张蓓,等.汉族脑梗死患者中氯吡格雷抵抗的相关因素研究[J].山西医科大学学报,2013,44(12): 953-956.
Correlation between CYP2C19 gene polymorphisms and efficacy of clopidogrel in patients with cerebral infarction
【Abstract】Objective To investigate the correlation between CYP2C19 gene polymorphisms and the efficacy of clopidogrel in patients with cerebral infarction. Methods Two hundred patients with cerebral infarction treated in our hospital from January 2012 to January 2015 were included in the study. The DNA was extracted from blood samples and the CYP2C19 gene polymorphisms were detected by PCR-RFLP. According to the genotypes of CYP2C19 gene, patients were divided into extensive metabolic group, intermediate metabolic group and poor metabolic group. The impedance platelet aggregometry was measured, the National Institute of the Health stroke scale (NIHSS), activities of daily living (ADL) were assessed before and 1st, 6th day and 8th week after clopidogrel administration. The incidence of cerebro-cardiovascular events in one year were documented. Results The impedance platelet aggregometry in extensive metabolic group was the highest 1st day and 6th day after treatment, followed by the intermediate, and that was the lowest in the poor group (P<0.05), there was no statistical significance between that in the 6th day and 8 weeks. There were significant differences in NIHSS and ADL scores at the first, third and the sixth month after treatment among three groups (P<0.05), and the improvement in extensive group was the best, followed by intermediate and the poor groups. The incidence of cerebro-cardiovascular events of extensive metabolic group in one year was significantly lower than that of other two groups (P<0.05). Conclusion CYP2C19 gene polymorphisms are associated with the efficacy of clopidogrel in patients with cerebral infarction, which may be related to the activation of metabolic enzymes.
【Key words】cerebral infarction; clopidogrel; CYP2C19; gene polymorphisms
doi:10.16118/j.1008-0392.2017.02.012
收稿日期:2016-08-18
【中图分类号】R 743.33
【文献标志码】A
【文章编号】1008-0392(2017)02-0060-05