·临床研究·
甲状腺局部注射地塞米松治疗Graves病的临床疗效及生活质量评估
姚 蔚, 方铭喜, 翟迎九, 张 菁, 杨燕萍, 方 琦
(上海市浦东新区周浦医院内分泌科,上海 201318)
【摘要】目的 观察甲状腺局部注射地塞米松治疗Graves病临床疗效及生活质量的观察评估。方法 60例常规口服甲硫咪唑的Graves病患者,随机分为A、B两组,A组加用甲状腺局部注射地塞米松,观察6个月间的临床指标以及生活质量变化情况。结果 A组临床症状、血清学指标以及患者生活质量相比对照组在短时间内均有所提高(P<0.05)。结论 甲状腺局部注射地塞米松不仅对Graves病安全有效,而且短时间内改善患者生活质量方面也有一定的帮助。
【关键词】Graves病; 局部甲状腺注射; 临床疗效
Graves病(Graves’ disease, GD)又称弥漫性毒性甲状腺肿,是一种伴甲状腺激素分泌增多的自身免疫性甲状腺疾病。该病的患病率约为0.5%[1],是甲亢中最常见的类型,占所有甲亢的50%~85%左右[2-3]。女性显著高发,男女比为1∶5~6。近年来,该病有逐渐升高的趋势。该疾患不仅是躯体性疾患,还可伴发神经精神方面的异常,如记忆下降、情绪不稳、易怒、抑郁、焦虑和轻度躁狂等,对患者的生活质量造成一定的影响。健康调查量表(36-item Short Form Health Survey, SF-36)全面概括了生理、心理和社会等方面的健康状况,常用于一般人群和一些慢性病患者的生活质量评价[4],在GD患者生活质量评价方面也具有较高的信效度。采用甲状腺局部注射地塞米松联合口服甲硫咪唑治疗Graves病,取得了较好的疗效,不仅从改善患者的临床症状方面,也能在短时间内能提高患者生活质量,现报道如下。
1 资料与方法
1.1 一般资料
研究对象为上海市浦东新区周浦医院2013年1月至2014年12月收治的上海市浦东新区周康航地区GD患者共60例,其中男23例,女37例。年龄19~ 55岁,平均年龄33.87±9.34岁。随机分为联合治疗组(A组)和单纯药物治疗组(B组),每组各30例。两组患者在年龄、性别、甲状腺质量及甲状腺功能指标FT3、FT4、TSH、TRAb等方面比较均无统计学差异(均P>0.05),具有可比性(表1)。同时对比了患者的文化程度、职业、婚姻状况等,也无显著的统计学差异(均P>0.05)。入选患者均符合Graves病的诊断标准[3],排除患有严重心肺疾患、肝肾功能不全、严重出血倾向、精神异常不能合作、糖尿病或糖耐量异常、糖皮质激素禁忌以及处于妊娠期或哺乳期的妇女。所有患者均签署知情同意书。
表1 两组患者治疗前的临床资料比较
Tab.1 General information of patients in two groups before treatment
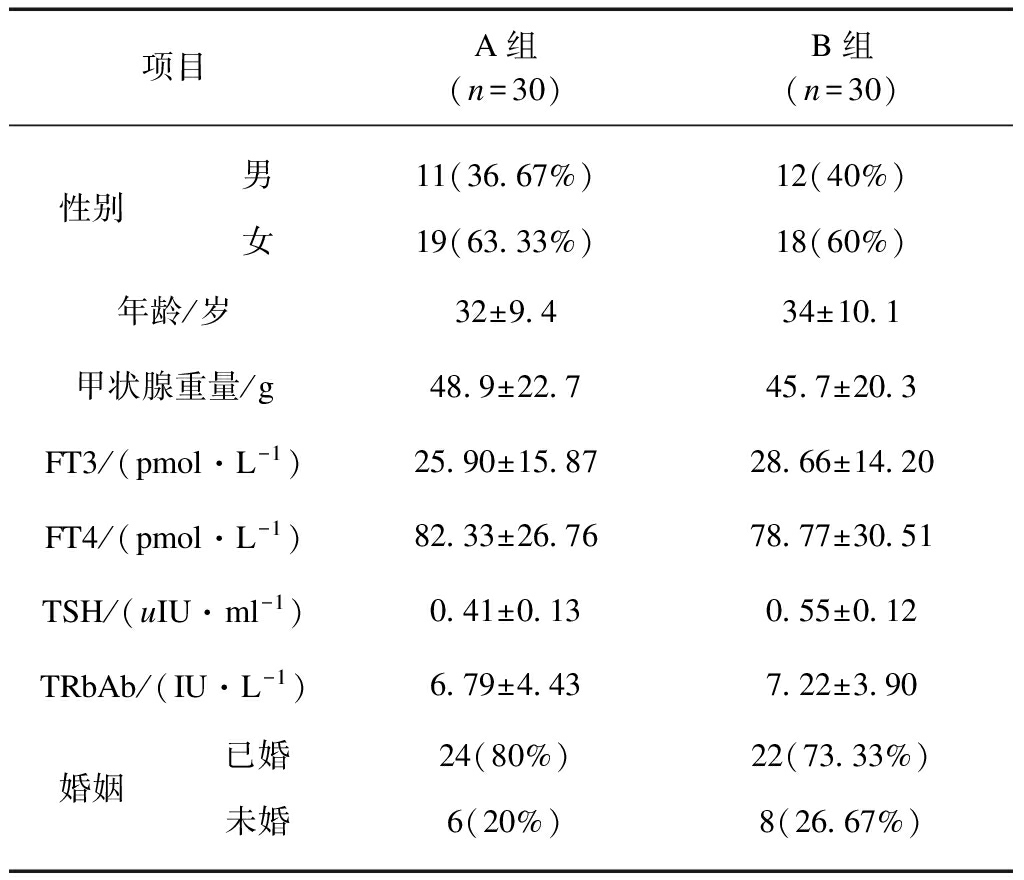
项目A组(n=30)B组(n=30)性别男11(36 67%)12(40%)女19(63 33%)18(60%)年龄/岁32±9 434±10 1甲状腺重量/g48 9±22 745 7±20 3FT3/(pmol·L-1)25 90±15 8728 66±14 20FT4/(pmol·L-1)82 33±26 7678 77±30 51TSH/(uIU·ml-1)0 41±0 130 55±0 12TRbAb/(IU·L-1)6 79±4 437 22±3 90婚姻已婚24(80%)22(73 33%)未婚6(20%)8(26 67%)
(续表1)
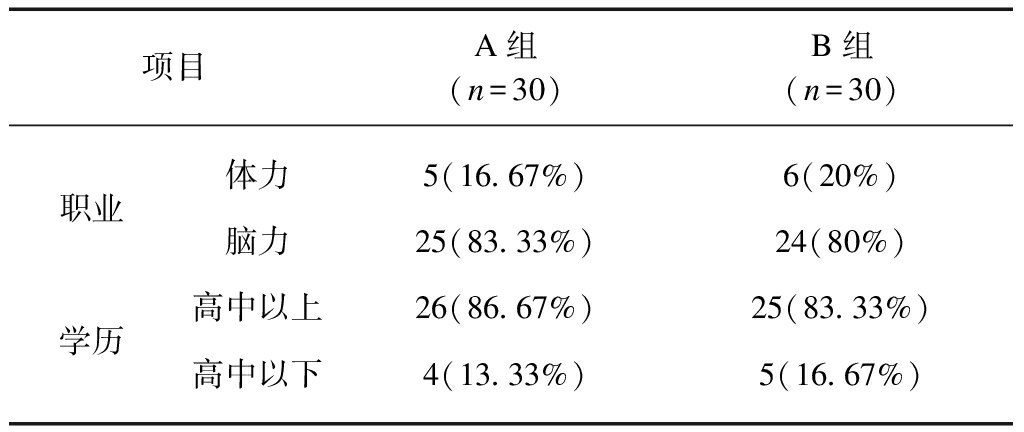
项目A组(n=30)B组(n=30)职业体力5(16 67%)6(20%)脑力25(83 33%)24(80%)学历高中以上26(86 67%)25(83 33%)高中以下4(13 33%)5(16 67%)
注: 两组比较各项指标,P>0.05
1.2 治疗方法
两组患者均忌含碘饮食,给予口服甲硫咪唑10mg,每日2~3次,心得安10mg,每日2~3次。A组患者同时予甲状腺局部注射地塞米松,双侧各注射5mg,每周一次,五周为一疗程,每疗程最后一次改为注射曲安奈德10mg,间隔一个月行第二疗程,共2~3个疗程。注射方法为患者取仰卧位,枕垫于颈后,头轻度后仰,充分显露甲状腺,常规消毒,用1ml注射器抽吸地塞米松,在B超引导下或在直视下触及甲状腺最宽大处,于气管旁垂直或斜行进针,达甲状腺中央部位回抽无血后,多方向缓慢注入药物,为防止疼痛,可加少许利多卡因,拔针后局部压迫5~15min,观察有无出血等副反应。
1.3 观察指标
(1) 临床症状、体征: 如心慌、出汗、食欲亢进、消瘦及眼睛胀感等;(2) 血清学检查: FT3、FT4、TSH、TRAb;(3) 超声检查: 甲状腺体积、回声、密度、血流状况;(4) 显效例数;(5) 副反应观察;(6) 甲 状腺重量计算公式: 按标准椭圆公式每叶体积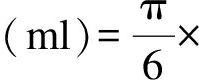 长径(cm)×宽径(cm)×厚径(cm)(π/6≈0.52),将甲状腺左、右叶及峡部相加为总体积。(7) 生活质量调查: 在治疗的2个月、4个月、6个月行门诊或电话随访,用SF-36量表从功能状态、健康满意程度和健康总评价三大方面来进行生活质量评估,包括8个维度: ① 生理功能(physicalfunction, RF);② 生理职能(rolephysical, RP);③ 躯体疼痛(bodilypain, BP);④ 一般健康状况(generalhealth, GH);⑤ 精力(vitality, VT);⑥ 社 会功能(socialfunction, SF);⑦ 情感职能(roleemotion, RE);⑧ 精神健康(mentalhealth, MH)。将生理功能、生理职能、躯体疼痛、一般健康状况4个维度得分总和作为躯体健康总评(physicalcomponentsummary, PCS),反映生理健康;将精力、社会功能、情感职能以及精神健康4个维度得分总和作为精神健康总评(mentalcom-ponent summary, MCS),反映精神健康。每个维度的得分范围为0~100分,得分越高代表该维度的生活质量越好。
长径(cm)×宽径(cm)×厚径(cm)(π/6≈0.52),将甲状腺左、右叶及峡部相加为总体积。(7) 生活质量调查: 在治疗的2个月、4个月、6个月行门诊或电话随访,用SF-36量表从功能状态、健康满意程度和健康总评价三大方面来进行生活质量评估,包括8个维度: ① 生理功能(physicalfunction, RF);② 生理职能(rolephysical, RP);③ 躯体疼痛(bodilypain, BP);④ 一般健康状况(generalhealth, GH);⑤ 精力(vitality, VT);⑥ 社 会功能(socialfunction, SF);⑦ 情感职能(roleemotion, RE);⑧ 精神健康(mentalhealth, MH)。将生理功能、生理职能、躯体疼痛、一般健康状况4个维度得分总和作为躯体健康总评(physicalcomponentsummary, PCS),反映生理健康;将精力、社会功能、情感职能以及精神健康4个维度得分总和作为精神健康总评(mentalcom-ponent summary, MCS),反映精神健康。每个维度的得分范围为0~100分,得分越高代表该维度的生活质量越好。
1.4 疗效评价
(1) 临床治愈: 临床症状消失,甲状腺质量减少达50%或以上,FT3、FT4、TSH、TRAb恢复正常;(2) 显效: 临床症状消失,甲状腺质量减少达25%或以上,FT3、FT4、TSH、TRAb基本恢复或接近正常;(3) 无效: 临床症状好转、甲状腺质量减少达25%以下,FT3、FT4、TSH、TRAb仍异常。
1.5 量表测评方法
所有研究对象均在同一医师指导下进行测评,测评在单独、安静的环境下进行,评定方式以自评为主,对阅读及作答有困难者,调查者进行协助。每个维度包含的条目数不同,不利于比较,故采用公式进行分数转换后纳入统计学处理,各维度转换公式为: 转换分数=[(实际评分-最低可能评分)/一般平均可能评分]×100。8个维度转换分数的平均值为总评分。
1.6 统计分析
采用SPSS 15.0统计软件,计量资料以 ±s表示,两组以上的均数比较采用方差分析,组间比较采用t检验。P<0.05为差异有显著性。
±s表示,两组以上的均数比较采用方差分析,组间比较采用t检验。P<0.05为差异有显著性。
2 结 果
2.1 两组患者临床治愈情况比较(表2)
表2 两组患者临床治愈情况比较
Tab.2 Comparison of cure rate between two groups [%(n)]
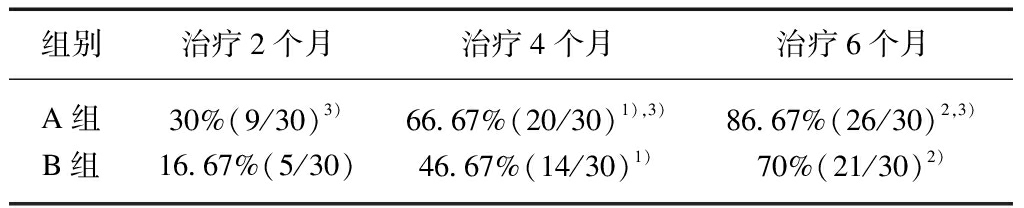
组别治疗2个月治疗4个月治疗6个月A组30%(9/30)3)66 67%(20/30)1),3)86 67%(26/30)2,3)B组16 67%(5/30)46 67%(14/30)1)70%(21/30)2)
注: 本组比较,与治疗2个月比较,1) P<0.05;与治疗4个月比较,2) P<0.05;两组比较,3) P<0.05
2.2 两组患者治疗后显效例数比较(表3)
表3 两组患者治疗后显效例数比较
Tab.3 Comparison of response rate between two groups [%(n)]

组别治疗2个月治疗4个月治疗6个月A组36 67%(11/30)3)76 67%(23/30)1),3)96 67%(29/30)2),3)B组26 67%(8/30)56 67%(17/30)1)76 67%(23/30)2)
注: 本组比较,与治疗2个月比较,1) P<0.05;与治疗4个月比较,2) P<0.05;两组比较,3) P<0.05
2.3 两组患者治疗后甲状腺重量减少情况比较(表4)
表4 两组患者治疗后甲状腺重量减少情况比较
Tab.4 Comparison of thyroid weight reduction after treatment between two groups (g)
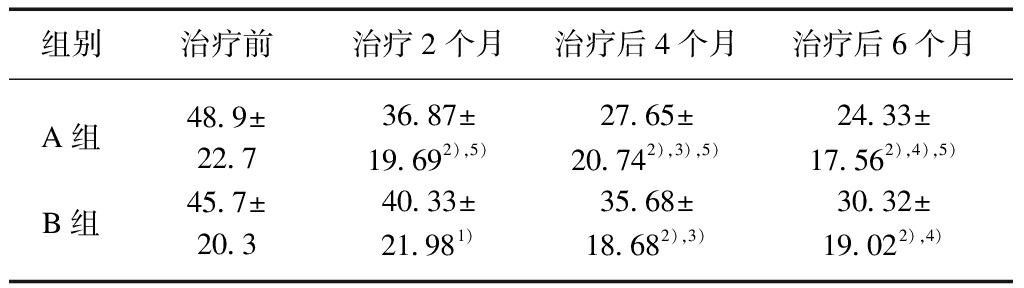
组别治疗前治疗2个月治疗后4个月治疗后6个月A组48 9±22 736 87±19 692),5)27 65±20 742),3),5)24 33±17 562),4),5)B组45 7±20 340 33±21 981)35 68±18 682),3)30 32±19 022),4)
注: 本组比较,与治疗前比较,1) P<0.05;2) P<0.01;与治疗2个月比较;3) P<0.01;与治疗4个月比较,4) P<0.01;两组比较,5) P<0.05
2.4 两组患者血清学指标治疗前后比较(表5)
表5 两组患者血清学指标治疗前后比较
Tab.5 Comparison of serological indexes before and after treatment in two groups

组别血清学指标治疗前治疗2个月治疗4个月治疗6个月A组FT3/(pmol·L-1)25 90±15 8718 12±15 341),5)13 20±11 903),5)6 42±5 104),5)FT4/(pmol·L-1)82 33±26 7645 14±20 981),6)30 27±18 763),5)17 17±12 744),6)TSH/(μIU·ml-1)0 01±0 131 07±0 591),6)1 84±0 993),5)2 74±0 394),5)TRAb/(IU·L-1)7 19±4 434 99±1 761),6)2 01±1 253),5)1 70±0 984),6)B组FT3/(pmol·L-1)28 66±14 2020 67±19 431)15 66±7 983)10 87±6 734)FT4/(pmol·L-1)78 77±30 5156 28±28 672)34 12±20 773)23 54±15 144)TSH/(μIU·ml-1)0 01±0 120 66±0 241)1 37±0 313)4 01±0 184)TRAb/(IU·L-1)6 92±3 906 89±4 811)6 14±3 083)2 61±2 004)
注: 本组比较,与治疗前比较,1) P<0.05;2) P<0.01;与治疗2个月比较,3) P<0.01;与治疗4个月比较,4) P<0.01;两组比较,5) P<0.05;6)P<0.01
2.5 副反应及并发症
两组患者均全部完成治疗,且无严重并发症发生,A组仅3例患者在初次注射后出现一过性面红,1例患者阵发性心悸,休息1~2h后症状消失,无明显神经损伤以及注射后大出血。
2.6 生活质量调查
两组SF-36量表各维度评分比较结果示,GD患者除躯体疼以及生理功能前后比较变化无显著性差异,其他维度评分中从治疗2个月起评分A组较B组明显改善,除RP、GH、PCS在治疗6个月时两组差别无统计学意义,另外维度(VT、SF、RE、MH、MCS、TS)在治疗6个月时仍有显著差异,见表6。
表6 两组SF-36量表各维度评分比较
Tab.6 Comparison of SF-36 scores between two groups  ±s)
±s)
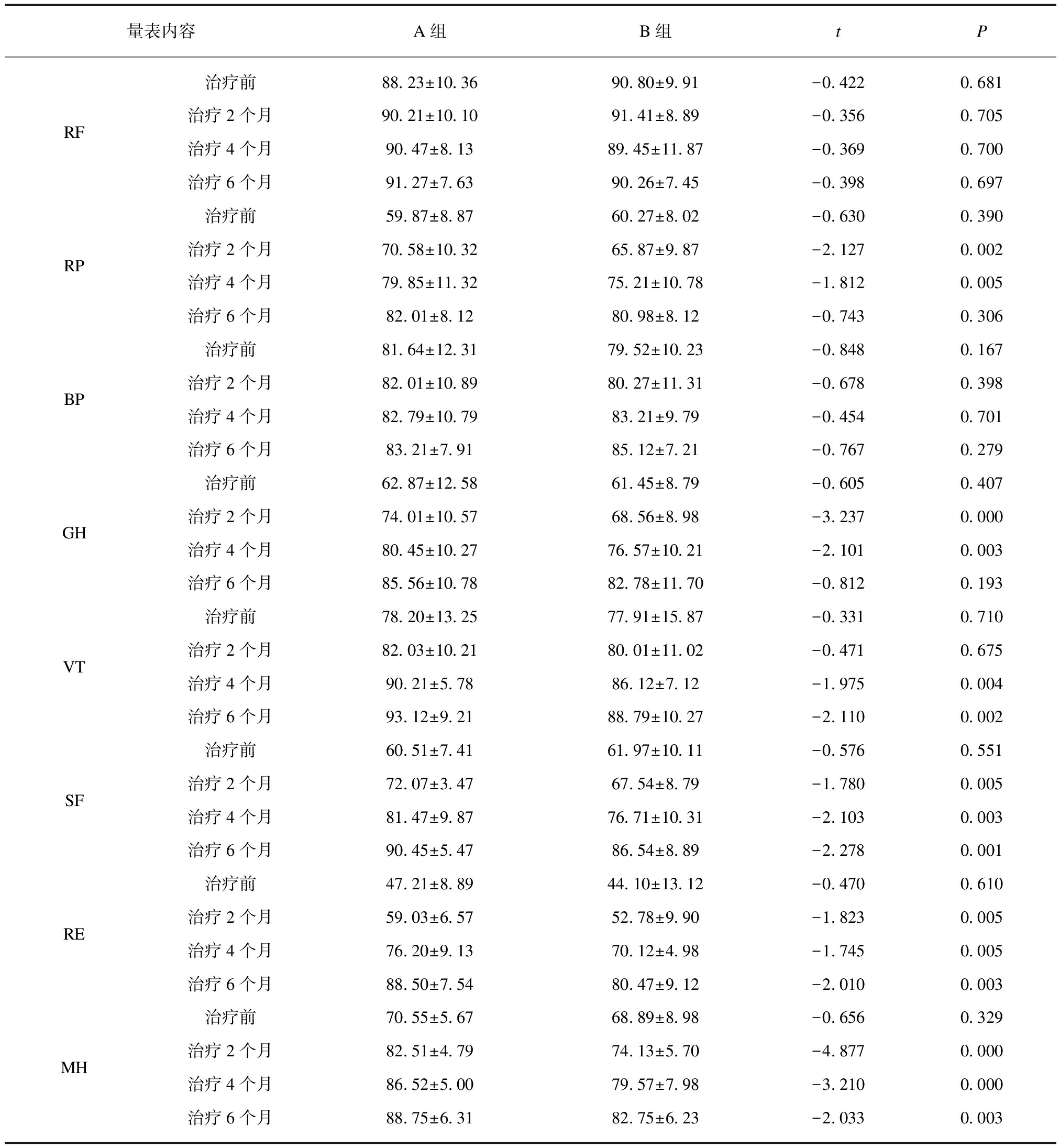
量表内容A组B组tPRF治疗前88 23±10 3690 80±9 91-0 4220 681治疗2个月90 21±10 1091 41±8 89-0 3560 705治疗4个月90 47±8 1389 45±11 87-0 3690 700治疗6个月91 27±7 6390 26±7 45-0 3980 697RP治疗前59 87±8 8760 27±8 02-0 6300 390治疗2个月70 58±10 3265 87±9 87-2 1270 002治疗4个月79 85±11 3275 21±10 78-1 8120 005治疗6个月82 01±8 1280 98±8 12-0 7430 306BP治疗前81 64±12 3179 52±10 23-0 8480 167治疗2个月82 01±10 8980 27±11 31-0 6780 398治疗4个月82 79±10 7983 21±9 79-0 4540 701治疗6个月83 21±7 9185 12±7 21-0 7670 279GH治疗前62 87±12 5861 45±8 79-0 6050 407治疗2个月74 01±10 5768 56±8 98-3 2370 000治疗4个月80 45±10 2776 57±10 21-2 1010 003治疗6个月85 56±10 7882 78±11 70-0 8120 193VT治疗前78 20±13 2577 91±15 87-0 3310 710治疗2个月82 03±10 2180 01±11 02-0 4710 675治疗4个月90 21±5 7886 12±7 12-1 9750 004治疗6个月93 12±9 2188 79±10 27-2 1100 002SF治疗前60 51±7 4161 97±10 11-0 5760 551治疗2个月72 07±3 4767 54±8 79-1 7800 005治疗4个月81 47±9 8776 71±10 31-2 1030 003治疗6个月90 45±5 4786 54±8 89-2 2780 001RE治疗前47 21±8 8944 10±13 12-0 4700 610治疗2个月59 03±6 5752 78±9 90-1 8230 005治疗4个月76 20±9 1370 12±4 98-1 7450 005治疗6个月88 50±7 5480 47±9 12-2 0100 003MH治疗前70 55±5 6768 89±8 98-0 6560 329治疗2个月82 51±4 7974 13±5 70-4 8770 000治疗4个月86 52±5 0079 57±7 98-3 2100 000治疗6个月88 75±6 3182 75±6 23-2 0330 003
(续表6)
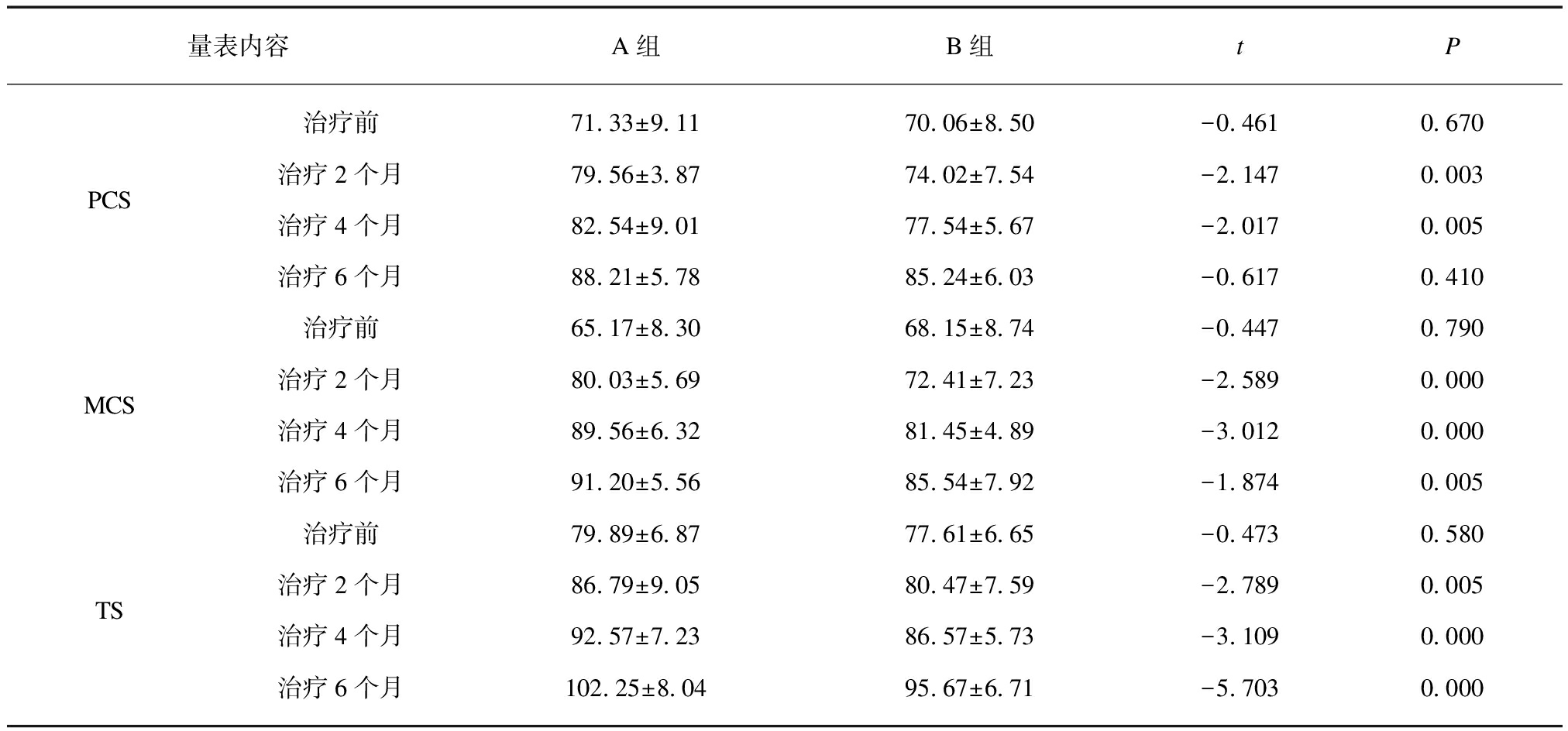
量表内容A组B组tPPCS治疗前71 33±9 1170 06±8 50-0 4610 670治疗2个月79 56±3 8774 02±7 54-2 1470 003治疗4个月82 54±9 0177 54±5 67-2 0170 005治疗6个月88 21±5 7885 24±6 03-0 6170 410MCS治疗前65 17±8 3068 15±8 74-0 4470 790治疗2个月80 03±5 6972 41±7 23-2 5890 000治疗4个月89 56±6 3281 45±4 89-3 0120 000治疗6个月91 20±5 5685 54±7 92-1 8740 005TS治疗前79 89±6 8777 61±6 65-0 4730 580治疗2个月86 79±9 0580 47±7 59-2 7890 005治疗4个月92 57±7 2386 57±5 73-3 1090 000治疗6个月102 25±8 0495 67±6 71-5 7030 000
3 讨 论
GD为器官自身免疫性疾病,患者体内可产生许多自身抗体,如甲状腺球蛋白抗体、甲状腺微粒体抗体、甲状腺过氧化物酶抗体等[5],其病理特征为甲状腺滤泡上皮细胞增生,滤泡腔内的胶质减少或消失,滤泡间可见不同程度的淋巴细胞浸润,且以T淋巴细胞为主。目前普遍认为GD的发病机制主要是由于抑制性T细胞(Ts细胞)功能缺陷、抑制性T细胞和辅助性T细胞平衡紊乱、免疫调节失衡,导致GD的发生[6]。
GD的治疗主要包括抗甲状腺药物、放射性碘及手术[7-8]。由于各有利弊,不同国家的不同医生往往选择不同的治疗方法。我国和欧洲国家以选用药物为主,但常用的抗甲状腺药物疗程长,复发率高,对甲状腺的消肿作用差。近10年来,甲状腺局部免疫调节治疗得到临床医生的青睐,通过对表浅的甲状腺注射药物,利用药物在局部的高浓度状态,经过直接接触和缓慢浸润作用,达到稳定甲状腺细胞膜结构,抑制炎症及减轻免疫反应的效果;其在提高有效药物浓度的同时,还具有用量少,操作简单,消肿率高,维持时间长,无明显不良反应等特点。
甲状腺局部免疫调节治疗常用的药物主要有糖皮质激素、免疫抑制剂、生长抑素类似物及无水乙醇等,而地塞米松是使用较多且被推荐为首选的药物。地塞米松是人工合成的长效糖皮质激素类药物,是一种免疫抑制药,其作用包括抑制周围组织脱碘酶,使T3产生减少;抑制淋巴细胞活性,干扰淋巴组织在抗原作用下的分裂及增殖,阻断了致敏T淋巴细胞释放各种细胞因子,使免疫活性细胞因子减少,抑制了淋巴滤泡的形成,减少了淋巴滤泡对甲状腺组织的破坏,并使肿大的甲状腺缩小变软;降低促甲状腺激素受体抗体(TRAB)的水平,减少肿大的甲状腺体积,降低甲亢复发率[9];体外研究表明[10],地塞米松可以显著改善GD患者外周血调节性T细胞功能,重建辅助性T细胞1及辅助性T细胞2的平衡等。研究显示,地塞米松局部免疫调节治疗在肿块缩小、质地改善、抗体恢复和淋巴细胞浸润减轻方面有着显著的效果[11]。
研究观察联合地塞米松局部注射治疗的GD患者,其临床症状缓解时间、血清学指标恢复时间、甲状腺重量等,在治疗的早期就较单纯口服抗甲状腺药物的患者明显缩短或减轻(P<0.05),与相关报道[12]显示了一致的结果。特别是血清学指标的持续改善,尤其是TRAb的好转,纠正了机体的免疫紊乱,在甲亢的预后、复发方面有着更强的保护意义。
既往对于疾病的评价多为客观评价,在目前的医疗模式下,越来越多的学者关注到疾病个体的主管评价,生活质量无疑是评价健康的重要发展方向。Graves病作为一种慢性疾患,其在确诊前就存在甲状腺毒性全身症状,如怕热、多汗、多食易饥等,也存在焦虑、烦躁、失眠以及认知功能减退等神经精神症状,甚至一些Graves病治愈后,一些神经精神症状仍持续存在[13]。有学者发现Graves病患者的躯体健康可以基本恢复正常,而精神健康仍可能有不同程度受损[14]。
本课题所选用的生活质量量表为SF-36(Short Form 36 Health Survey Questionnaire)作为一种简明健康调查问卷[15],它全面概括了生理、心理和社会等方面的健康情况,SF-36用于一般人群中的生活质量评价已经相当广泛,同时,对于一些慢性病患者的生活质量评价也有一些应用[16],有研究表明SF-36量表用于甲亢患者生存质量测定具有较好的信度和效度[17]。
选用生活质量量表可以发现,在生理功能以及躯体疼痛这两个维度方面,两组治疗后无明显统计学差异;其他六个维度在起始治疗时即出现统计学差异,这六个维度多反应患者社交等生活质量相关。同时这一结果提示,精神心理因素对疾病症状的产生有一定作用。而Graves病患者的生命质量与抑郁或焦虑状态水平密切相关。
针对GD的核心问题—免疫因素,寻求和开辟新的治愈率高、并发症少的有效治疗途径是临床医生面临的课题。甲状腺局部免疫调节治疗是对传统治疗措施的补充和创新。但是目前该治疗方法应用尚不广泛,缺乏大样本的资料,对该治疗方法的适应证、禁忌证、药物品种和剂量以及注射方法等问题,还需要进一步的研究和完善。同时,通过局部注射地塞米松治疗GD患者,从生活质量方面在治疗早期也起了积极的作用,在临床治疗过程中不仅要改善甲状腺毒性的危害性,也有关注患者心理健康的恢复,全面提高患者生活质量。
【参考文献】
[1] Girgis CM, Champion BL, Wall JR. Current concepts in Graves’ disease[J]. Ther Adv Endocrinol Metab, 2011,2(3): 135-144.
[2] Franklyn JA, Boelaert K. Thyrotoxicosis[J]. Lancet, 2012,379(9821): 1155-1166.
[3] 孟召伟,谭建.解读美国甲状腺协会和临床内分泌医师协会2011年甲亢诊疗指南[J].国际放射医学核医学杂志,2011,35(4): 193-201.
[4] Kristian HW. The chronic autoimmune thyroiditis quality of life selenium trial(CATALYST): study protocol for a randomized controlled trial[J]. Trials, 2014,15(1): 115.
[5] 徐伟良,聂芙蓉,曹绮雯,等.血清甲状腺球蛋白抗体、甲状腺微粒体抗体、甲状腺过氧化物酶抗体对自身免疫性甲状腺疾病的诊断价值[J].实用临床医药杂志,2014,18(5): 10-12.
[6] 王曙,郭华.Graves病的发病机制[J].内科理论与实践,2010,5(2): 153-159.
[7] 王舰,蔡海东,吕明丽,等.131I固定计量法及计算计量法治疗甲亢的疗效评价[J].同济大学学报: 医学版,2012,33(1): 83-93.
[8] Muldoon BT, Mai VQ, Burch HB. Management of graves’ disease anoverview and comparison of clinical practice guidelines with actual practice trends[J]. Endocrinol Metab Clin N Am, 2014,43(2): 495-516.
[9] 何珂,胡蕴,毛晓明.甲状腺局部注射地塞米松治疗Graves病中调节性T细胞变化的研究[J].免疫学杂志,2013,29(9): 787-791.
[10] Hu Y, Tian W, Zhang LL, et al. function of regulatory T-cells improved by dexamethasone in Graves’ disease[J]. Eur J Endocrinol, 2012,166(4): 641-646.
[11] 苏振丽,马丽芬.甲状腺内注射地塞米松治疗桥本甲状腺炎[J].吉林医学,2013(8): 1476-1477.
[12] 张月成.丙基硫氧嘧啶联合地塞米松治疗甲状腺功能亢进疗效观察[J].医药论坛杂志,2013,34(4): 15-17.
[13] 曾菁,严悦溶.Graves病患者抑郁状态与甲状腺激素水平关系研究[J].四川大学学报: 医学版,2014,45(3): 460-463.
[14] 胡斌,成莉霞.131I治疗Graves病患者1年后社会心理状况及生活质量研究[J].中国现代医学杂志,2015,25(13): 61-65.
[15] 王坤.健康状况调查简表(SF-36)[J].中华神经外科杂志,2012(6): 571-571.
[16] 汪海峰.老年恶性肿瘤患者MNA-SF营养评价和SF-36生活质量评价[J].同济大学学报: 医学版,2009,30(3): 129-131.
[17] 赵萍.Graves病患者生命质量与影响因素探讨[D].中南大学,2011,doi: 10.7666/d.y1917765.
Efficacy of local injection of dexamethasone for treatment of Graves’ disease
YAO Wei, FANG Ming-xi, ZHAI Ying-jiu, ZHANG Jing, YANG Yan-ping, FANG Qi
(Dept. of Endocrinology, Pudong New Area Zhoupu Hospital, Shanghai 201318, China)
【Abstract】Objective To evaluate the efficacy of local injection of dexamethasone for treatment of Graves’ disease. Methods Sixty patients with Graves’ disease were randomly divided into group A and group B with 30 cases in each group. Patients in both groups received conventional methimazole treatment; those in group A were given additional local injection of dexamethasone. The clinical indexes and quality of life quality in both groups were evaluated after 6 months of treatment. Results The clinical symptoms, serological indexes and the quality of life in group A were improved more markedly than those in group B(P<0.05). Conclusion Local injection of dexamethasone is safe and effective, and can improve the quality of life for patients with Graves’ disease.
【Key words】Graves’ disease; local injection of thyroid; clinical efficacy
doi:10.16118/j.1008-0392.2016.06.016
收稿日期:2016-08-27
作者简介:姚 蔚(1979—),女,主治医师,硕士研究生.E-mail: 29619195@qq.com
通信作者:方 琦.E-mail: fq118478@163.com
【中图分类号】R 581
【文献标志码】A
【文章编号】1008-0392(2016)06-0082-06







