·基础研究·
【摘要】目的 探讨微等离子体射频技术治疗凹陷性瘢痕及面部年轻化的可能作用机制,为临床应用提供理论依据。方法 使用相同治疗参数的微等离子体射频技术分别照射受试者的左背部皮肤,在术后即刻和术后1、3、5、7、14、28、90、180d,于照射区域及非照射区域分别取皮肤活检,对活检的皮肤标本分别作H-E染色,Masson三色染色,Ⅰ型及Ⅲ型胶原、VEGF、热休克蛋白70(heat shock proteins 70, HSP70)免疫组化染色。结果 微等离子体作用于皮肤后产生不连续分布的热气化区。照射后5d胶原纤维开始增多,并持续至照射后180d。照射后即刻,VEGF就开始高表达,并维持28d左右。照射3d后,HSP70就开始增加,主要表达在表皮和真皮浅层,7d到达高峰,并维持90d。结论 微等离子体射频作用于人体皮肤组织可以刺激人皮肤真胶原纤维和弹力纤维增生,并且持续时间可达半年。
【关键词】微等离子体; 胶原蛋白; 血管内皮生长因子; 热休克蛋白70
微等离子体技术是一种微创式剥脱性点阵模式新技术,临床上主要应用于痤疮后凹陷性瘢痕和光老化性细纹,疗效较为确切。微等离子体技术是由多点单极射频在距离皮肤很微小的距离内激发空气中的氮气分子,并形成等离子放电,产生的电火花引起皮肤轻微的剥脱,其能量以点阵形式发射,形成“微剥脱区”,在皮肤上形成表皮至真皮上层可以控制的小孔;当治疗头与皮肤接触时,单极射频的能量使真皮层受到高温刺激,形成阵列样排列的“热损伤区”。目前,国内外尚无微等离子体技术作用于人活体的组织病理研究,且对治疗后真皮胶原含量的变化也没有定量分析。故本研究进行相关的测定,为临床治疗提供理论依据和指导。
1.1 一般资料
健康蒙古利亚人种志愿者3名,年龄24~55岁。Fitzpatrick皮肤类型Ⅲ~Ⅳ型。排除孕妇、哺乳期、有增生性瘢痕及瘢痕疙瘩史、光敏性疾病、6个月内服用过维A酸类药物或接受过激光治疗者、试验期有系统或局部感染者。
1.2 方法
1.2.1 微等离子体治疗及取材 采用闪耀TM离子束射频治疗仪(以色列飞顿激光公司),选择左背部皮肤作为治疗区域,相同光照条件下拍照。术前清水清洁治疗区域皮肤,复方利多卡因乳膏(北京紫光制药有限公司)封包1h麻醉,酒精清洁治疗区域皮肤。治疗模式采用滚轮头,治疗4遍,能量80W,释放持续时间30s。术后创面避水3d。在治疗后即刻,术后1、3、5、7、14、28、90、180d分别在照射部位和非照射部位取活检。
1.2.2 标本处理 取得的活检标本立刻放入0.1mol/L 磷酸酸盐缓冲的10%甲醛溶液,固定24h。固定后的标本脱水,石蜡包埋切片。切片后分别进行H-E染色,Masson三色染色,Ⅰ型及Ⅲ型胶原、VEGF、热休克蛋白70免疫组化染色。
1.3 统计学处理
用CCD数码相机对每张染色切片进行低倍 2.5×10×4.0和高倍10×10×4.0拍照。取得的照片用图像分析软件Image-Pro Plus 6.0(Media Cybernetics公司)进行半定量分析。每张高倍镜照片随机选取5个视野,得到的数值以![]() 表示,使用SPSS 19.0进行各组配对t检验分析。P<0.05为差异有统计学意义。
表示,使用SPSS 19.0进行各组配对t检验分析。P<0.05为差异有统计学意义。
2.1 微等离子体照射后胶原纤维变化
H-E染色结果显示,热气化区宽而浅,并环绕以相应的热凝固区。照射3d后,表皮完全复上皮化。照射7d后,开始痂皮脱落。通过H-E常规染色、Masson三色胶原特殊染色可以发现,皮肤在未照射微等离子体时,真皮浅层胶原纤维稀疏,纤细,真皮深层胶原纤维分布紊乱,不规则。照射后1、3、5、7、14d后,真皮胶原未见明显变化。照射28d后,浅层胶原纤维变粗,真皮深层胶原纤维排列整齐,粗大。胶原在真皮全层均有增强,表现为新生的胶原重排,胶原纤维的走行方向与表皮大体平行,真皮浅层的胶原沉积增多。免疫组织化学染色(棕黄色为染色阳性)的结果与H-E常规染色结果大致符合。Ⅰ、Ⅲ型胶原免疫组化染色结果显示,照射5d后,Ⅲ型胶原就染色开始增强,尤其以真皮浅层增强明显。Ⅰ型胶原免疫组化染色结果显示,照射28d后,Ⅰ型胶原染色明显增强,真皮浅层及深层染色均增强,并于90d到达峰值,与未照射组相比差异显著(P<0.05),见图1。
2.2 微等离子体照射后VEGF的动态变化
免疫组化显示,对照组VEGF弱表达。在照射4h后即可观察到皮肤表皮和真皮浅层VEGF表达增加。照射3、5、7、14、28d后,VEGF表达继续增加。此后VEGF表达下降。照射90d后,VEGF表达下降到与对照组类似,此后VEGF表达基本无太大的变化,见表1。
2.3 微等离子体照射皮肤HSP70的动态变化
免疫组化显示,对照组HSP70呈弱阳性。微等离子体照射皮肤3d后,HSP70的表达开始上调。此后HSP70进一步增强。照射7d后达到高峰,此后HSP70表达下降,照射90d后才降到基础值,见表1。
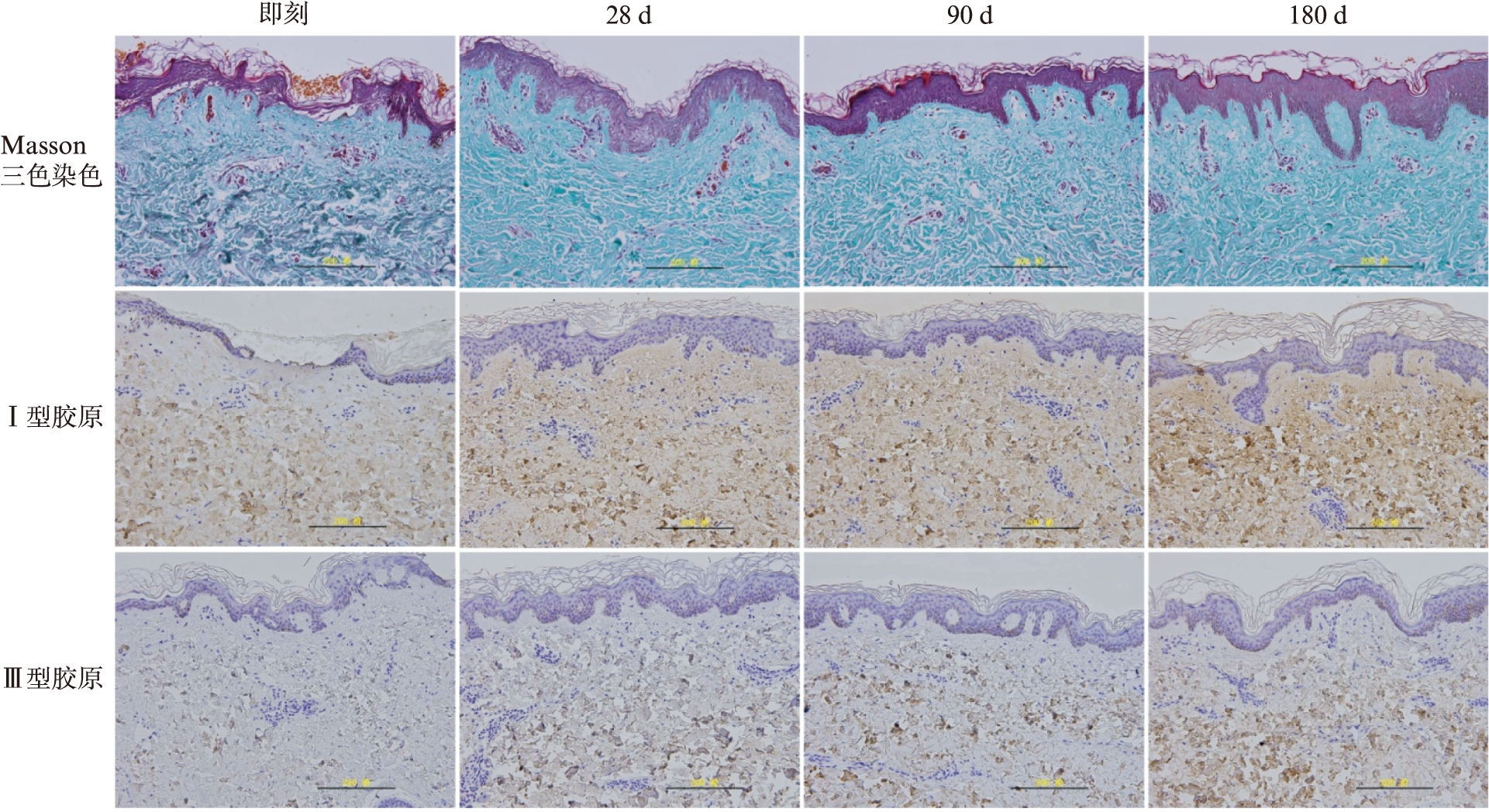
图1 微等离子体照射后Masson三色胶原特殊染色及Ⅰ、Ⅲ型胶原免疫组化染色
Fig.1 Masson staining and typeⅠand Ⅲ collagen immunohistochemical staining after irradiation of microplasma radiofrequency
表1 微等离子体照射后Ⅰ、Ⅲ型胶原、VEGF、HSP70的动态变化
Tab.1 Dynamic changes of typeⅠand Ⅲ collagen, and expression of VEGF, HSP70 after irradiation of microplasma radiofrequency![]()
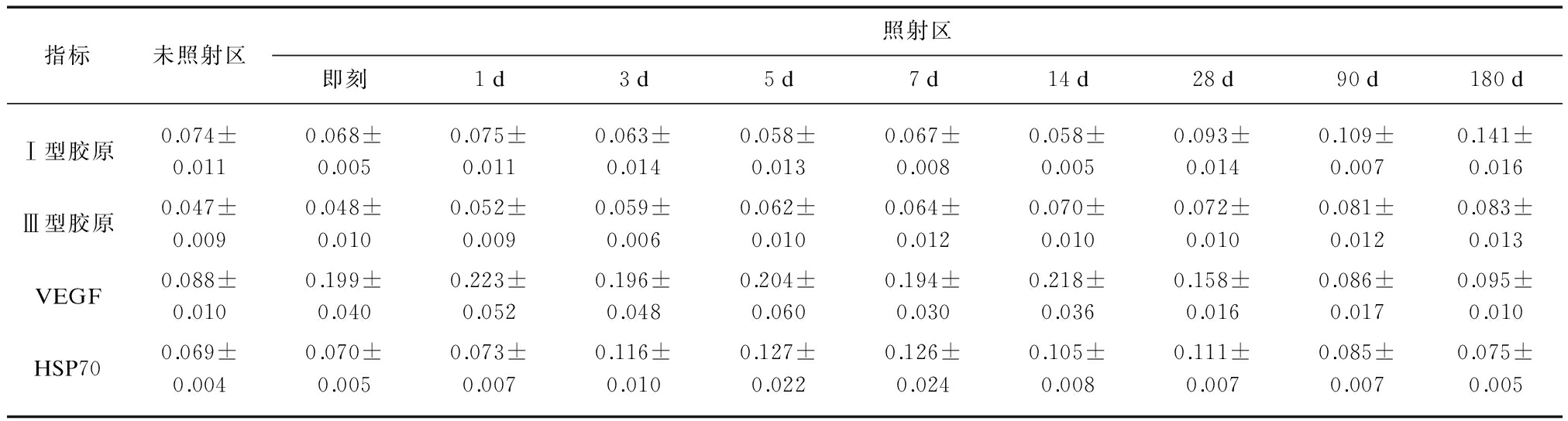
指标未照射区照射区即刻1d3d5d7d14d28d90d180dⅠ型胶原0.074±0.0110.068±0.0050.075±0.0110.063±0.0140.058±0.0130.067±0.0080.058±0.0050.093±0.0140.109±0.0070.141±0.016Ⅲ型胶原0.047±0.0090.048±0.0100.052±0.0090.059±0.0060.062±0.0100.064±0.0120.070±0.0100.072±0.0100.081±0.0120.083±0.013VEGF0.088±0.0100.199±0.0400.223±0.0520.196±0.0480.204±0.0600.194±0.0300.218±0.0360.158±0.0160.086±0.0170.095±0.010HSP700.069±0.0040.070±0.0050.073±0.0070.116±0.0100.127±0.0220.126±0.0240.105±0.0080.111±0.0070.085±0.0070.075±0.005
2005年,等离子体治疗仪应用于皮肤外科,其通过氮气等离子体高温烧灼而非光或射频能量传递进行治疗。微等离子体技术是新近才开发出来的一种微创烧灼性技术,它利用多点单极射频,将设备的手具与皮肤之间的空气中的氮气分子解离为气态的电子和光子,即所谓等离子化,引起皮肤轻微的剥脱,在皮肤上形成表皮和真皮浅层可以控制的点阵形式的微小穿孔,形成“微剥脱区”[1]。目前,临床上微等离子体治疗细纹和痤疮后凹陷性瘢痕的效果较确切[2-3],但治疗的组织学变化和内在机制却不完全清楚。
本研究显示,微等离子体照射后即刻,表皮和真皮浅层出现非连续性气化区和热凝固区。Ⅲ型胶原在照射5d后开始明显增加,Ⅰ 型胶原在照射30d后开始明显增加,与临床疗效较为符合。推测胶原增加的原因可能为微等离子体对皮肤表皮的真皮浅层形成热损伤,引起机体的创伤修复机制,刺激胶原纤维增生。
此外,Ⅲ型胶原的增加是持续的,在观察终点,即术后180d发现Ⅲ型胶原仍然比未照射区的含量明显增加,与创伤愈合早期Ⅲ型胶原含量增多,随着时间推移其含量逐渐恢复正常的传统观点不符。本研究推测其可能的原因是微等离子体造成的创伤与一般的创伤不同,模式是微小而持续的,这样可以持续刺激机体产生新的胶原。
本研究首次观察了微等离子体作用于人体皮肤后胶原增生的时间变化规律,为微等离子体技术的临床治疗提供了重要的帮助。本研究显示,照射180d后,真皮的胶原纤维含量达到最大值,即在治疗后半年,微等离子体技术的胶原重排和增生作用才达到最优结果。目前,临床上该技术治疗痤疮后凹陷性瘢痕的治疗间隔一般为1~3个月,只是临床上的经验值,没有明确的组织病理学支持。本研究提示,微等离子体技术的临床治疗间隔时间半年更为合理。
微等离子体技术可能通过热损伤激活皮肤创伤修复过程来达到刺激真皮胶原增生的作用。热诱导的创伤修复可能涉及多种因子。越来越多的研究[4-5]表明,VEGF在增生期可能有助于伤口的愈合与组织修复。VEGF促进伤口愈合通过多种机制,包括胶原蛋白的沉积,血管生成等。本研究观察了VEGF在伤口愈合的不同阶段的动态变化。在微等离子体作用于皮肤1h后即可观察到VEGF水平明显高于对照组。此后VEGF的表达逐渐升高,照射28d后到达峰值。从理论上讲,VEGF诱导的血管舒张和血管通透性增加发生允许氧气和葡萄糖运送和沉积在伤口附近,可以认为VEGF可作为一种有效的血管扩张剂。本研究证实微等离子体技术引起的伤口愈合的早期阶段中血管内皮生长因子的作用。从成纤维细胞释放VEGF是缺氧依赖性的。在热损伤导致伤口愈合的重塑阶段,VEGF对胶原蛋白的直接影响仍有待确定。在本研究中,胶原蛋白均有显著增加,Ⅰ型胶原蛋白从照射28d后表达上调,Ⅲ型胶原蛋白从照射5d后表达上调。本研究发现,VEGF在创伤修复早期表达上调,与Ⅲ型胶原蛋白早期即可上调相吻合。因此,本研究推断Ⅲ型胶原蛋白的上调可能与VEGF有关。VEGF对伤口愈合中后期阶段的细胞外基质和瘢痕形成的影响,仍有进一步研究的需要。
热休克蛋白是细胞内蛋白质最丰富的蛋白质之一,但是它们是在正常生理条件下低水平表达。只有在应对各种压力的情况下热休克蛋白才明显上调。热休克蛋白的功能主要是作为分子伴侣促进其他细胞蛋白质的折叠,防止蛋白聚集,或诱发不当折叠的蛋白质降解。创伤诱导的热休克蛋白主要在表皮中上调。伤口中含有丰富的HSP蛋白通过维持细胞内环境动态平衡和细胞的存活,来促进伤口愈合[6]。其中HSP70是HSP家族较重要的一族。HSP70的过表达增加成纤维细胞的生存及减少氧化损伤并抑制炎症反应。
在本研究中,热休克蛋白在微等离子体照射皮肤3d后表达增加,主要表达于表皮和真皮浅层,此后HSP70信号进一步增强,照射7d后达到峰值,此后阳性反应逐渐降低,但是仍然高于未照射时,并持续约90d。本研究结果表明: HSP70在微等离子体技术照射皮肤后的全程均有作用。HSP70可以促进新生成的胶原蛋白的正确折叠,抑制真皮成纤维细胞的凋亡等。因此,微等离子体技术作用于人体皮肤后,HSP70可能是其中较重要的一个分子机制。本研究对微等离子体技术作用于人体皮肤后的HSP70的动态变化进行了观察,为微等离子体技术的治疗提供了重要的理论依据。但是其治疗还有许多其他分子参与,有待于进一步研究。
【参考文献】
[1] Halachmi S, Orenstein A, Meneghel T, et al. A novel fractional micro-plasma radio-frequency technology for the treatment of facial scars and rhytids: a pilot study[J]. J Cosmet Laser Ther, 2010,12(5): 208-212.
[2] 陆雯丽,张振,费烨,等.微等离子体与超脉冲CO2点阵激光治疗痤疮凹陷性瘢痕的对比研究[J].中华皮肤科杂志,2012,45(3): 165-168.
[3] 刘鹤,杨时昕.微等离子体射频技术联合长脉冲 1064nm Nd: YAG激光治疗增生性瘢痕的临床研究[J].中国医学创新,2014,10: 15-17.
[4] Asadi MR, Torkaman G, Hedayati M. Effect of sensory and motor electrical stimulation in vascular endothelial growth factor expression of muscle and skin in full-thickness wound[J]. J Rehabil Res Dev, 2011,48(3): 195-201.
[5] Spanholtz, TA, Theodorou P, Holzbach T, et al. Vascular endothelial growth factor(VEGF 165) plus basic fibroblast growth factor(bFGF) producing cells induce a mature and stable vascular network—a future therapy for ischemically challenged tissue[J]. J Surg Res, 2011,171(1): 329-338.
[6] Wagstaff MJ, Shah M, McGrouther DA, et al. The heat shock proteins and plastic surgery[J]. J Plast, Reconstr Aesthet Surg, 2007,60(9): 974-982.
Effects of microplasma radiofrequency technique on human skin tissue
【Abstract】Objective To investigate the effects of microplasma radiofrequency on human skin tissue. Methods Microplasma radiofrequency irradiation was performed on the left dorsal region of 3 healthy volunteers. Skin biopsies were taken from irradiated and non-irradiated regions immediately and 1, 3, 5, 7, 14, 28, 90, 180d after the treatment. H-E staining, Masson staining, and type Ⅰ/Ⅲ collagen, vascular endothelial growth factor(VEGF), heat shock proteins 70(HSP70)immunohistochemical stainings were performed. Results The radiofrequency ablative zone was wide and shallow with thermal coagulation. Collagen fibers started to increase 5d after treatment and maintained until d180. The expression of VEGF was elevated right after the treatment and maintained about 30d. The expression of HSP70 was increased 3d after treatment, mainly in epidermis and papillary dermis; it reached to the peak on d7 and maintained about 90d, then decreased. Conclusion Microplasma radiofrequency can stimulate the long-term proliferation of collagen fibers and elastic fibers in human dermis. The study may provide a theoretical basis for microplasma radiofrequency technique in treatment of depressed scars.
【Key words】microplasma; collagen; vascular endothelial growth factor; heat shock proteins 70
doi:10.16118/j.1008-0392.2016.05.008
收稿日期:2016-01-15
【中图分类号】R 751
【文献标志码】A
【文章编号】1008-0392(2016)05-0040-04